Clear Sky Science · zh
慢性应激通过肠道微生物—维生素—Sting1/Slc9c2 轴导致少弱精症
当压力影响到生殖系统
大多数人知道慢性应激会消耗精力、扰乱睡眠并影响情绪,但很少有人意识到它也可能悄然损害男性生育力。这项大鼠研究揭示了长期心理应激如何通过干扰肠道微生物及其提供的维生素,降低精子数量和活动力——而不仅仅是通过激素途径。该研究指出了大脑、肠道与睾丸之间一条隐蔽的沟通通路,并提示未来通过支持有益菌群与关键营养素或许能帮助在承受压力的男性中保护生育能力。
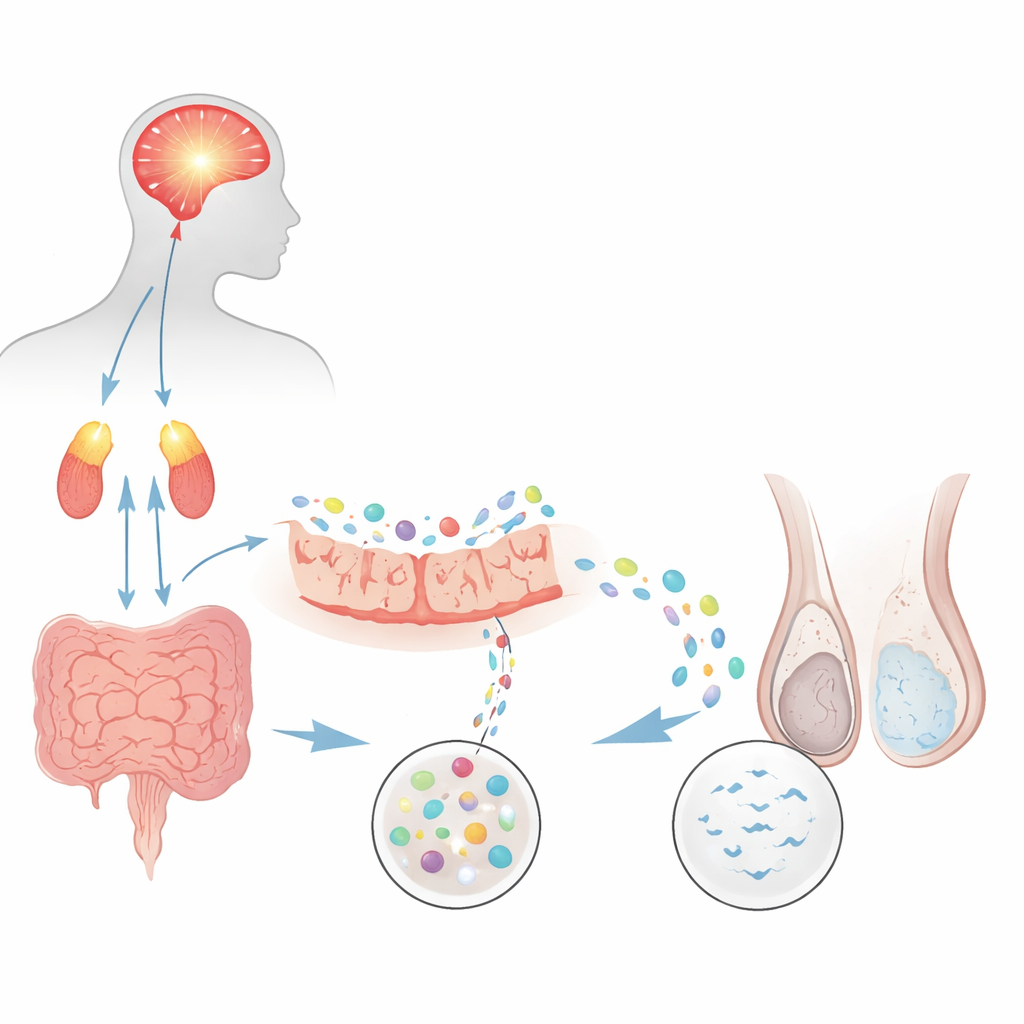
从精神负担到精子减少
研究者首先检验一种成熟的大鼠慢性心理应激模型是否能模拟一种常见的男性不育形式——少弱精症,即精子既稀少又活动力不足。反复强制游泳的老鼠出现明显的焦虑和抑郁行为,并伴随脑—肾上腺系统分泌的应激激素升高。用自动化手段检测精液时,应激组动物的精子浓度约为对照组的一半且活动力显著降低。睾丸内与精子发生相关的标志物也下降,交配试验显示妊娠率与胎窝数减少。综上,这些发现表明,持续的应激本身即可损害精子生成与功能。
肠道作为中介
由于肠道对应激激素高度敏感,研究团队接着观察了肠道。在应激大鼠中,通常紧密封闭肠上皮的蛋白连接被削弱,提示肠道屏障出现“通透性”增加。用药物阻断糖皮质激素受体——应激激素的主要作用位点——在很大程度上恢复了肠道完整性与精子质量,将损害归因于激素信号。为检验肠道微生物本身是否参与病因,科学家将来自应激或对照供体的粪菌移植到先用抗生素清除自身菌群的新鼠体内。接受应激供体微生物的动物尽管自身未受应激,也出现相同的低精子数、低活动力与生育力下降,表明受扰动的肠道群落可以远距离驱动生殖问题。
一种有益细菌与缺失的维生素
微生物 DNA 分析显示,慢性应激降低了小肠的整体多样性,尤其耗损了乳酸杆菌属(Lactobacillus),这一类菌常与肠道和生殖健康相关。此类微生物的丰度与精子数量和活动力高度相关。当在应激期间持续口服乳酸杆菌时,应激大鼠的精液质量和睾丸标志物有所改善,生育结果也向正常靠拢。与此同时,对肠内容物、血液和睾丸的化学分析显示,应激扰乱了胆汁酸和脂溶性维生素代谢,尤其是维生素 A 与 E,这些维生素对生殖细胞发育与抵御氧化损伤很重要。循环与睾丸组织中若干胆汁酸和这些维生素的水平下降,这些下降与乳酸杆菌减少以及精子参数恶化密切相关。
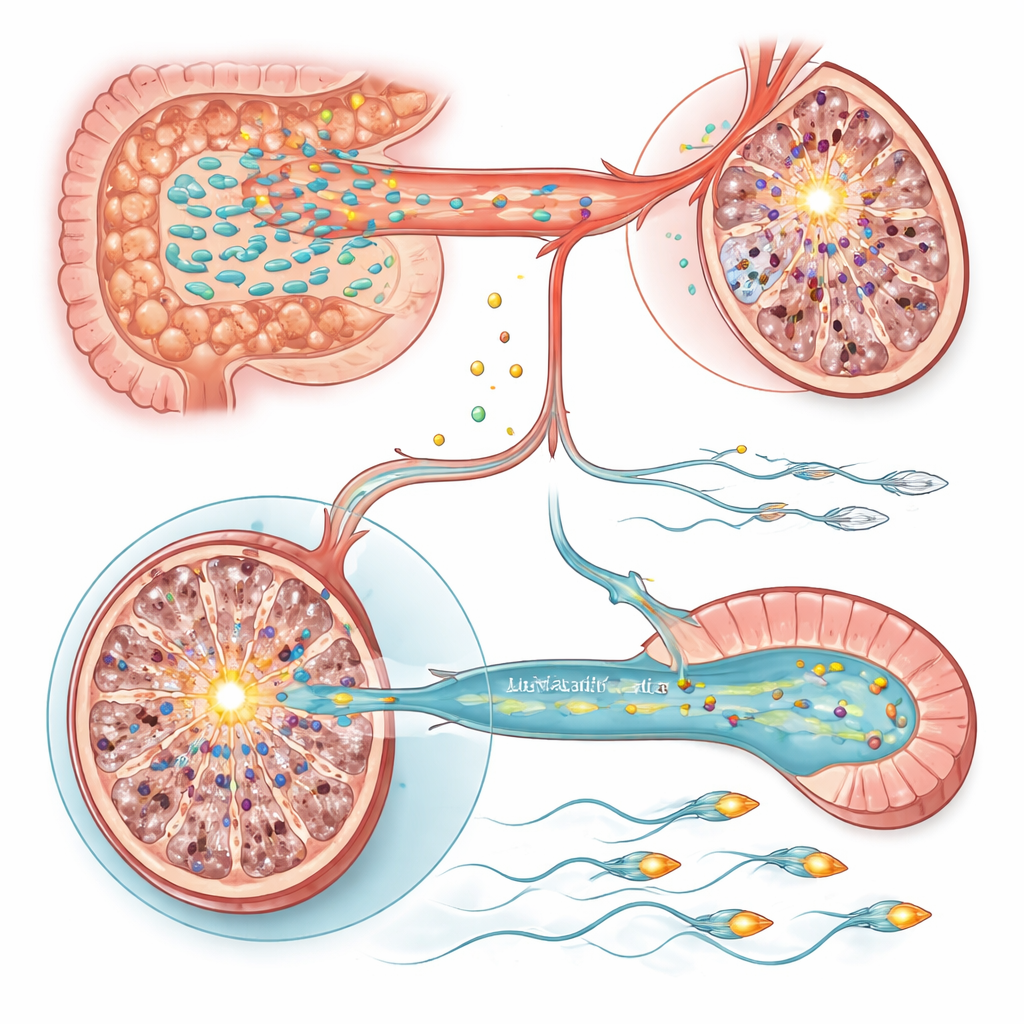
睾丸与精子中的两个分子开关
为了解这些代谢改变如何影响细胞,团队检查了睾丸与附睾(精子成熟之处)的基因表达。在应激大鼠的睾丸中,一个基因尤为突出:Sting1,这是先天免疫与细胞死亡通路的主控开关,显著激活。人工在健康动物中增强 Sting1 的表达就足以降低精子生成,而在应激大鼠中沉默该基因则部分挽救了精子数量。乳酸杆菌治疗和维生素 A、E 补充都能使 Sting1 表达回落,将微生物驱动的维生素平衡与这一炎症开关联系起来。相反,精子运动能力下降可追溯至附睾,在那里名为 Slc9c2 的基因被抑制,该基因编码精子特异的离子交换蛋白 NHE11,帮助控制细胞内 pH 与鞭毛功能。NHE11 水平下降与精子运动减弱及受精所需激活步骤受损相关。恢复 Slc9c2 表达,或补充乳酸杆菌或维生素 A/E,均能改善运动能力,而实验性敲低 Slc9c2 则抹去了这些改善效果。
这对承受压力的男性意味着什么
综合来看,这项研究勾勒出一条从慢性心理压力到精子减少与活性下降的事件链。应激激素削弱肠道屏障并减少有益的乳酸杆菌群,进而扰乱胆汁酸和维生素 A、E 的平衡。这些营养变化通过激活睾丸中的 Sting1 细胞死亡通路削减精子生成,并通过降低附睾中 NHE11 活性减慢精子尾部运动。尽管该研究在大鼠中完成,且仍需更多人体研究,但它将某些男性不育病例重新框定为涉及大脑、肠道微生物、营养与生殖器官的全身性状况。研究还提出了这样的可能性:结合压力管理,精心设计的益生菌与维生素策略或许有朝一日能帮助保护或恢复长期承受心理应激男性的生育能力。
引用: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
关键词: 男性不育, 慢性应激, 肠道微生物群, 维生素 A 与 E, 精子运动能力