Clear Sky Science · ar
الإجهاد المزمن يقود إلى قلة عدد وحركة الحيوانات المنوية عبر محور ميكروبيوتا الأمعاء-الفيتامين-ِSting1/Slc9c2
عندما يصل الإجهاد إلى الجهاز التناسلي
يعلم معظم الناس أن الإجهاد المزمن يمكن أن يستنزف الطاقة ويعكر النوم ويؤثر على المزاج، لكن القليل يدرك أنه قد يقوض خصوبة الذكور بهدوء أيضاً. تكشف هذه الدراسة في الفئران كيف يمكن للإجهاد النفسي طويل الأمد أن يقلل عدد الحيوانات المنوية وحركتها، ليس فقط عبر الهرمونات، وإنما عن طريق إحداث خلل في ميكروبات الأمعاء والفيتامينات التي تساعد هذه الميكروبات في توفيرها. تشير الدراسة إلى وجود خط اتصال خفي بين الدماغ والأمعاء والخصيتين، وتقترح أن دعم البكتيريا المفيدة والمغذيات الأساسية قد يساعد في المستقبل على حماية الخصوبة لدى الرجال المتعرضين للإجهاد.
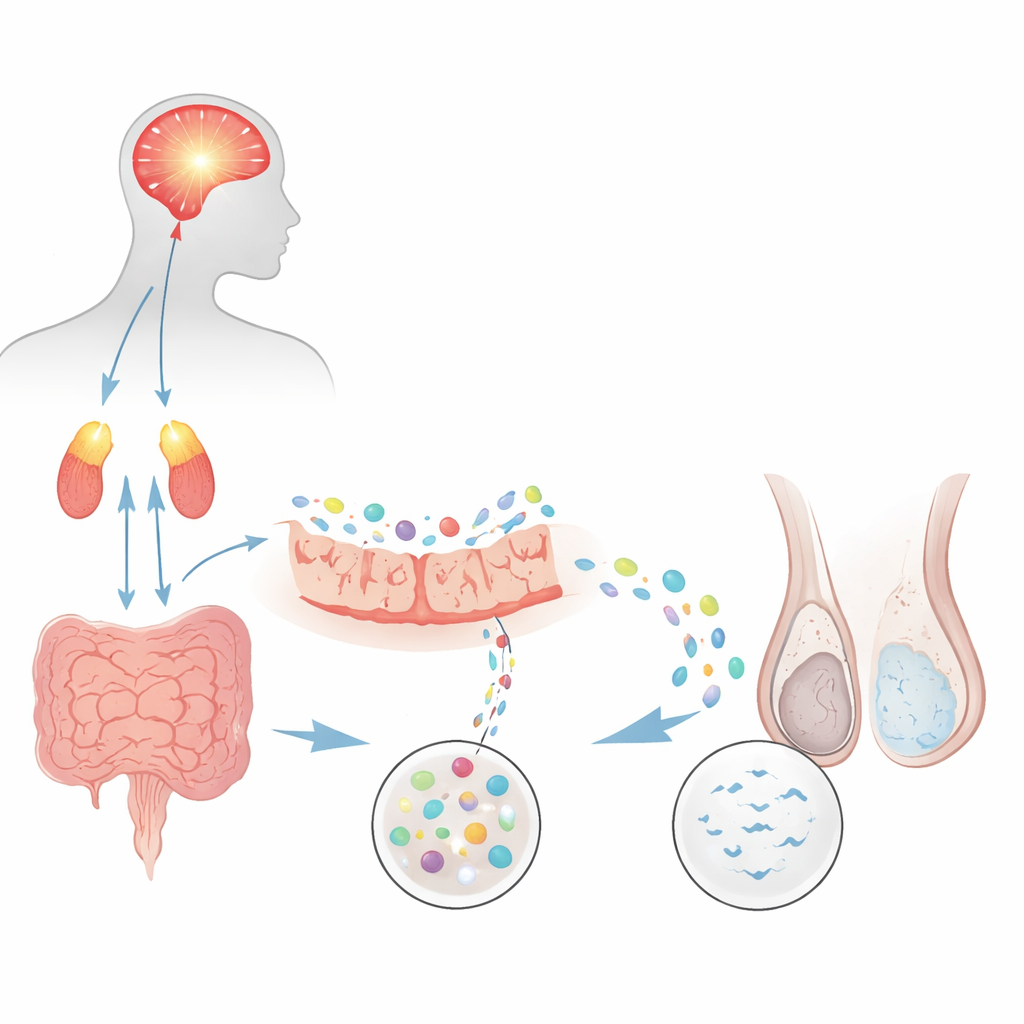
من الضغط النفسي إلى قلة الحيوانات المنوية
سأل الباحثون أولاً ما إذا كان نموذج الفئران المعروف للإجهاد النفسي المزمن يمكن أن يحاكي شكلًا شائعًا من عقم الذكور يُسمى قلة حركة وعدد الحيوانات المنوية (oligoasthenozoospermia)، حيث يكون عدد الحيوانات المنوية قليلاً وحركتها بطيئة. الفئران التي تعرضت مراراً للسباحة القسرية طورت علامات قوية للقلق والاكتئاب، إلى جانب ارتفاع هرمونات الإجهاد من محور الدماغ-الغدة الكظرية. عند فحص سائلاً منوياً آلياً، كان لدى الحيوانات المتعرضة للإجهاد نحو نصف تركيز الحيوانات المنوية وحركة أقل بكثير مقارنة بالمجموعات الضابطة. كما انخفضت مؤشرات تطور الحيوانات المنوية داخل الخصيتين، وأظهرت اختبارات التزاوج حالات حمل أقل وذراري أصغر. مجتمعة، أوضحت هذه النتائج أن الإجهاد المستمر وحده يمكن أن يضر بإنتاج الحيوانات المنوية وأدائها.
الأمعاء كوسيط
بما أن القناة المعوية حساسة للغاية لهرمونات الإجهاد، فحص الفريق بعد ذلك الأمعاء. في الفئران المتعرضة للإجهاد، كانت البروتينات التي تغلق بطانة الأمعاء أضعف، مما يشير إلى حاجز معوي «مسرب». إن حجب مستقبل الجلوكوكورتيكويد—وهو نقطة الالتحام الرئيسية لهرمونات الإجهاد—بواسطة دواء أعاد إلى حد كبير كل من سلامة الأمعاء وجودة الحيوانات المنوية، مما ربط الضرر بالإشارات الهرمونية. لاختبار ما إذا كانت ميكروبات الأمعاء نفسها جزءاً من المشكلة، زرع العلماء بكتيريا برازية من متبرعين متوترين أو ضوابط إلى فئران جديدة أُزيلت ميكروبيوتاها بمضادات حيوية. الحيوانات التي تلقت ميكروبات من متبرعين متوترين طورت نفس انخفاضات عدد الحيوانات المنوية وضعف الحركة وقلة الخصوبة، على الرغم من أنها لم تتعرض للإجهاد قط، كاشفة أن المجتمعات المعوية المضطربة يمكن أن تسبب مشكلات تناسلية عن بعد.
بكتيريا مفيدة وفيتامينات مفقودة
أظهر تحليل حمض نووي ميكروبي أن الإجهاد المزمن قلل التنوع العام في الأمعاء الدقيقة وخاصة قلل من عشيرة اللاكتوباسيلس، وهي مجموعة بكتيرية غالباً ما ترتبط بصحة الأمعاء والتكاثر. وتابعت وفرة هذه الميكروبات ارتباطها القوي مع عدد الحيوانات المنوية وحركتها. عندما أعطي اللاكتوباسيلس عن طريق الفم للفئران المتعرضة للإجهاد طوال فترة التعرض، تحسنت جودة السائل المنوي ومؤشرات الخصية، وعادت نتائج الخصوبة إلى الاقتراب من الطبيعي. في الوقت نفسه، كشفت التحليلات الكيميائية لمحتويات الأمعاء والدم والخصيتين أن الإجهاد عطل أحماض الصفراء والفيتامينات الذائبة في الدهون، وخاصة فيتامينات أ و هـ، المهمة لتطور الخلايا الجرثومية والحماية من التلف التأكسدي. انخفضت مستويات عدة أحماض صفراوية وهذه الفيتامينات في الدورة الدموية وفي نسيج الخصية، وكانت هذه الانخفاضات مرتبطة ارتباطاً وثيقاً بفقدان اللاكتوباسيلس وتدهور مؤشرات الحيوانات المنوية.
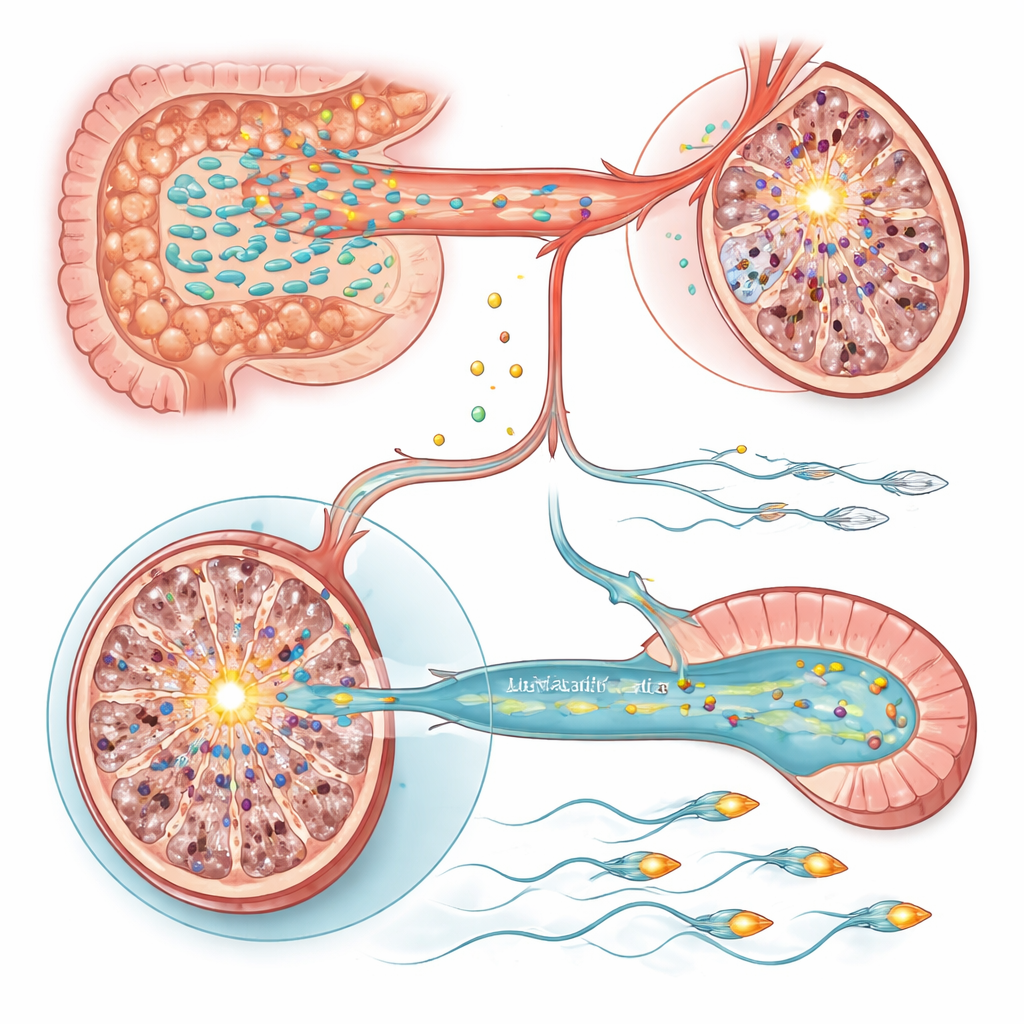
مفتاحان جزيئيان في الخصية والحيوانات المنوية
لفهم كيف تغير هذه التغيرات الأيضية الخلايا، فحص الفريق نشاط الجينات في الخصيتين والوباء (epididymis)، حيث تنضج الحيوانات المنوية. في خصيتي الفئران المتعرضة للإجهاد، برز جين واحد: Sting1، مفتاح رئيسي في مسارات المناعة الفطرية وموت الخلايا، كان مفعلًا بشدة. زيادة Sting1 اصطناعياً في حيوانات سليمة كافية لتقليل إنتاج الحيوانات المنوية، بينما أدى إسكاتها في الفئران المتوترة إلى إنقاذ جزئي لأعداد الحيوانات المنوية. كل من علاج اللاكتوباسيلس وتكميل فيتامينات أ و هـ خففا من تنشيط Sting1، رابطين توازن الفيتامينات الناجم عن الميكروبات بهذا المفتاح الالتهابي. بالمقابل، عُزو انخفاض حركة الحيوانات المنوية إلى الوباء، حيث تم قمع جين يُدعى Slc9c2، المشفر لمبادل الأيونات الخاص بالحيوانات المنوية NHE11 الذي يساعد على التحكم في الحموضة الداخلية ووظيفة الذيل، بفعل الإجهاد. ارتبط انخفاض NHE11 بحركة حيوانات منوية أضعف وقدرة منخفضة على إجراء خطوات التفعيل اللازمة للإخصاب. إن استعادة تعبير Slc9c2، أو مكملات اللاكتوباسيلس أو فيتامينات أ/هـ، حسنت الحركة، فيما أزال التثبيط التجريبي لـSlc9c2 هذه التحسينات.
ماذا يعني هذا للرجال تحت الضغط
توصّف الدراسة مجتمعة سلسلة من الأحداث تبدأ بالضغط النفسي المزمن وتنتهي بقلة وعدد أقل نشاطاً من الحيوانات المنوية. تضعف هرمونات الإجهاد حاجز الأمعاء وتقلل مجموعات اللاكتوباسيلس المفيدة، مما يعطل أحماض الصفراء والفيتامينات أ و هـ. تؤدي تغييرات هذه المغذيات إلى تفعيل مسار موت الخلايا في الخصية عبر Sting1، مما يقلل إنتاج الحيوانات المنوية، وتضعف نشاط NHE11 في الوباء، مما يبطئ ذيول الحيوانات المنوية. على الرغم من أن العمل أُجري على الفئران وهناك حاجة لمزيد من الأبحاث في البشر، فإنه يعيد تأطير بعض حالات عقم الذكور كحالة جهازية تشمل الدماغ وميكروبات الأمعاء والمغذيات والأعضاء التناسلية. كما يفتح الاحتمال أمام أن تساعد استراتيجيات بروبيوتيك وفيتامين مدروسة بعناية، إلى جانب إدارة الإجهاد، في المستقبل على حماية أو استعادة الخصوبة لدى الرجال الذين يعانون من ضغط نفسي مزمن.
الاستشهاد: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
الكلمات المفتاحية: عقم الذكور, الإجهاد المزمن, ميكروبيوتا الأمعاء, الفيتامينات أ و هـ, حركة الحيوان المنوي