Clear Sky Science · es
El estrés crónico provoca oligoastenozoospermia a través del eje microbiota intestinal–vitaminas–Sting1/Slc9c2
Cuando el estrés alcanza el sistema reproductor
La mayoría sabe que el estrés crónico puede agotar la energía, alterar el sueño y empañar el ánimo, pero pocos se imaginan que también puede socavar silenciosamente la fertilidad masculina. Este estudio en ratas descubre cómo el estrés psicológico prolongado puede reducir el recuento y el movimiento de los espermatozoides, no solo a través de hormonas, sino alterando los microbios intestinales y las vitaminas que estos ayudan a suministrar. El trabajo señala una línea de comunicación oculta entre el cerebro, el intestino y los testículos, y sugiere que apoyar a las bacterias beneficiosas y a nutrientes clave podría algún día ayudar a proteger la fertilidad en hombres estresados.
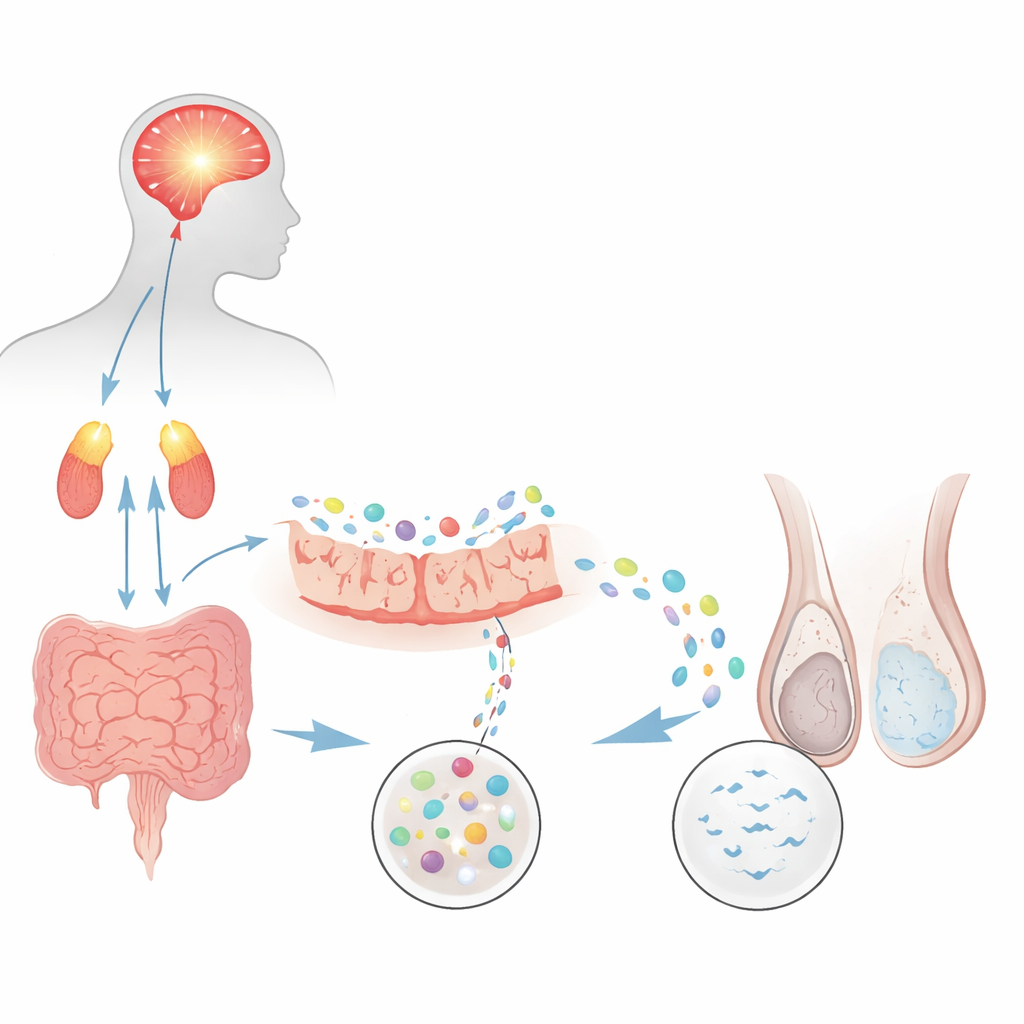
Del esfuerzo mental a menos espermatozoides
Los investigadores plantearon primero si un modelo bien establecido de estrés psicológico crónico en ratas podría imitar una forma común de infertilidad masculina llamada oligoastenozoospermia, en la que los espermatozoides son a la vez escasos y lentos. Las ratas expuestas repetidamente a natación forzada desarrollaron signos marcados de ansiedad y depresión, junto con hormonas del estrés elevadas procedentes del eje cerebro‑suprarrenal. Al examinar su semen con herramientas automatizadas, los animales estresados tenían aproximadamente la mitad de la concentración de espermatozoides y una motilidad notablemente menor en comparación con los controles. También descendieron marcadores de desarrollo espermático dentro de los testículos, y las pruebas de apareamiento mostraron menos embarazos y camadas más pequeñas. En conjunto, estos hallazgos demostraron que el estrés persistente por sí solo puede dañar la producción y el rendimiento espermático.
El intestino como intermediario
Dado que el tracto intestinal es muy sensible a las hormonas del estrés, el equipo examinó a continuación el intestino. En las ratas estresadas, las proteínas que sellan normalmente el revestimiento intestinal se debilitaron, lo que sugiere una barrera “permeable”. Bloquear el receptor de glucocorticoides—el principal punto de unión de las hormonas del estrés—con un fármaco restauró en gran medida tanto la integridad intestinal como la calidad del semen, vinculando el daño con la señalización hormonal. Para probar si los microbios intestinales eran parte del problema, los científicos transplantaron bacterias fecales de donantes estresados o controles a nuevas ratas cuyo propio microbioma había sido eliminado con antibióticos. Los animales que recibieron microbios de donantes estresados desarrollaron los mismos recuentos espermáticos bajos, baja motilidad y fertilidad reducida, a pesar de no haber sido estresados nunca, lo que revela que las comunidades intestinales alteradas pueden provocar problemas reproductivos a distancia.
Una bacteria útil y vitaminas ausentes
El análisis del ADN microbiano mostró que el estrés crónico redujo la diversidad global en el intestino delgado y, en particular, agotó Lactobacillus, un grupo de bacterias a menudo asociado con la salud intestinal y reproductiva. La abundancia de estos microbios se correlacionó fuertemente con los recuentos y la motilidad espermática. Cuando a las ratas estresadas se les administró Lactobacillus por vía oral durante todo el periodo de estrés, la calidad de su semen y los marcadores testiculares mejoraron, y los resultados de fertilidad volvieron hacia la normalidad. Al mismo tiempo, los análisis químicos del contenido intestinal, la sangre y los testículos revelaron que el estrés alteró los ácidos biliares y las vitaminas liposolubles, especialmente las vitaminas A y E, importantes para el desarrollo de las células germinales y la protección contra el daño oxidativo. Los niveles de varios ácidos biliares y de estas vitaminas descendieron en la circulación y en el tejido testicular, y estas caídas se relacionaron estrechamente tanto con la pérdida de Lactobacillus como con el empeoramiento de los parámetros espermáticos.
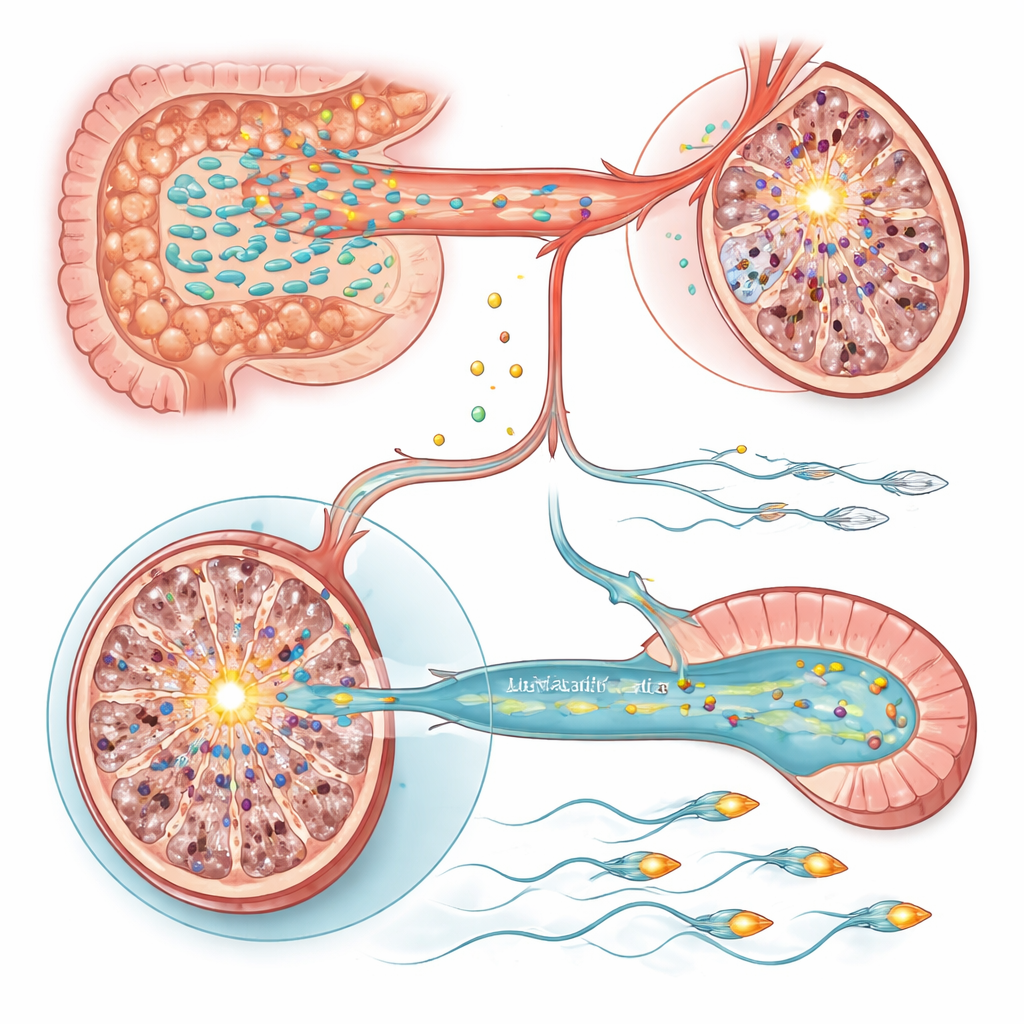
Dos interruptores moleculares en testículo y esperma
Para entender cómo estos cambios metabólicos alteran las células, el equipo examinó la actividad génica en los testículos y el epidídimo, donde maduran los espermatozoides. En los testículos de ratas estresadas destacó un gen: Sting1, un interruptor maestro en las vías inmunitarias innatas y de muerte celular, estaba fuertemente activado. Potenciar artificialmente Sting1 en animales por lo demás sanos fue suficiente para reducir la producción de espermatozoides, mientras que silenciarlo en ratas estresadas rescató parcialmente el número de espermatozoides. Tanto el tratamiento con Lactobacillus como la suplementación con vitaminas A y E redujeron la actividad de Sting1, vinculando el equilibrio microbiano‑vitamínico a este interruptor inflamatorio. En contraste, la reducción de la motilidad espermática se rastreó hasta el epidídimo, donde un gen llamado Slc9c2, que codifica el intercambiador iónico específico del esperma NHE11 y ayuda a controlar el pH interno y la función de la cola, fue suprimido por el estrés. Menos NHE11 se asoció con un movimiento espermático más débil y una capacidad deteriorada para sufrir los pasos de activación necesarios para la fertilización. Restaurar la expresión de Slc9c2, o suplementar con Lactobacillus o vitaminas A/E, mejoró la motilidad, y la interferencia experimental de Slc9c2 borró estas mejoras.
Qué significa esto para los hombres bajo presión
En conjunto, el estudio traza una cadena de eventos que comienza con la tensión psicológica crónica y termina con espermatozoides menos numerosos y menos activos. Las hormonas del estrés debilitan la barrera intestinal y reducen las poblaciones beneficiosas de Lactobacillus, que a su vez alteran los ácidos biliares y las vitaminas A y E. Estos cambios de nutrientes activan una vía de muerte celular en los testículos a través de Sting1, reduciendo la producción de esperma, y atenúan la actividad de NHE11 en el epidídimo, frenando las colas espermáticas. Aunque el trabajo se realizó en ratas y se necesitan más estudios en humanos, replantea ciertos casos de infertilidad masculina como una condición de todo el organismo que involucra cerebro, microbios intestinales, nutrientes y órganos reproductores. También plantea la posibilidad de que estrategias bien diseñadas de probióticos y vitaminas, junto con el manejo del estrés, puedan algún día ayudar a proteger o restaurar la fertilidad en hombres que viven con estrés psicológico crónico.
Cita: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
Palabras clave: infertilidad masculina, estrés crónico, microbiota intestinal, vitaminas A y E, motilidad espermática