Clear Sky Science · nl
Chronische stress veroorzaakt oligoasthenozoöspermie via de darmmicrobiota‑vitamine‑Sting1/Slc9c2‑as
Wanneer stress het voortplantingssysteem bereikt
De meeste mensen weten dat chronische stress energie kan uitputten, slaap kan verstoren en stemming kan vertroebelen, maar weinigen beseffen dat het ook stilletjes de mannelijke vruchtbaarheid kan ondermijnen. Deze studie bij ratten onthult hoe langdurige psychologische stress het spermaaantal en de beweging kan verminderen, niet alleen via hormonen, maar ook door verstoring van darmmicroben en de vitaminen die zij helpen leveren. Het werk wijst op een verborgen communicatielijn tussen de hersenen, de darm en de testikels — en suggereert dat het ondersteunen van gunstige bacteriën en belangrijke voedingsstoffen mogelijk kan helpen om de vruchtbaarheid bij gestreste mannen te beschermen.
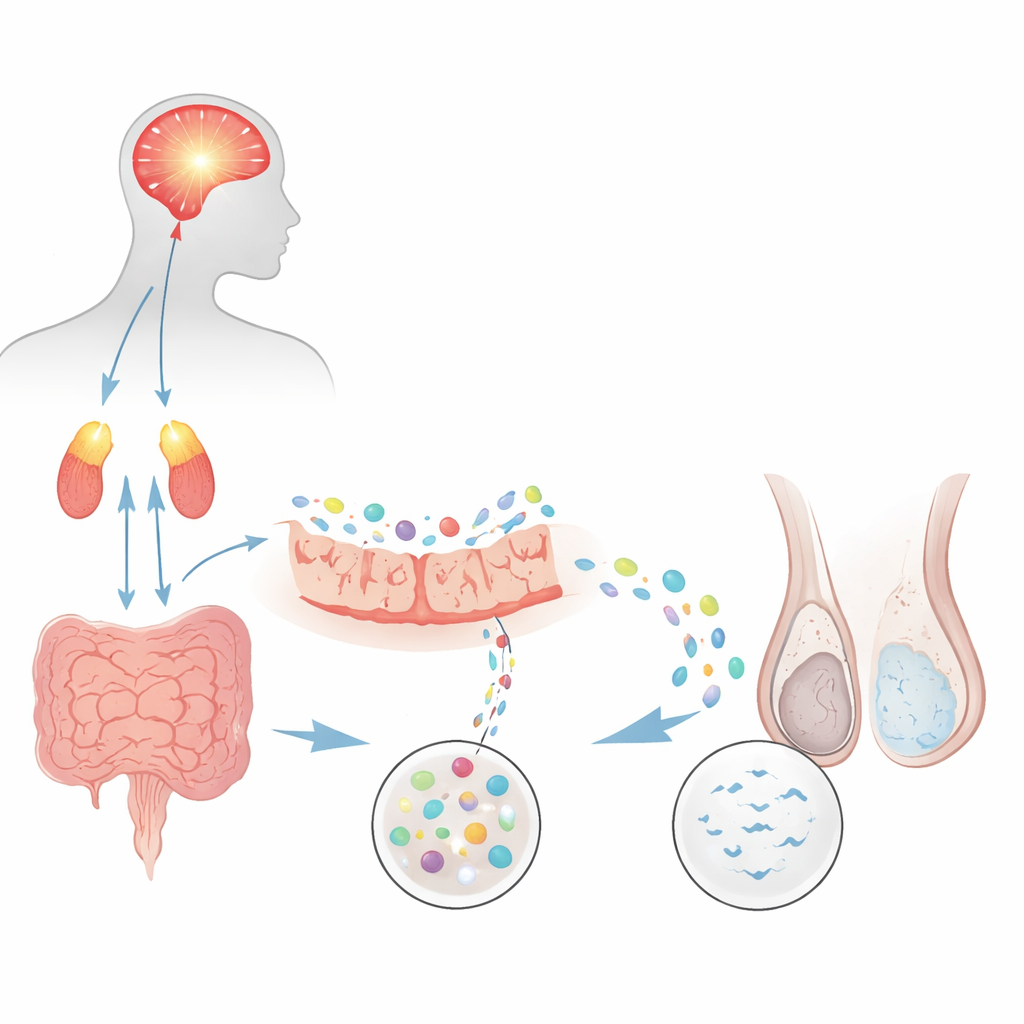
Van mentale belasting naar minder zaadcellen
De onderzoekers vroegen zich eerst af of een goed vastgesteld rattenmodel van chronische psychologische stress een veelvoorkomende vorm van mannelijke onvruchtbaarheid, oligoasthenozoöspermie — waarbij zaadcellen zowel te weinig als te traag zijn — kon nabootsen. Ratten die herhaaldelijk aan gedwongen zwemmen werden blootgesteld, ontwikkelden sterke tekenen van angst en depressie, samen met verhoogde stresshormonen uit het hersen‑bijnierstelsel. Bij onderzoek van hun sperma met automatische hulpmiddelen hadden gestreste dieren ruwweg de helft van de zaadconcentratie en veel lagere motiliteit vergeleken met controles. Merkers van zaadcelontwikkeling in de testikels daalden ook, en paringstests lieten minder drachtigheidsgevallen en kleinere worpen zien. Samen tonen deze bevindingen aan dat aanhoudende stress op zichzelf de zaadproductie en -prestaties kan beschadigen.
De darm als tussenpersoon
Aangezien het darmkanaal zeer gevoelig is voor stresshormonen, richtte het team zich vervolgens op de darm. Bij gestreste ratten waren de eiwitverbindingen die de darmwand normaal afsluiten verzwakt, wat wijst op een “lekkende” barrière. Het blokkeren van de glucocorticoïdreceptor — het belangrijkste aangrijpingspunt voor stresshormonen — met een geneesmiddel herstelde grotendeels zowel de integriteit van de darm als de spermakwaliteit, waarmee de schade aan hormoonsignalering werd gekoppeld. Om te testen of darmmicroben zelf deel van het probleem waren, transplantaten van fecale bacteriën van gestreste of controledonoren werden overgebracht naar nieuwe ratten waarvan de eigen microbiota door antibiotica waren uitgewist. Dieren die microben van gestreste donoren ontvingen, ontwikkelden dezelfde slechte zaadtellingen, lage motiliteit en verminderde vruchtbaarheid, hoewel ze nooit zelf gestrest waren geweest, wat toont dat verstoorde darmgemeenschappen op afstand voortplantingsproblemen kunnen veroorzaken.
Een behulpzame bacterie en ontbrekende vitaminen
Microbieel DNA‑profielonderzoek toonde aan dat chronische stress de algehele diversiteit in de dunne darm verminderde en in het bijzonder Lactobacillus uitdaagde — een groep bacteriën die vaak wordt geassocieerd met darm‑ en voortplantingsgezondheid. De aanwezigheid van deze microben correleerde sterk met zaadtelling en motiliteit. Toen gestreste ratten gedurende de stressperiode oraal Lactobacillus kregen, verbeterden hun spermakwaliteit en testismerkers, en keerden de vruchtbaarheidsuitkomsten grotendeels terug naar normaal. Tegelijkertijd toonden chemische analyses van darminhoud, bloed en testikels aan dat stress galzuren en vetoplosbare vitaminen verstoorde, met name de vitaminen A en E, die belangrijk zijn voor de ontwikkeling van kiemcellen en bescherming tegen oxidatieve schade. De niveaus van meerdere galzuren en deze vitaminen daalden in de circulatie en in testiculair weefsel, en deze teruglopen waren nauw verbonden met zowel het verlies van Lactobacillus als met verslechterende zaadparameters.
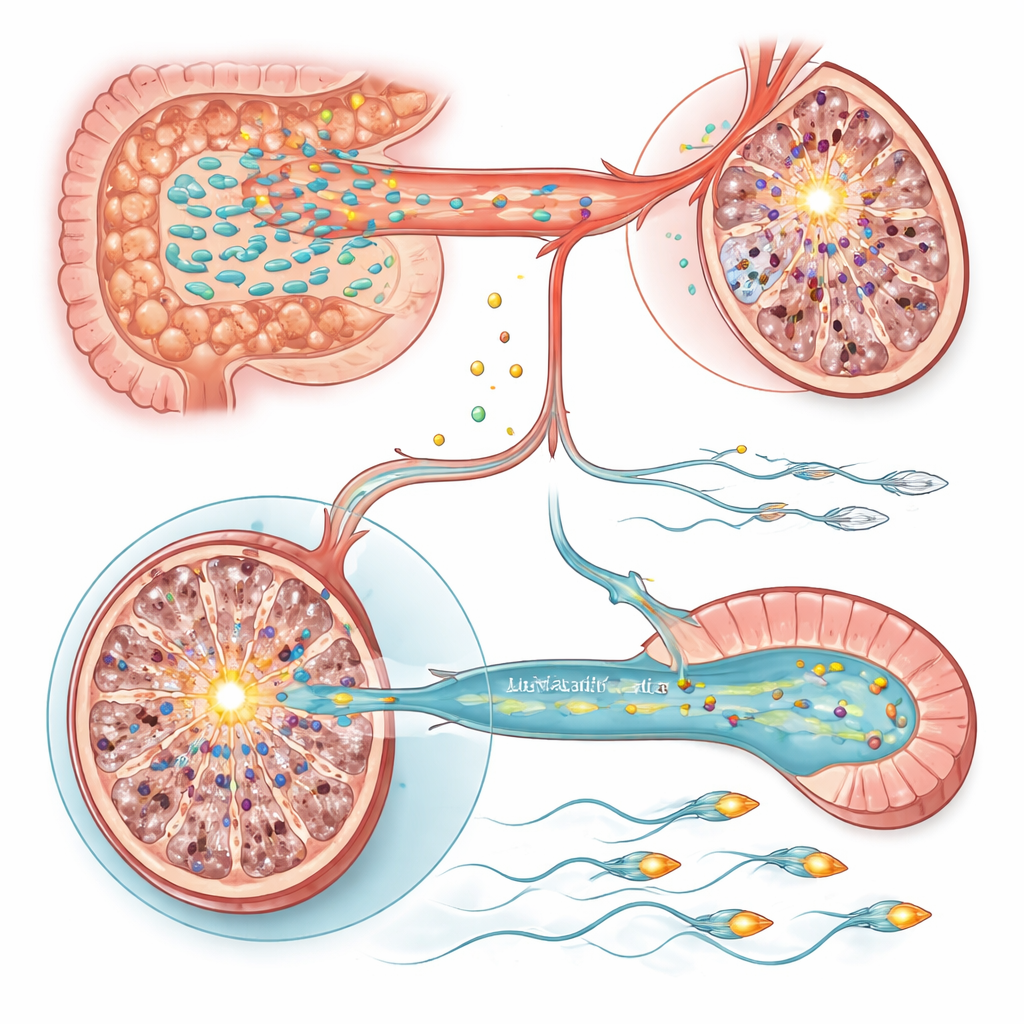
Twee moleculaire schakelaars in testis en spermatozoa
Om te begrijpen hoe deze metabole veranderingen cellen beïnvloeden, onderzocht het team genexpressie in de testikels en epididymis, waar zaadcellen rijpen. In de testikels van gestreste ratten stak één gen erbovenuit: Sting1, een hoofdschakelaar in aangeboren immuun‑ en celdoodroutes, was sterk geactiveerd. Kunstmatig verhogen van Sting1 in anderszins gezonde dieren volstond om de zaadproductie te verminderen, terwijl het stilleggen ervan in gestreste ratten de zaadcelaantallen deels herstelde. Zowel behandeling met Lactobacillus als suppletie met vitaminen A en E dempten Sting1, waarmee de door microben aangedreven vitaminenbalans aan deze inflammatoire schakel werd gekoppeld. In contrast daarmee was de verminderde zaadmotiliteit te herleiden tot de epididymis, waar een gen genaamd Slc9c2, dat de zaadspecifieke ionenuitwisselaar NHE11 codeert die helpt de interne pH en staartfunctie te regelen, door stress werd onderdrukt. Lager NHE11 hield verband met zwakkere zaadbeweging en een verminderde capaciteit om activatiestappen te doorlopen die nodig zijn voor bevruchting. Het herstellen van Slc9c2‑expressie, of het toedienen van Lactobacillus of vitaminen A/E, verbeterde de motiliteit, en experimenteel neerhalen van Slc9c2 maakte deze verbeteringen ongedaan.
Wat dit betekent voor onder druk staande mannen
Gezamenlijk schetst de studie een keten van gebeurtenissen die begint met chronische psychologische belasting en eindigt met minder en minder actieve zaadcellen. Stresshormonen verzwakken de darmbarrière en doen gunstige Lactobacillus‑populaties krimpen, wat op zijn beurt galzuren en de vitaminen A en E verstoort. Deze voedingsverschuivingen schakelen via Sting1 een celdoodpad in de testikels in, waardoor de zaadproductie daalt, en verminderen de activiteit van NHE11 in de epididymis, waardoor staarten van zaadcellen trager worden. Hoewel het werk bij ratten is uitgevoerd en meer onderzoek bij mensen nodig is, plaatst het bepaalde gevallen van mannelijke onvruchtbaarheid in een nieuw licht als een geheel‑organismeprobleem waarin hersenen, darmmicroben, voedingsstoffen en voortplantingsorganen samenhangen. Het vergroot ook de mogelijkheid dat zorgvuldig samengestelde probiotische en vitamine‑strategieën, naast stressmanagement, op termijn kunnen helpen de vruchtbaarheid te beschermen of te herstellen bij mannen die leven met chronische psychologische stress.
Bronvermelding: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
Trefwoorden: mannelijke onvruchtbaarheid, chronische stress, darmmicrobiota, vitamine A en E, zaadcelmotiliteit