Clear Sky Science · de
Chronischer Stress verursacht Oligoasthenozoospermie über die Darmmikrobiota‑Vitamin‑Sting1/Slc9c2‑Achse
Wenn Stress das Fortpflanzungssystem erreicht
Die meisten Menschen wissen, dass chronischer Stress Energie rauben, den Schlaf stören und die Stimmung trüben kann, doch nur wenige ahnen, dass er auch still die männliche Fruchtbarkeit untergraben kann. Diese Studie an Ratten zeigt, wie anhaltender psychischer Stress Spermienanzahl und -bewegung verringern kann — nicht nur über hormonelle Wege, sondern durch die Störung der Darmmikroben und der von ihnen mitbeeinflussten Vitamine. Die Arbeit weist auf eine verborgene Kommunikationslinie zwischen Gehirn, Darm und Hoden hin und legt nahe, dass die Unterstützung nützlicher Bakterien und wichtiger Nährstoffe eines Tages helfen könnte, die Fruchtbarkeit gestresster Männer zu schützen.
Vom psychischen Druck zu weniger Spermien
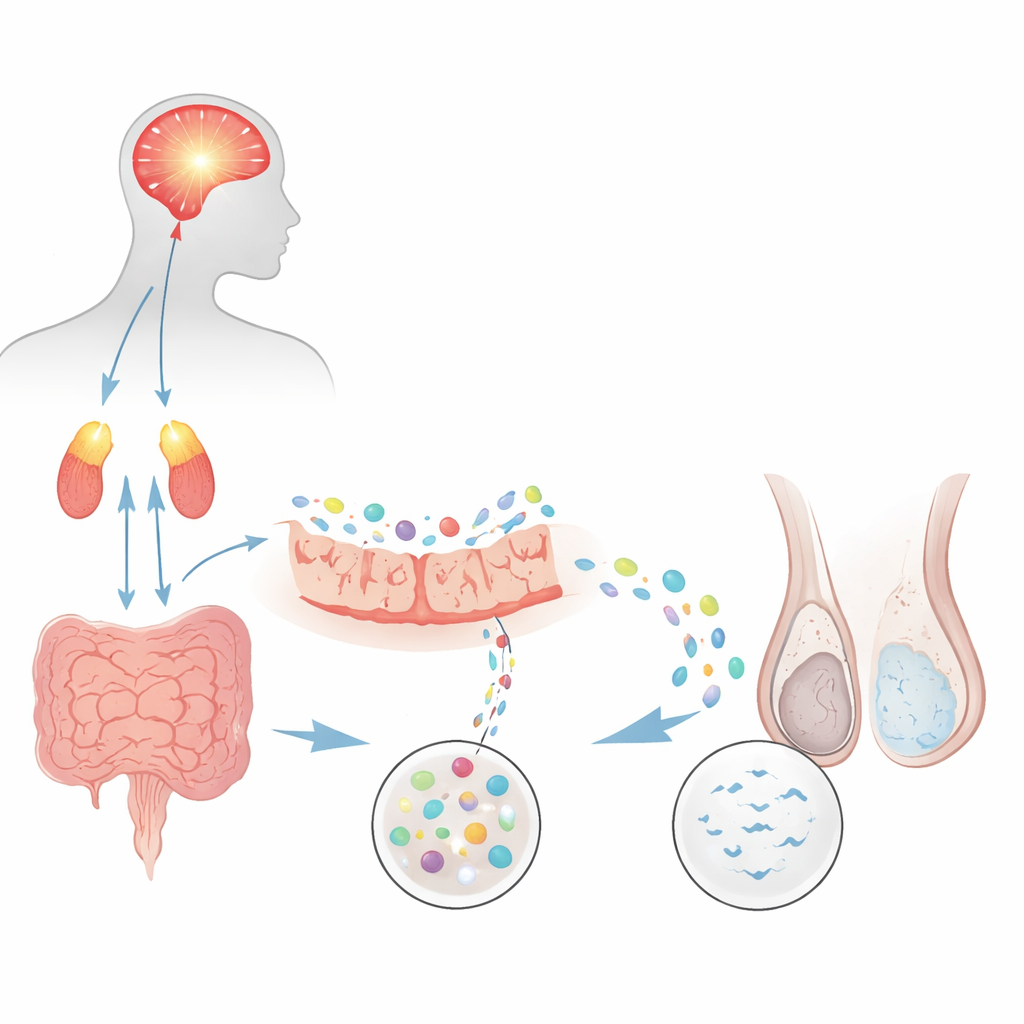
Die Forscher fragten zunächst, ob ein etabliertes Rattenmodell für chronischen psychologischen Stress eine häufige Form männlicher Unfruchtbarkeit nachbilden kann, die als Oligoasthenozoospermie bekannt ist und durch zu wenige und zu behäbige Spermien gekennzeichnet ist. Ratten, die wiederholt zum Schwimmen gezwungen wurden, entwickelten starke Anzeichen von Angst und Depression sowie erhöhte Stresshormone aus dem Gehirn‑Nebenniere‑System. Bei automatisierten Analysen ihres Spermas zeigten gestresste Tiere etwa die Hälfte der Spermienkonzentration und deutlich geringere Motilität im Vergleich zu Kontrollen. Marker der Spermienentwicklung in den Hoden sanken ebenfalls, und Paarungstests ergaben weniger Schwangerschaften und kleinere Würfe. Zusammengenommen zeigen diese Befunde, dass anhaltender Stress allein die Spermienproduktion und -leistung schädigen kann.
Der Darm als Vermittler
Weil der Darmtrakt sehr empfindlich auf Stresshormone reagiert, untersuchten die Forscher als Nächstes den Darm. Bei gestressten Ratten waren die Proteindichtungen, die normalerweise das Darmepithel abdichten, geschwächt, was auf eine „leckende“ Barriere hindeutet. Die Blockade des Glukokortikoidrezeptors — des Hauptangriffspunkts für Stresshormone — mit einem Wirkstoff stellte weitgehend sowohl die Darmintegrität als auch die Spermienqualität wieder her und verband den Schaden mit Hormon‑Signalwegen. Um zu prüfen, ob die Darmmikroben selbst Teil des Problems sind, transplantierten die Wissenschaftler Fäkalbakterien von gestressten bzw. Kontrollspendern in neue Ratten, deren eigene Mikrobiota durch Antibiotika ausgeschaltet worden war. Tiere, die Mikroben von gestressten Spendern erhielten, entwickelten dieselben schlechten Spermienzahlen, niedrige Motilität und verringerte Fruchtbarkeit, obwohl sie nie gestresst worden waren — ein Hinweis darauf, dass gestörte Darmgemeinschaften reproduktive Probleme über Distanz verursachen können.
Ein nützliches Bakterium und fehlende Vitamine
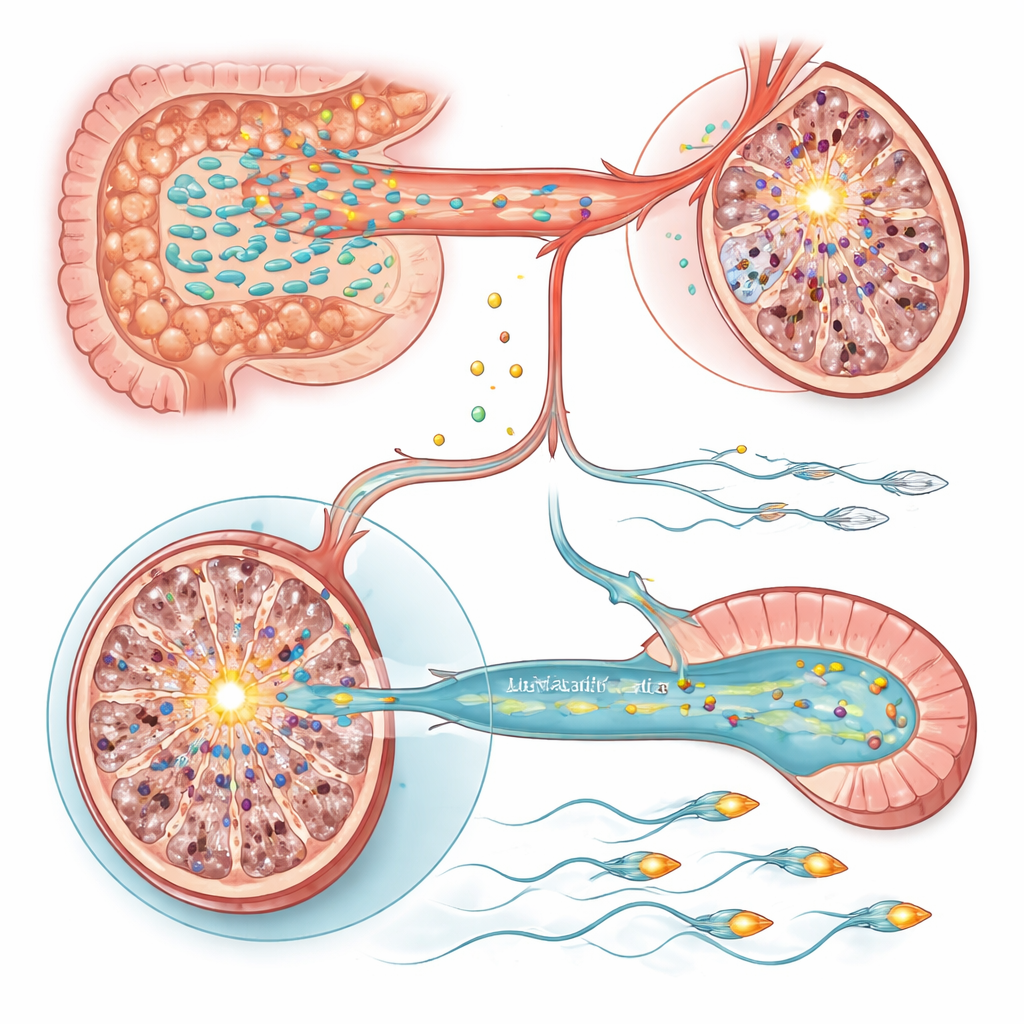
Mikrobielle DNA‑Analysen zeigten, dass chronischer Stress die Gesamtdiversität im Dünndarm reduzierte und insbesondere Lactobacillus dezimierte, eine Bakteriengruppe, die oft mit Darm‑ und Reproduktionsgesundheit in Verbindung gebracht wird. Die Häufigkeit dieser Mikroben korrelierte stark mit Spermienzahl und Motilität. Bekamen gestresste Ratten während der Stressperiode oral Lactobacillus, verbesserten sich Spermaqualität und Hodensignale, und die Fruchtbarkeit näherte sich wieder dem Normalwert an. Gleichzeitig zeigten chemische Analysen von Darminhalten, Blut und Hoden, dass Stress Gallensäuren und fettlösliche Vitamine, insbesondere die Vitamine A und E, störte — Nährstoffe, die wichtig für die Keimzell‑Entwicklung und den Schutz vor oxidativem Schaden sind. Die Spiegel mehrerer Gallensäuren und dieser Vitamine sanken im Kreislauf und im Hoden‑Gewebe, und diese Rückgänge standen in engem Zusammenhang sowohl mit dem Verlust von Lactobacillus als auch mit der Verschlechterung der Spermienparameter.
Zwei molekulare Schalter in Hoden und Spermien
Um zu verstehen, wie diese metabolischen Veränderungen Zellen beeinflussen, untersuchte das Team die Genaktivität in Hoden und Nebenhoden, wo Spermien reifen. Im Hodengewebe gestresster Ratten stach ein Gen hervor: Sting1, ein zentraler Schalter in angeborenen Immun‑ und Zellsterbewegen, war stark aktiviert. Das künstliche Hochfahren von Sting1 bei ansonsten gesunden Tieren reichte aus, um die Spermienproduktion zu reduzieren, während das Abschalten von Sting1 in gestressten Ratten die Spermienzahlen teilweise rettete. Sowohl die Behandlung mit Lactobacillus als auch die Supplementierung mit den Vitaminen A und E dämpften Sting1 wieder, wodurch die Verbindung zwischen mikrobengetriebener Vitaminbalance und diesem Entzündungsschalter sichtbar wurde. Im Gegensatz dazu ließ sich die verringerte Spermienmotilität auf den Nebenhoden zurückführen, wo ein Gen namens Slc9c2, das den spermien‑spezifischen Ionenaustauscher NHE11 kodiert und die intrazelluläre pH‑Regulation und Schwanzfunktion unterstützt, durch Stress unterdrückt wurde. Ein niedrigerer NHE11‑Spiegel war mit schwächerer Spermienbewegung und einer beeinträchtigten Fähigkeit verbunden, die Aktivierungsschritte für die Befruchtung durchzuführen. Die Wiederherstellung der Slc9c2‑Expression oder die Gabe von Lactobacillus bzw. Vitaminen A/E verbesserte die Motilität, und das experimentelle Herunterregulieren von Slc9c2 hob diese Verbesserungen wieder auf.
Was das für gestresste Männer bedeutet
Insgesamt skizziert die Studie eine Ereigniskette, die mit chronischer psychischer Belastung beginnt und mit weniger, weniger aktiven Spermien endet. Stresshormone schwächen die Darmbarriere und verringern nützliche Lactobacillus‑Populationen, die ihrerseits Gallensäuren sowie die Vitamine A und E stören. Diese Nährstoffverschiebungen schalten über Sting1 einen Zellsterbeweg in den Hoden ein und drosseln die Aktivität von NHE11 im Nebenhoden, was die Spermienschwanzfunktion verlangsamt. Obwohl die Arbeiten an Ratten durchgeführt wurden und weitere Studien am Menschen erforderlich sind, betrachtet die Studie bestimmte Fälle männlicher Unfruchtbarkeit neu — als einen Ganzkörperzustand, der Gehirn, Darmmikroben, Nährstoffe und Fortpflanzungsorgane umfasst. Sie wirft auch die Möglichkeit auf, dass gut konzipierte Probiotika‑ und Vitamin‑Strategien neben Stressmanagement eines Tages helfen könnten, die Fruchtbarkeit von Männern mit chronischem psychologischen Stress zu schützen oder wiederherzustellen.
Zitation: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
Schlüsselwörter: männliche Unfruchtbarkeit, chronischer Stress, Darmmikrobiota, Vitamine A und E, Spermienmotilität