Clear Sky Science · pt
Estresse crônico causa oligoastenozoospermia via eixo microbiota intestinal‑vitamina‑Sting1/Slc9c2
Quando o Estresse Alcança o Sistema Reprodutor
A maioria das pessoas sabe que o estresse crônico pode drenar a energia, atrapalhar o sono e afetar o humor, mas poucos percebem que ele também pode minar silenciosamente a fertilidade masculina. Este estudo em ratos revela como o estresse psicológico prolongado pode reduzir tanto a contagem quanto a motilidade dos espermatozoides, não apenas por hormônios, mas perturbando os microrganismos intestinais e as vitaminas que eles ajudam a fornecer. O trabalho aponta uma linha de comunicação oculta entre cérebro, intestino e testículos — e sugere que apoiar bactérias benéficas e nutrientes-chave pode um dia ajudar a proteger a fertilidade em homens sob estresse.
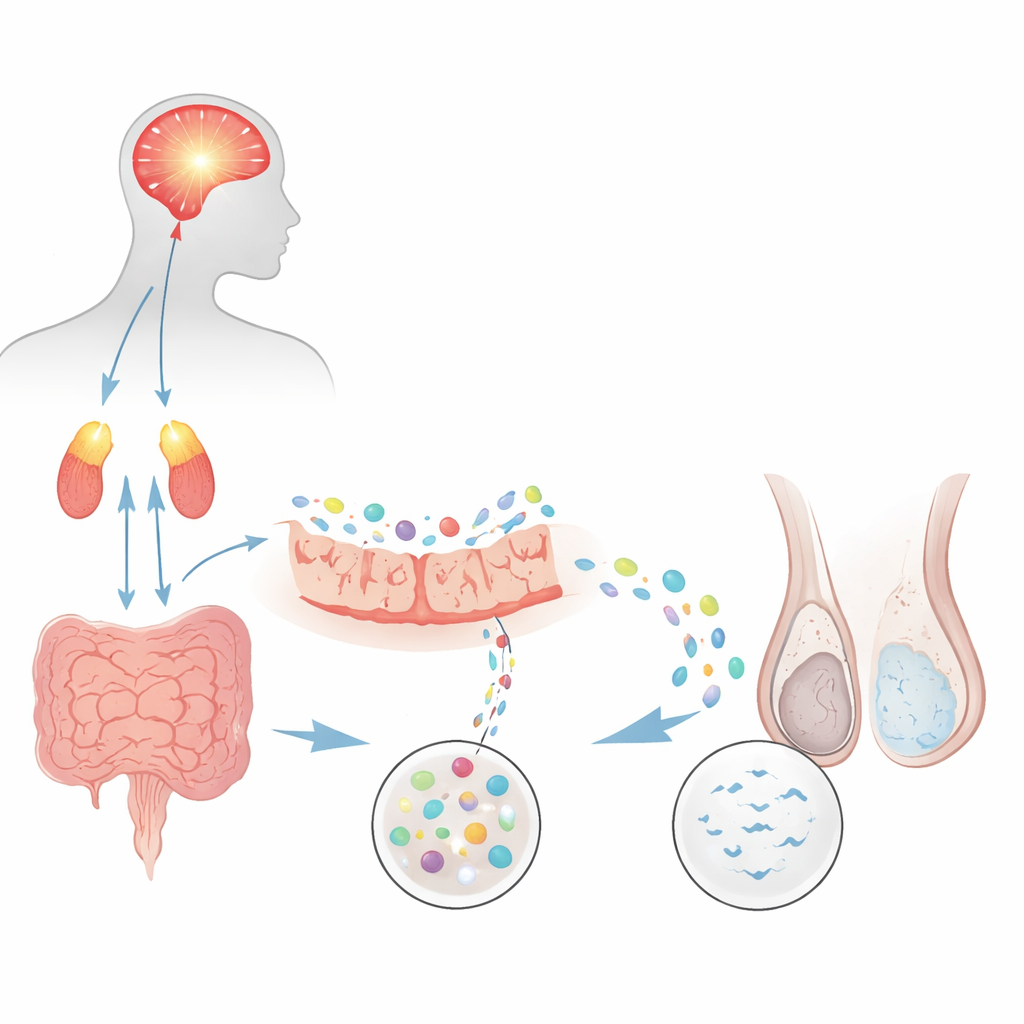
Do Esforço Mental a Menos Espermatozoides
Os pesquisadores primeiro perguntaram se um modelo bem estabelecido de estresse psicológico crônico em ratos poderia imitar uma forma comum de infertilidade masculina chamada oligoastenozoospermia, em que os espermatozoides são tanto poucos quanto lentos. Ratos repetidamente expostos a nado forçado desenvolveram sinais fortes de ansiedade e depressão, junto com hormônios de estresse elevados do eixo cérebro‑adrenal. Ao examinar o sêmen com ferramentas automatizadas, os animais estressados apresentaram aproximadamente metade da concentração de espermatozoides e motilidade muito menor em comparação com os controles. Marcadores do desenvolvimento espermático nos testículos também caíram, e testes de acasalamento mostraram menos gestações e ninhadas menores. Em conjunto, esses achados mostraram que o estresse persistente por si só pode prejudicar a produção e o desempenho dos espermatozoides.
O Intestino como Intermediário
Como o trato intestinal é altamente sensível a hormônios do estresse, a equipe investigou o intestino. Em ratos estressados, as junções proteicas que normalmente apertam o revestimento intestinal estavam enfraquecidas, sugerindo uma barreira “vazante”. Bloquear o receptor de glicocorticoide — o principal ponto de acoplamento para hormônios do estresse — com um fármaco restaurou em grande parte tanto a integridade intestinal quanto a qualidade dos espermatozoides, vinculando o dano à sinalização hormonal. Para testar se os micróbios intestinais eram parte do problema, os cientistas transplantaram bactérias fecais de doadores estressados ou controles em novos ratos cuja própria microbiota havia sido eliminada por antibióticos. Animais que receberam micróbios de doadores estressados desenvolveram as mesmas contagens baixas de espermatozoides, motilidade reduzida e fertilidade prejudicada, mesmo sem terem sido expostos ao estresse, revelando que comunidades intestinais perturbadas podem provocar problemas reprodutivos a distância.
Uma Bactéria Útil e Vitaminas em Falta
O perfil do DNA microbiano mostrou que o estresse crônico reduziu a diversidade geral no intestino delgado e, em particular, esgotou Lactobacillus, um grupo de bactérias frequentemente associado à saúde intestinal e reprodutiva. A abundância desses microrganismos acompanhou fortemente as contagens e a motilidade dos espermatozoides. Quando ratos estressados receberam Lactobacillus por via oral durante o período de estresse, a qualidade do sêmen e os marcadores testiculares melhoraram, e os desfechos de fertilidade voltaram em direção ao normal. Ao mesmo tempo, análises químicas do conteúdo intestinal, sangue e testículos revelaram que o estresse perturbou ácidos biliares e vitaminas lipossolúveis, especialmente as vitaminas A e E, importantes para o desenvolvimento das células germinativas e proteção contra dano oxidativo. Os níveis de vários ácidos biliares e dessas vitaminas caíram na circulação e no tecido testicular, e essas quedas foram fortemente associadas tanto à perda de Lactobacillus quanto ao piora dos parâmetros espermáticos.
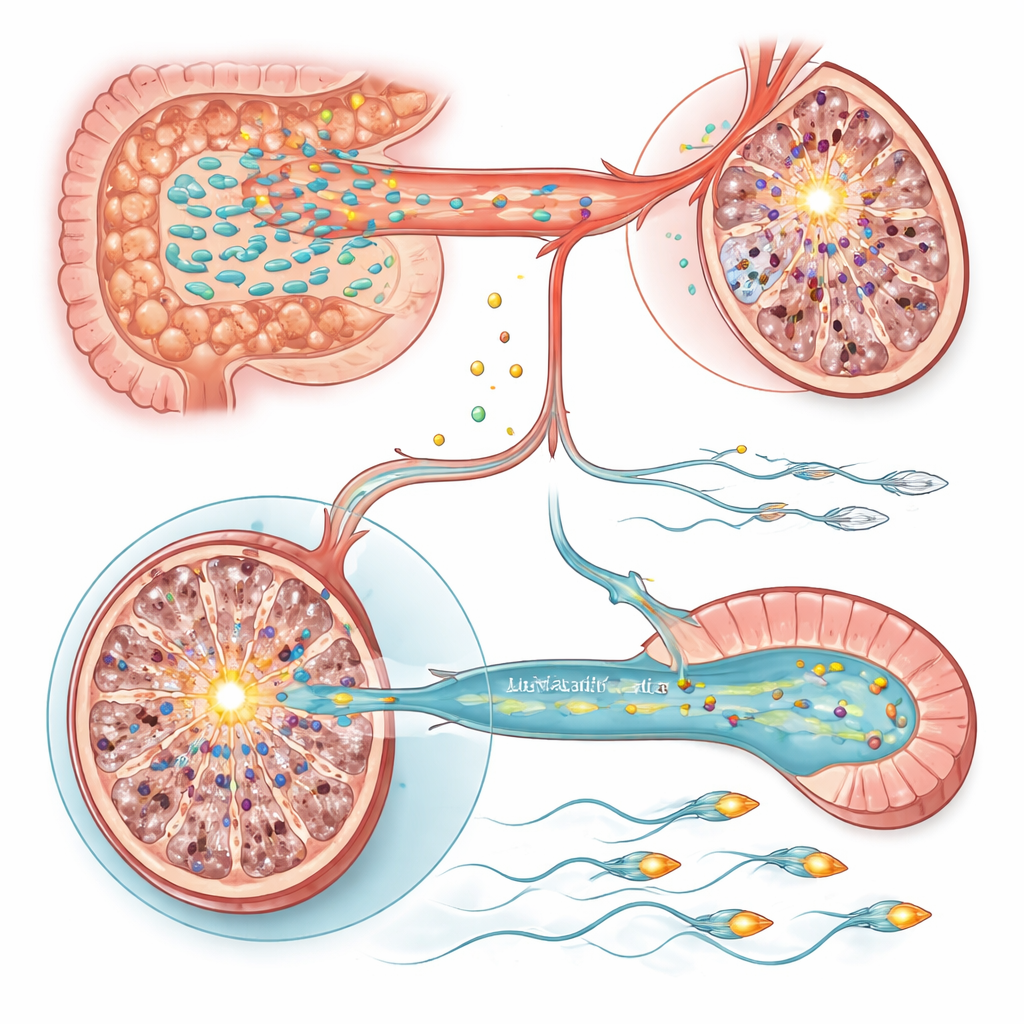
Dois Interruptores Moleculares em Testículos e Espermatozoides
Para entender como essas mudanças metabólicas afetam as células, a equipe examinou a atividade gênica nos testículos e no epidídimo, onde os espermatozoides amadurecem. Nos testículos de ratos estressados, um gene se destacou: Sting1, um interruptor mestre em vias imunes inatas e de morte celular, estava fortemente ativado. Estimular artificialmente Sting1 em animais saudáveis foi suficiente para reduzir a produção de espermatozoides, enquanto silenciá‑lo em ratos estressados resgatou parcialmente o número de espermatozoides. Tanto o tratamento com Lactobacillus quanto a suplementação com vitaminas A e E reduziram a atividade de Sting1, ligando o equilíbrio de vitaminas dirigido por micróbios a esse interruptor inflamatório. Em contraste, a redução da motilidade espermática foi atribuída ao epidídimo, onde um gene chamado Slc9c2, que codifica o trocador iônico específico de espermatozoides NHE11 — que ajuda a controlar o pH interno e a função da cauda — foi suprimido pelo estresse. Menores níveis de NHE11 associaram‑se a movimentos mais fracos dos espermatozoides e à capacidade reduzida de passar pelos passos de ativação necessários para a fertilização. Restaurar a expressão de Slc9c2, ou suplementar com Lactobacillus ou vitaminas A/E, melhorou a motilidade, e a interferência experimental em Slc9c2 aboliu esses ganhos.
O Que Isso Significa para Homens Sob Pressão
Em conjunto, o estudo descreve uma cadeia de eventos que começa com tensão psicológica crônica e termina com espermatozoides menos numerosos e menos ativos. Hormônios do estresse enfraquecem a barreira intestinal e reduzem populações benéficas de Lactobacillus, o que, por sua vez, perturba ácidos biliares e vitaminas A e E. Essas alterações nutricionais ativam uma via de morte celular nos testículos via Sting1, reduzindo a produção de espermatozoides, e diminuem a atividade de NHE11 no epidídimo, retardando as caudas espermáticas. Embora o trabalho tenha sido realizado em ratos e mais pesquisas em humanos sejam necessárias, ele reconfigura certos casos de infertilidade masculina como uma condição de corpo inteiro envolvendo cérebro, microrganismos intestinais, nutrientes e órgãos reprodutivos. Também levanta a possibilidade de que estratégias cuidadosas com probióticos e vitaminas, juntamente com manejo do estresse, possam um dia ajudar a proteger ou restaurar a fertilidade em homens vivendo com estresse psicológico crônico.
Citação: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
Palavras-chave: infertilidade masculina, estresse crônico, microbiota intestinal, vitaminas A e E, motilidade espermática