Clear Sky Science · fr
Le stress chronique provoque une oligo-asthénozoospermie via l’axe microbiote intestinal‑vitamines‑Sting1/Slc9c2
Quand le stress atteint le système reproducteur
La plupart des gens savent que le stress chronique peut épuiser l’énergie, perturber le sommeil et altérer l’humeur, mais peu réalisent qu’il peut aussi saper silencieusement la fertilité masculine. Cette étude chez le rat révèle comment un stress psychologique prolongé peut réduire le nombre et la mobilité des spermatozoïdes, non seulement via les hormones, mais aussi en perturbant les microbes intestinaux et les vitamines qu’ils contribuent à fournir. Ce travail met en lumière une ligne de communication cachée entre le cerveau, l’intestin et les testicules — et suggère que soutenir des bactéries bénéfiques et des nutriments clés pourrait un jour aider à protéger la fertilité des hommes stressés.
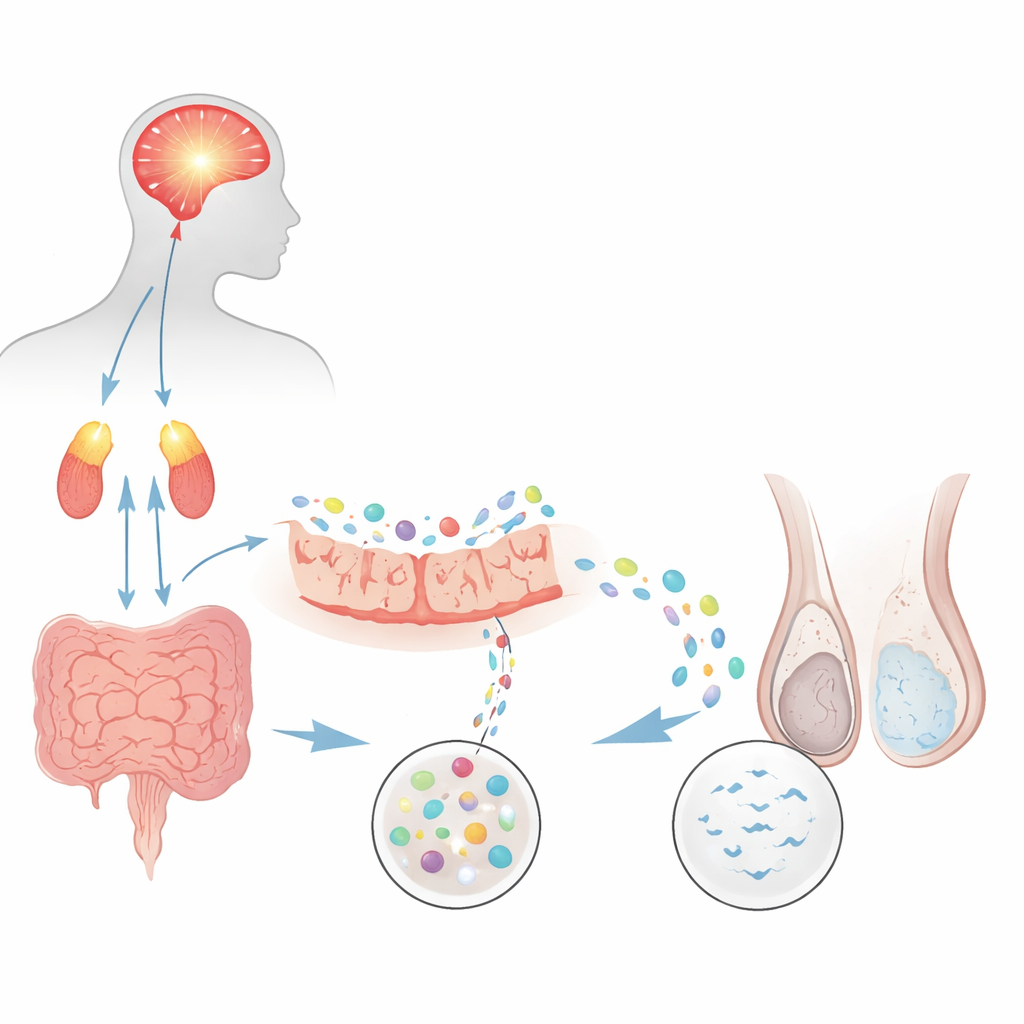
Du stress mental à moins de spermatozoïdes
Les chercheurs ont d’abord cherché à savoir si un modèle connu de stress psychologique chronique chez le rat pouvait reproduire une forme courante d’infertilité masculine appelée oligo-asthénozoospermie, dans laquelle les spermatozoïdes sont à la fois trop peu nombreux et trop lents. Des rats exposés de façon répétée à la nage forcée ont développé des signes marqués d’anxiété et de dépression, accompagnés d’une élévation des hormones de stress issues de l’axe cerveau‑surrénales. L’examen du sperme avec des outils automatisés a montré que les animaux stressés présentaient environ la moitié de la concentration en spermatozoïdes et une motilité fortement réduite par rapport aux contrôles. Les marqueurs du développement des spermatozoïdes au sein des testicules ont également diminué, et les tests de reproduction ont montré moins de grossesses et des portées plus petites. Ensemble, ces résultats montrent que le stress persistant seul peut endommager la production et la performance des spermatozoïdes.
L’intestin comme intermédiaire
Comme le tractus intestinal est très sensible aux hormones du stress, l’équipe s’est intéressée ensuite au microbiote. Chez les rats stressés, les protéines assurant l’étanchéité de la muqueuse intestinale étaient affaiblies, suggérant une barrière « perméable ». Le blocage du récepteur aux glucocorticoïdes — le principal point d’action des hormones de stress — par un médicament a largement restauré à la fois l’intégrité intestinale et la qualité du sperme, reliant les dommages à la signalisation hormonale. Pour tester si les microbes intestinaux faisaient eux‑mêmes partie du problème, les scientifiques ont transplanté des bactéries fécales de donneurs stressés ou témoins dans de nouveaux rats dont le microbiote avait été éliminé par antibiotiques. Les animaux recevant des microbes de donneurs stressés ont développé les mêmes faibles nombres de spermatozoïdes, faible motilité et fertilité réduite, bien qu’ils n’aient jamais été stressés, révélant que des communautés intestinales perturbées peuvent provoquer à distance des problèmes reproductifs.
Une bactérie bénéfique et des vitamines manquantes
Le profilage de l’ADN microbien a montré que le stress chronique réduisait la diversité globale dans l’intestin grêle et, en particulier, appauvrissait les Lactobacillus, un groupe de bactéries souvent associé à la santé intestinale et reproductive. L’abondance de ces microbes corrélait fortement avec la concentration et la motilité des spermatozoïdes. Lorsque des rats stressés ont reçu par voie orale des Lactobacillus tout au long de la période de stress, la qualité du sperme et les marqueurs testiculaires se sont améliorés, et les résultats de fertilité se sont rapprochés de la normale. Parallèlement, des analyses chimiques des contenus intestinaux, du sang et des testicules ont révélé que le stress perturbait les acides biliaires et les vitamines liposolubles, en particulier les vitamines A et E, qui sont importantes pour le développement des cellules germinales et la protection contre les dommages oxydatifs. Les niveaux de plusieurs acides biliaires et de ces vitamines ont chuté dans la circulation et dans le tissu testiculaire, et ces baisses étaient étroitement liées à la perte de Lactobacillus et à la détérioration des paramètres spermatiques.
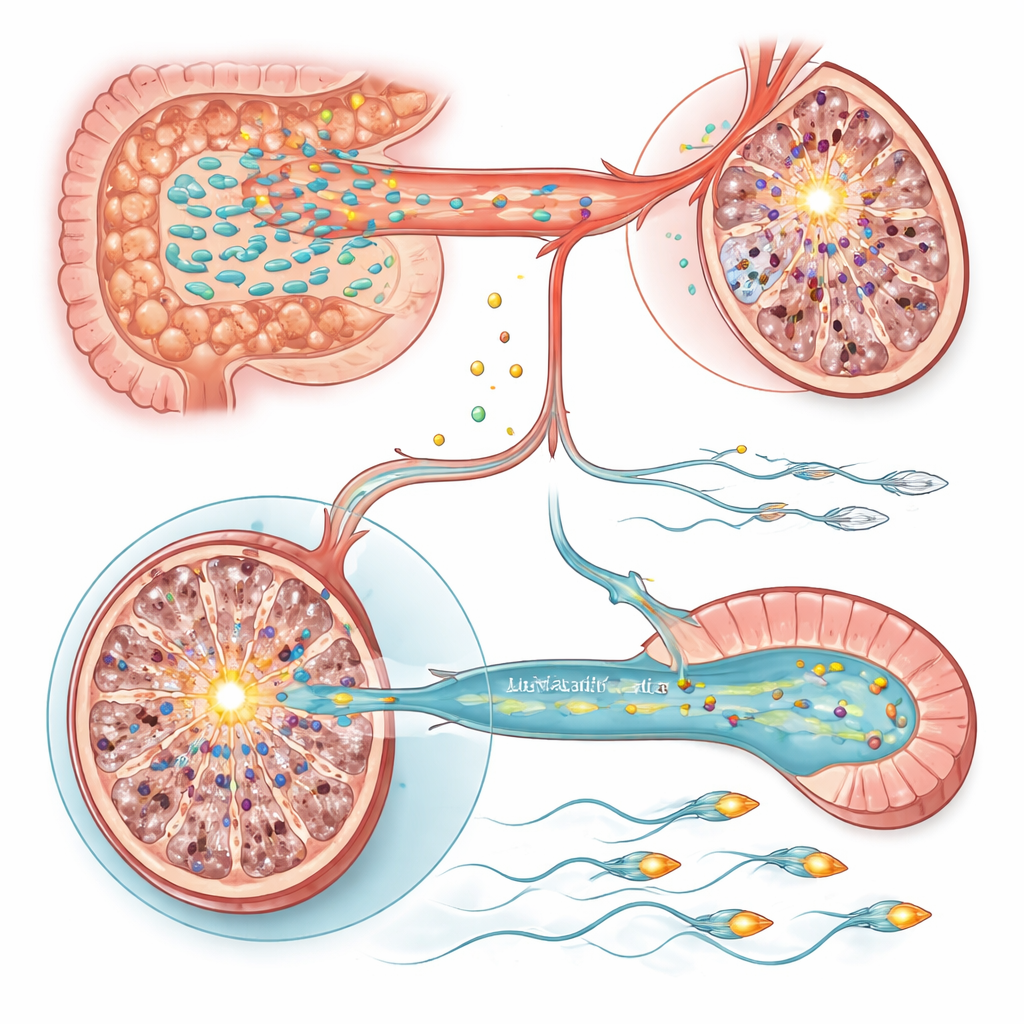
Deux interrupteurs moléculaires dans le testicule et le spermatozoïde
Pour comprendre comment ces changements métaboliques modifient les cellules, l’équipe a examiné l’activité génique dans les testicules et l’épididyme, où les spermatozoïdes mûrissent. Dans les testicules des rats stressés, un gène a émergé : Sting1, un régulateur majeur des voies immunitaires innées et de la mort cellulaire, était fortement activé. L’activation artificielle de Sting1 chez des animaux autrement sains suffisait à réduire la production de spermatozoïdes, tandis que son inhibition chez des rats stressés a partiellement restauré le nombre de spermatozoïdes. Le traitement par Lactobacillus et la supplémentation en vitamines A et E ont tous deux ramené Sting1 vers des valeurs plus basses, reliant l’équilibre microbien‑vitaminique à cet interrupteur inflammatoire. En revanche, la réduction de la motilité des spermatozoïdes était liée à l’épididyme, où un gène appelé Slc9c2, codant pour l’échangeur ionique spécifique aux spermatozoïdes NHE11 qui aide à contrôler le pH interne et la fonction de la queue, était supprimé par le stress. Une baisse de NHE11 s’associait à un mouvement moins vigoureux des spermatozoïdes et à une capacité altérée d’effectuer les étapes d’activation nécessaires à la fécondation. Restaurer l’expression de Slc9c2, ou supplémenter en Lactobacillus ou en vitamines A/E, améliorait la motilité, et l’inhibition expérimentale de Slc9c2 supprimait ces bénéfices.
Ce que cela signifie pour les hommes sous pression
Dans l’ensemble, l’étude décrit une chaîne d’événements qui commence par une contrainte psychologique chronique et aboutit à des spermatozoïdes moins nombreux et moins actifs. Les hormones de stress affaiblissent la barrière intestinale et réduisent les populations bénéfiques de Lactobacillus, ce qui perturbe à son tour les acides biliaires et les vitamines A et E. Ces modifications nutritives activent une voie de mort cellulaire dans les testicules via Sting1, réduisant la production de spermatozoïdes, et diminuent l’activité de NHE11 dans l’épididyme, ralentissant les flagelles. Bien que le travail ait été réalisé chez le rat et que des recherches supplémentaires chez l’homme soient nécessaires, il reframe certains cas d’infertilité masculine comme une condition systémique impliquant le cerveau, le microbiote intestinal, les nutriments et les organes reproducteurs. Il évoque aussi la possibilité que des stratégies probiotiques et vitaminées bien conçues, associées à la gestion du stress, puissent un jour aider à protéger ou restaurer la fertilité chez les hommes vivant avec un stress psychologique chronique.
Citation: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
Mots-clés: infertilité masculine, stress chronique, microbiote intestinal, vitamines A et E, motilité des spermatozoïdes