Clear Sky Science · sv
Kronisk stress driver oligoasthenozoospermi via tarmmikrobiota‑vitamin‑Sting1/Slc9c2‑axeln
När stress når fortplantningssystemet
De flesta vet att kronisk stress kan tömma energin, störa sömnen och påverka humöret, men få inser att den också i det tysta kan undergräva manlig fertilitet. Denna studie på råttor visar hur långvarig psykologisk stress kan minska både spermieantal och rörelseförmåga — inte bara via hormoner utan genom att rubba tarmens mikrober och de vitaminer de bidrar med. Arbetet pekar på en dold kommunikationslinje mellan hjärna, tarm och testiklar — och antyder att stöd för gynnsamma bakterier och nyckelnäringsämnen en dag kan hjälpa till att skydda fertiliteten hos stressade män.
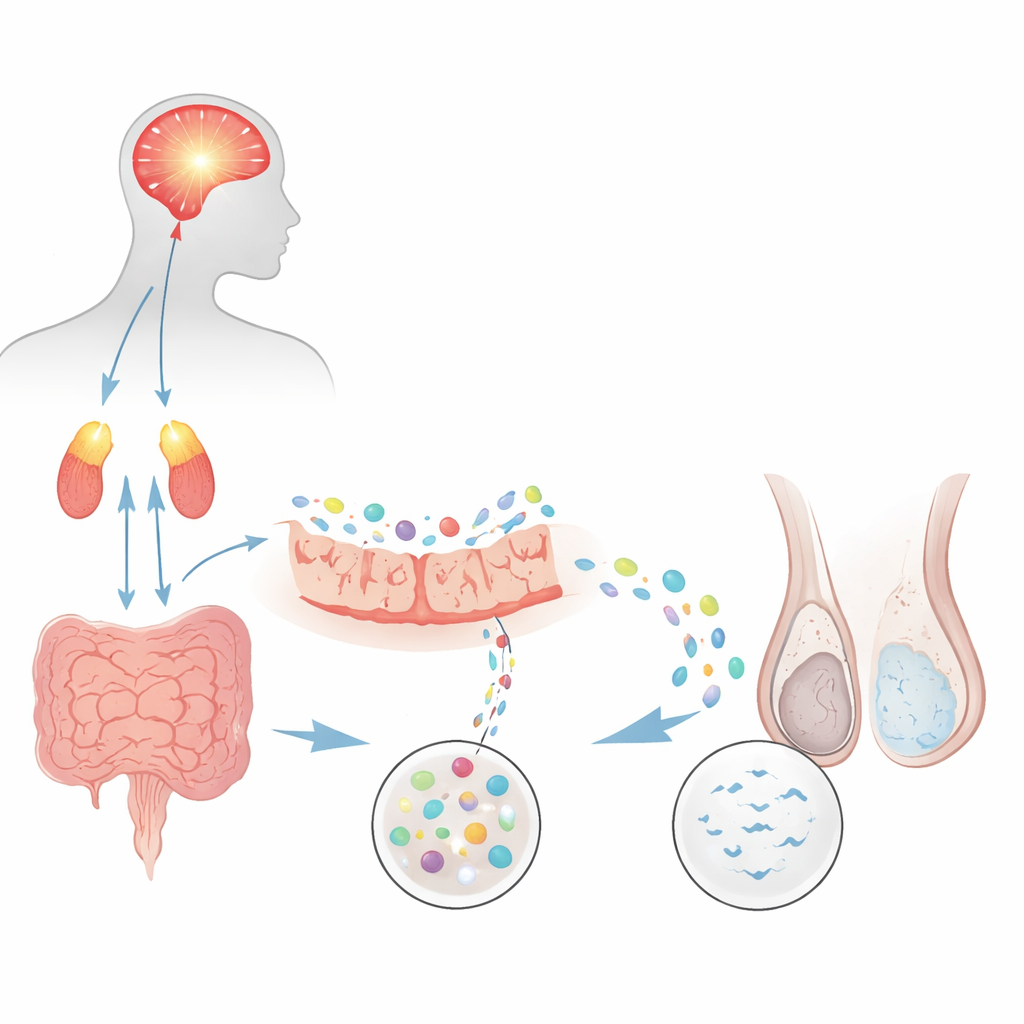
Från psykisk påfrestning till färre spermier
Forskarna frågade först om en väletablerad råttmodell för kronisk psykologisk stress kunde återskapa en vanlig form av manlig infertilitet som kallas oligoasthenozoospermi, där spermierna både är för få och för slöa. Råttor som upprepade gånger utsattes för tvångssimning utvecklade starka tecken på ångest och depression, tillsammans med förhöjda stresshormoner från hjärna–binjure‑systemet. När deras sperma undersöktes med automatiserade metoder hade de stressade djuren ungefär halva spermiekoncentrationen och markant lägre rörelseförmåga jämfört med kontroller. Markörer för spermieutveckling i testiklarna sjönk också, och parningstester visade färre dräktigheter och mindre kullstorlekar. Sammantaget visade dessa fynd att bestående stress ensam kan skada spermieproduktion och funktion.
Tarmen som mellanhantverkare
Eftersom tarmkanalen är mycket känslig för stresshormoner undersökte teamet nästa tarmen. Hos stressade råttor var de proteintätningsband som normalt håller tarmens epitel tätt försvagade, vilket tyder på en "läckande" barriär. Att blockera glukokortikoidreceptorn — huvudbindningsstället för stresshormoner — med ett läkemedel återställde i stor utsträckning både tarmens integritet och spermiekvaliteten, vilket kopplade skadan till hormonell signalering. För att testa om tarmmikroberna själva var en del av problemet transplanterade forskarna fekala bakterier från stressade respektive kontrollgivare till nya råttor vars egen mikrobiota hade slagits ut med antibiotika. Djur som fick mikrober från stressade givare utvecklade samma låga spermieantal, reducerade rörlighet och nedsatta fertilitet, trots att de aldrig varit stressade, vilket visar att rubbade tarmgemenskaper kan driva reproduktionsproblem på distans.
En hjälpsam bakterie och förlorade vitaminer
Profilering av mikrobiellt DNA visade att kronisk stress minskade den övergripande mångfalden i tunntarmen och särskilt utarmade Lactobacillus, en grupp bakterier som ofta förknippas med tarm‑ och reproduktionshälsa. Förekomsten av dessa mikrober följde starkt spermieantal och rörlighet. När stressade råttor gavs oral Lactobacillus under hela stressperioden förbättrades deras spermakvalitet och testismarkörer, och fertilitetsutfallen rörde sig tillbaka mot normalnivåer. Samtidigt visade kemiska analyser av tarminnehåll, blod och testiklar att stress störde gallsyremetabolismen och fettlösliga vitaminer, särskilt vitamin A och E, som är viktiga för könscellsutveckling och skydd mot oxidativ skada. Nivåerna av flera gallsyrror och dessa vitaminer föll i cirkulationen och i testikulär vävnad, och dessa minskningar var nära kopplade både till förlusten av Lactobacillus och till försämrade spermieparametrar.
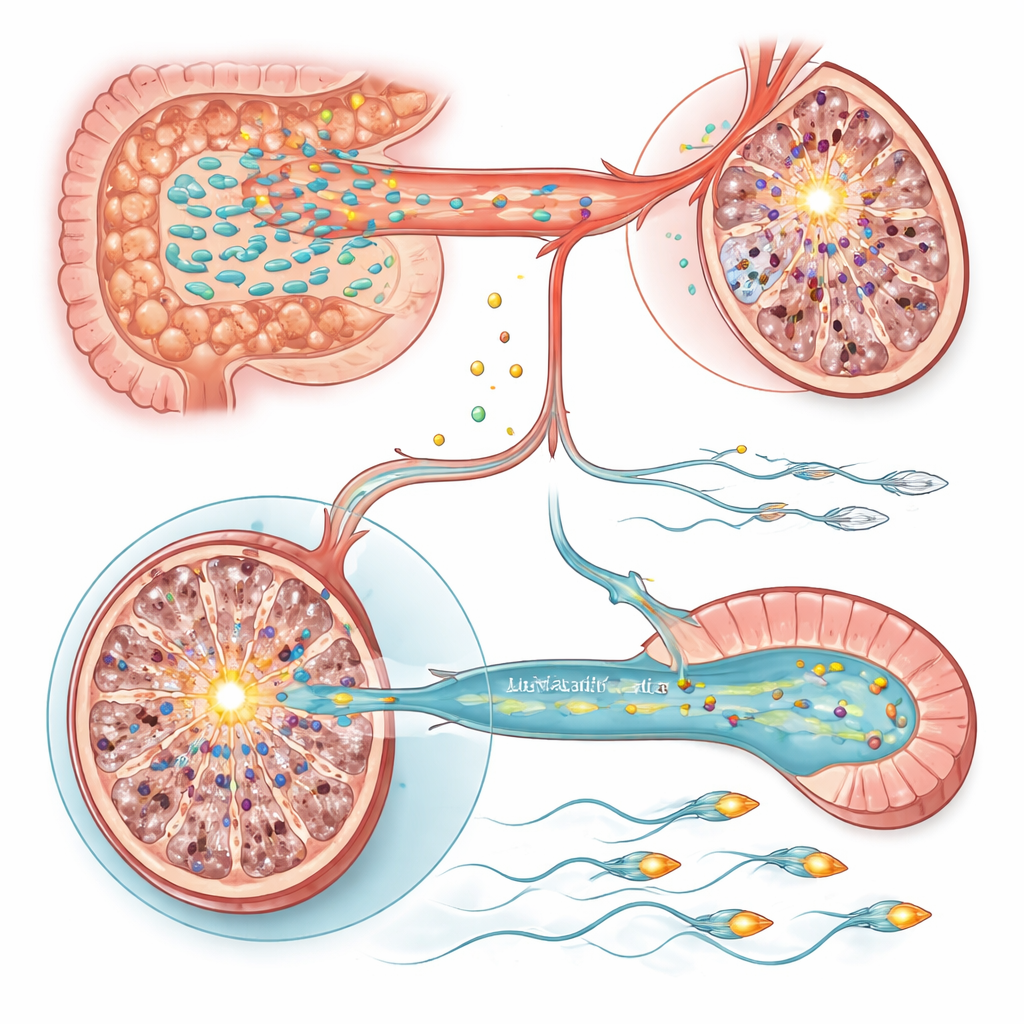
Två molekylära strömbrytare i testis och spermier
För att förstå hur dessa metabola förändringar påverkar celler undersökte teamet genaktivitet i testiklarna och bitestiklarna, där spermier mognar. I testiklarna hos stressade råttor stack en gen ut: Sting1, en huvudregulator i medfödda immunsvar och cell‑dödsvägar, var starkt aktiverad. Att konstgjort höja Sting1 i annars friska djur räckte för att minska spermieproduktionen, medan att tysta genen hos stressade råttor delvis återställde spermieantalet. Både behandling med Lactobacillus och tillskott av vitamin A och E sänkte Sting1‑aktiviteten, vilket kopplar mikrobiellt driven vitaminbalans till denna inflammatoriska strömbrytare. Däremot härleddes reducerad spermierörlighet till bitestiklarna, där en gen kallad Slc9c2, som kodar för spermiespecifika jonutbytaren NHE11 som hjälper styra intern pH och svansfunktion, undertrycktes av stress. Lägre NHE11 var associerat med svagare spermierörelser och nedsatt förmåga att genomgå aktiveringssteg som krävs för befruktning. Återställande av Slc9c2‑uttryck, eller tillskott av Lactobacillus eller vitaminerna A/E, förbättrade rörligheten, och experimentell nedtystning av Slc9c2 utslockade dessa förbättringar.
Vad detta betyder för män under press
Sammantaget beskriver studien en händelsekedja som börjar med kronisk psykologisk belastning och slutar med färre, mindre aktiva spermier. Stresshormoner försvagar tarmbarriären och minskar gynnsamma Lactobacillus‑populationer, vilket i sin tur stör gallsyra‑ och vitaminbalansen för vitamin A och E. Dessa näringsskiften aktiverar en celldödsväg i testiklarna via Sting1, vilket minskar spermieproduktionen, och dämpar aktiviteten hos NHE11 i bitestikeln, vilket saktar ner spermiesvansarna. Även om arbetet är gjort på råttor och mer forskning på människor behövs, omformulerar det vissa fall av manlig infertilitet som ett kroppsomfattande tillstånd som involverar hjärna, tarmmikrober, näringsämnen och fortplantningsorgan. Det väcker också möjligheten att noggrant utformade probiotika‑ och vitaminstrategier, tillsammans med stresshantering, en dag skulle kunna hjälpa till att skydda eller återställa fertilitet hos män som lever med kronisk psykologisk stress.
Citering: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
Nyckelord: manlig infertilitet, kronisk stress, tarmmikrobiota, vitamin A och E, spermierörlighet