Clear Sky Science · it
Lo stress cronico provoca oligoastenozoospermia tramite l’asse microbiota intestinale‑vitamine‑Sting1/Slc9c2
Quando lo stress raggiunge il sistema riproduttivo
La maggior parte delle persone sa che lo stress cronico può prosciugare le energie, disturbare il sonno e appannare l’umore, ma pochi realizzano che può anche compromettere silenziosamente la fertilità maschile. Questo studio sui ratti mostra come uno stress psicologico prolungato possa ridurre il numero e la motilità degli spermatozoi non solo attraverso gli ormoni, ma alterando il microbiota intestinale e le vitamine che esso contribuisce a fornire. Il lavoro indica una linea di comunicazione nascosta tra cervello, intestino e testicoli e suggerisce che sostenere batteri benefici e nutrienti chiave potrebbe un giorno aiutare a proteggere la fertilità negli uomini stressati.
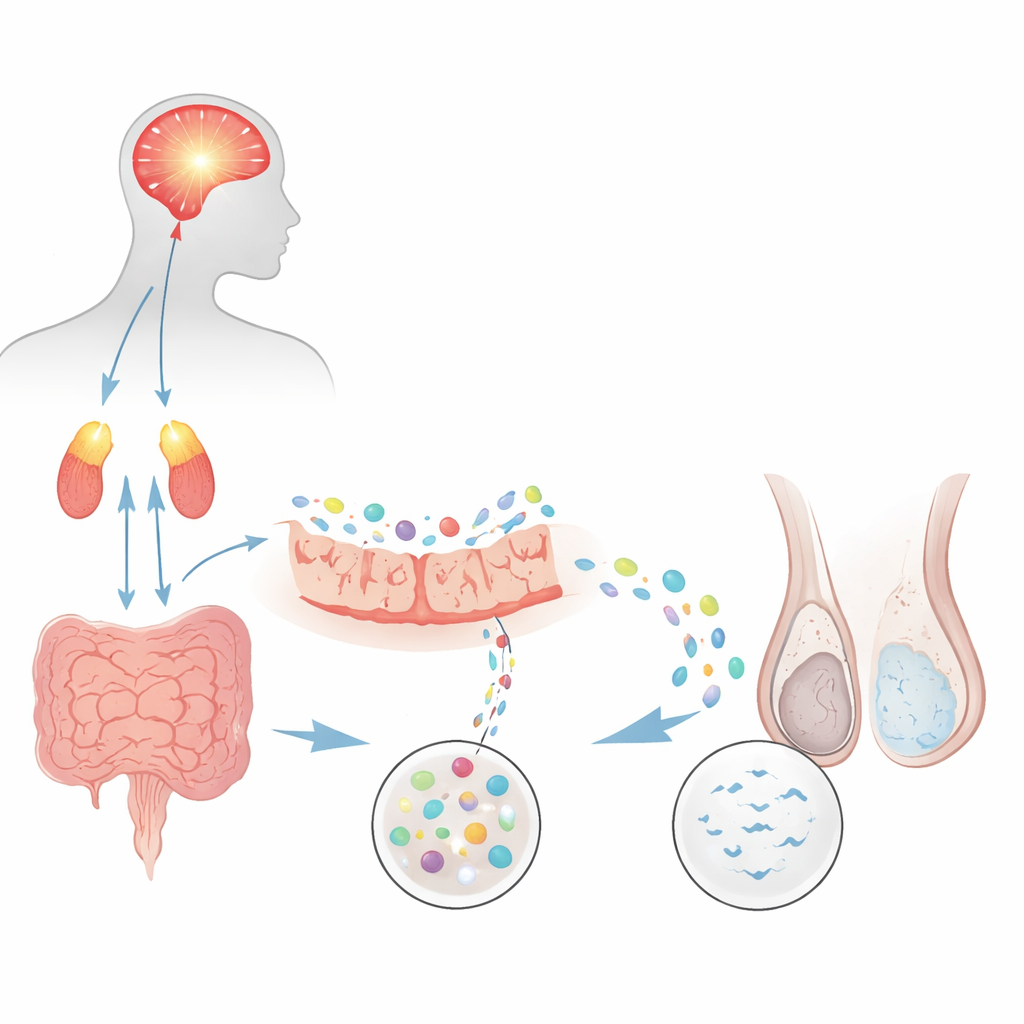
Dallo sforzo mentale a meno spermatozoi
I ricercatori si sono innanzitutto chiesti se un modello ben consolidato di stress psicologico cronico nei ratti potesse riprodurre una forma comune di infertilità maschile chiamata oligoastenozoospermia, in cui gli spermatozoi sono sia troppo pochi sia troppo lenti. I ratti sottoposti ripetutamente a nuoto forzato hanno sviluppato chiari segni di ansia e depressione, insieme a livelli aumentati di ormoni dello stress prodotti dall’asse cervello‑surrene. Analizzando il loro seme con strumenti automatizzati, gli animali stressati avevano circa la metà della concentrazione di spermatozoi e una motilità nettamente inferiore rispetto ai controlli. Anche i marcatori dello sviluppo degli spermatozoi nei testicoli sono diminuiti e i test di accoppiamento hanno mostrato meno gravidanze e cucciolate più piccole. Nel complesso, questi risultati dimostrano che lo stress persistente da solo può danneggiare produzione e prestazioni degli spermatozoi.
L’intestino come intermediario
Poiché l’intestino è molto sensibile agli ormoni dello stress, il gruppo ha quindi esaminato il tratto intestinale. Nei ratti stressati, le proteine che normalmente sigillano la parete intestinale risultavano indebolite, suggerendo una barriera “permeabile”. Il blocco del recettore dei glucocorticoidi — il principale punto di ancoraggio per gli ormoni dello stress — con un farmaco ha in gran parte ripristinato sia l’integrità intestinale sia la qualità degli spermatozoi, collegando il danno alla segnalazione ormonale. Per verificare se anche i microbi intestinali fossero parte del problema, gli scienziati hanno trapiantato batteri fecali da donatori stressati o di controllo in nuovi ratti il cui microbiota era stato cancellato dagli antibiotici. Gli animali che hanno ricevuto i microbi da donatori stressati hanno sviluppato gli stessi bassi conteggi di spermatozoi, la bassa motilità e la fertilità ridotta, pur non essendo mai stati stressati, rivelando che comunità microbiche disturbate possono causare problemi riproduttivi a distanza.
Un batterio utile e vitamine mancanti
Il profilo del DNA microbico ha mostrato che lo stress cronico ha ridotto la diversità complessiva nell’intestino tenue e, in particolare, ha impoverito i Lactobacillus, un gruppo di batteri spesso associato alla salute intestinale e riproduttiva. L’abbondanza di questi microrganismi era fortemente correlata con conteggi e motilità degli spermatozoi. Quando ai ratti stressati è stato somministrato oralmente Lactobacillus per tutta la durata dello stress, la qualità del seme e i marcatori testicolari sono migliorati e gli esiti di fertilità si sono avvicinati alla normalità. Parallelamente, le analisi chimiche del contenuto intestinale, del sangue e dei testicoli hanno rivelato che lo stress ha alterato gli acidi biliari e le vitamine liposolubili, in particolare le vitamine A ed E, importanti per lo sviluppo delle cellule germinali e la protezione dal danno ossidativo. I livelli di diversi acidi biliari e di queste vitamine sono diminuiti nella circolazione e nel tessuto testicolare, e questi cali erano strettamente collegati sia alla perdita di Lactobacillus sia al peggioramento dei parametri spermatici.
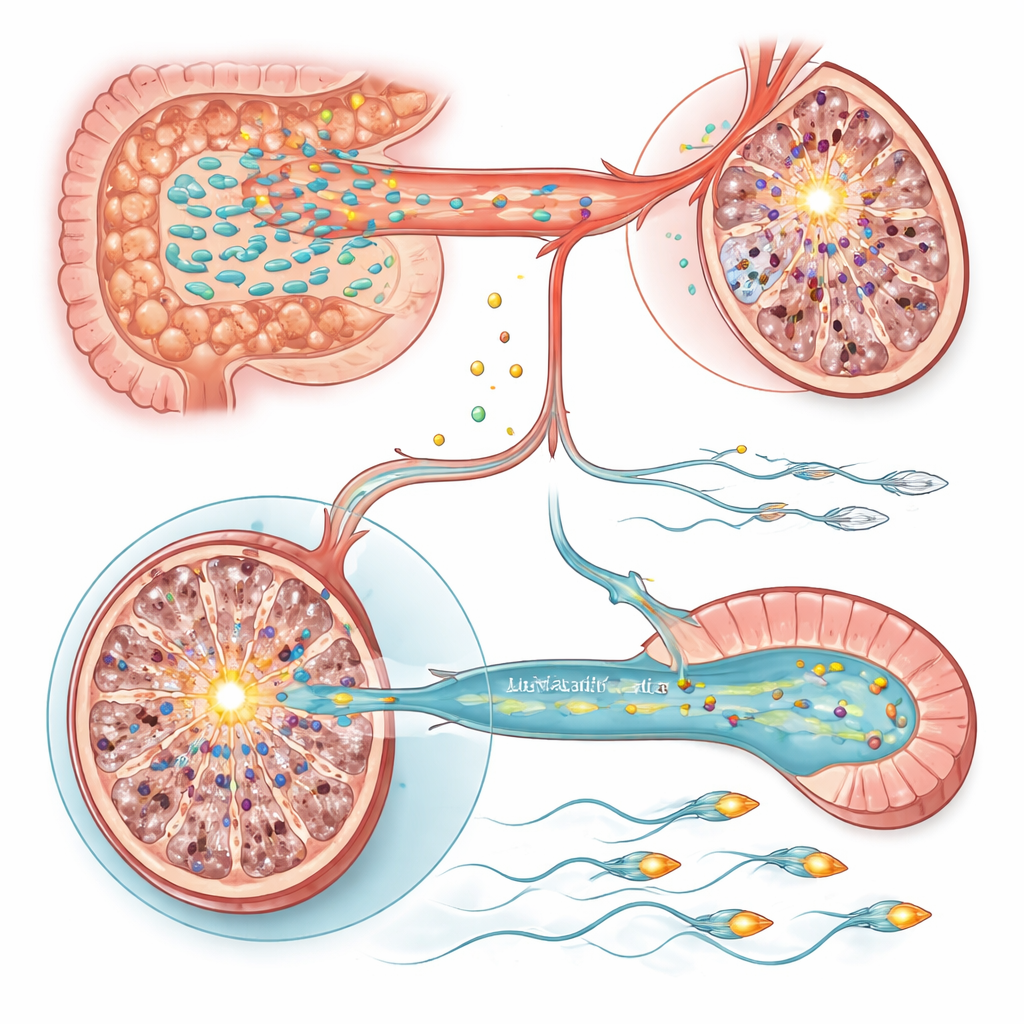
Due interruttori molecolari in testicoli e spermatozoi
Per capire come questi cambiamenti metabolici influenzano le cellule, il team ha esaminato l’attività genica nei testicoli e nell’epididimo, dove gli spermatozoi maturano. Nei testicoli dei ratti stressati è emerso un gene in particolare: Sting1, un interruttore maestro nelle vie immunitarie innate e di morte cellulare, era fortemente attivato. L’aumento artificiale di Sting1 in animali altrimenti sani è stato sufficiente a ridurre la produzione di spermatozoi, mentre il suo silenziamento nei ratti stressati ha in parte recuperato i numeri degli spermatozoi. Sia il trattamento con Lactobacillus sia l’integrazione con vitamine A ed E hanno abbassato l’attività di Sting1, collegando l’equilibrio microbico‑vitaminico a questo interruttore infiammatorio. Al contrario, la ridotta motilità degli spermatozoi è stata ricondotta all’epididimo, dove un gene chiamato Slc9c2, che codifica lo scambiatore ionico specifico per gli spermatozoi NHE11 che aiuta a controllare il pH interno e la funzione della coda, è stato soppresso dallo stress. Livelli più bassi di NHE11 erano associati a movimenti spermatici più deboli e a una ridotta capacità di subire i passaggi di attivazione necessari per la fertilizzazione. Ripristinare l’espressione di Slc9c2, oppure somministrare Lactobacillus o vitamine A/E, ha migliorato la motilità; la soppressione sperimentale di Slc9c2 ha annullato questi benefici.
Cosa significa per gli uomini sotto pressione
Nel complesso, lo studio delinea una catena di eventi che inizia con lo stress psicologico cronico e termina con spermatozoi meno numerosi e meno attivi. Gli ormoni dello stress indeboliscono la barriera intestinale e riducono le popolazioni di Lactobacillus, che a loro volta alterano acidi biliari e vitamine A ed E. Questi cambiamenti nutrizionali attivano una via di morte cellulare nei testicoli tramite Sting1, riducendo la produzione di spermatozoi, e attenuano l’attività di NHE11 nell’epididimo, rallentando la coda degli spermatozoi. Sebbene il lavoro sia stato condotto su ratti e siano necessarie ulteriori ricerche negli esseri umani, riformula alcuni casi di infertilità maschile come una condizione che coinvolge l’intero organismo — cervello, microbi intestinali, nutrienti e organi riproduttivi. Solleva inoltre la possibilità che strategie mirate di probiotici e integrazione vitaminica, insieme a interventi per la gestione dello stress, possano un giorno contribuire a proteggere o ripristinare la fertilità negli uomini che vivono con stress psicologico cronico.
Citazione: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
Parole chiave: infertilità maschile, stress cronico, microbiota intestinale, vitamine A ed E, motilità degli spermatozoi