Clear Sky Science · ru
Хронический стресс вызывает олигоастенозооспермию через ось микробиота кишечника — витамины — Sting1/Slc9c2
Когда стресс достигает репродуктивной системы
Многие знают, что хронический стресс истощает силы, нарушает сон и портит настроение, но немногие подозревают, что он также может незаметно подрывать мужскую фертильность. Это исследование на крысах выявляет, как длительный психологический стресс способен снижать число и подвижность сперматозоидов не только через гормоны, но и за счёт нарушения кишечных микробов и витаминов, которые они способствуют обеспечивать. Работа указывает на скрытую линию связи между мозгом, кишечником и яичками и предполагает, что поддержка полезных бактерий и ключевых нутриентов в будущем может помочь защитить фертильность у мужчин под стрессом.
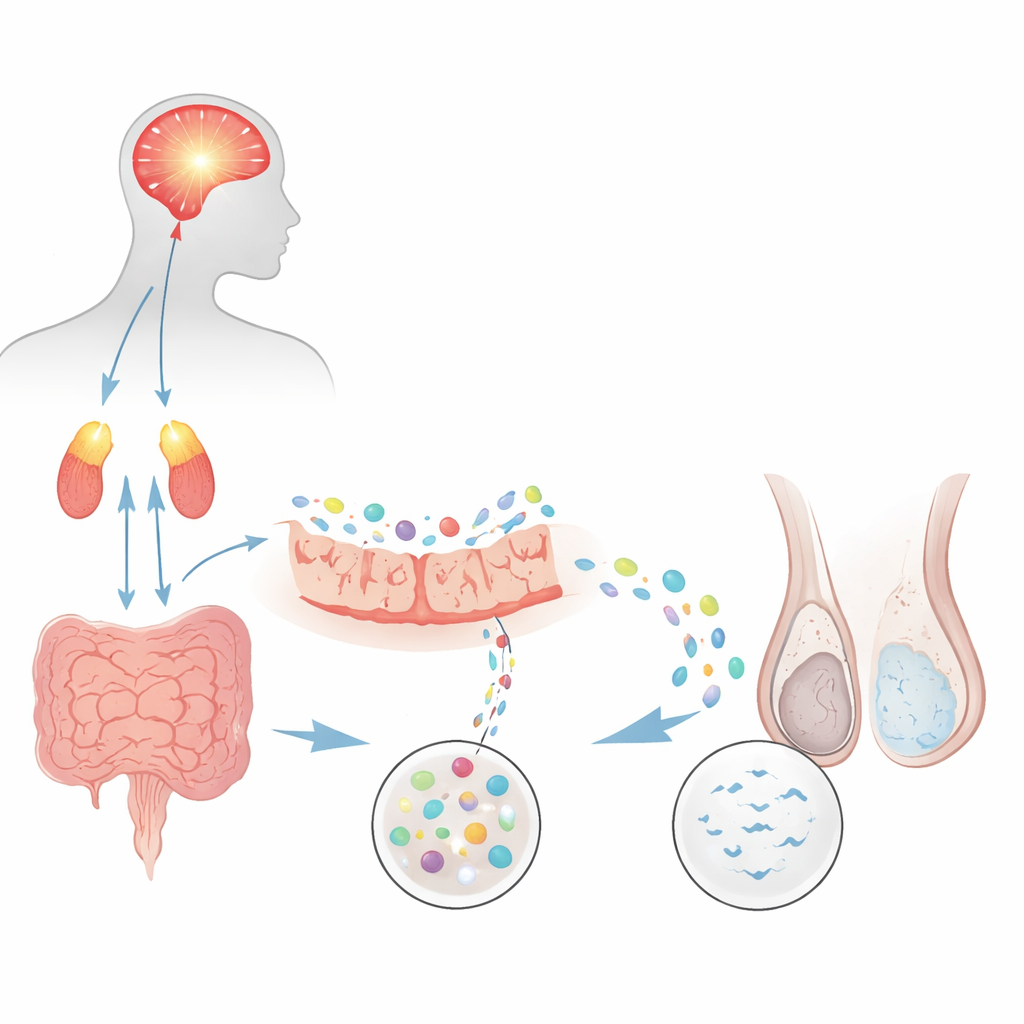
От психического напряжения к меньшему числу сперматозоидов
Исследователи сперва проверили, может ли хорошо изученная модель хронического психологического стресса у крыс воспроизвести распространённую форму мужского бесплодия — олигоастенозооспермию, при которой сперматозоидов и слишком мало, и они недостаточно подвижны. Крысы, многократно подвергавшиеся вынужденному плаванию, развили выраженные признаки тревоги и депрессии вместе с повышением гормонов стресса оси мозг‑надпочечники. При автоматизированном анализе семенной жидкости у испытывающих стресс животных концентрация сперматозоидов была примерно вдвое ниже, а подвижность заметно снижена по сравнению с контролем. Маркёры сперматогенеза в яичках также упали, а тесты на спаривание показали меньше беременностей и меньшие помёты. В сумме эти данные показывают, что постоянный стресс сам по себе может повреждать продукцию и работоспособность спермы.
Кишечник как посредник
Поскольку кишечник очень чувствителен к гормонам стресса, команда далее изучила состояние пищеварительного тракта. У стрессовых крыс ослабели белковые уплотнения, которые обычно укрепляют кишечный эпителий, что указывает на «проницаемость» барьера. Блокирование глюкокортикоидного рецептора — главной мишени гормонов стресса — с помощью препарата в значительной мере восстановило и целостность кишечника, и качество спермы, связывая повреждение с гормональной сигнализацией. Чтобы проверить, участвуют ли сами кишечные микробы в проблеме, учёные пересадили фекальную микробиоту от доноров со стрессом или от контролей новым крысам, чья собственная микробиота была уничтожена антибиотиками. Животные, получившие микробы от стрессовых доноров, развили те же низкие показатели числа сперматозоидов, снижение подвижности и ухудшение фертильности, хотя сами никогда не подвергались стрессу, что показывает: нарушённые сообщества кишечных бактерий могут вызывать репродуктивные проблемы на расстоянии.
Полезная бактерия и недостающие витамины
Профилирование микробной ДНК показало, что хронический стресс снижает общую разнообразность в тонком кишечнике и в частности истощает популяции Lactobacillus — группы бактерий, часто ассоциируемых со здоровьем кишечника и репродуктивной системы. Обилие этих микробов тесно коррелировало с количеством сперматозоидов и их подвижностью. При пероральном введении Lactobacillus в течение всего периода стресса у крыс качество спермы и маркёры в яичках улучшилось, а показатели фертильности приблизились к норме. Одновременно химический анализ содержимого кишечника, крови и яичек выявил, что стресс нарушает обмен желчных кислот и жирорастворимых витаминов, особенно витаминов A и E, важных для развития зародышевых клеток и защиты от окислительного повреждения. Уровни нескольких желчных кислот и этих витаминов падали в крови и в тестикулярной ткани, и эти снижения были тесно связаны как с потерей Lactobacillus, так и с ухудшением сперматологических параметров.
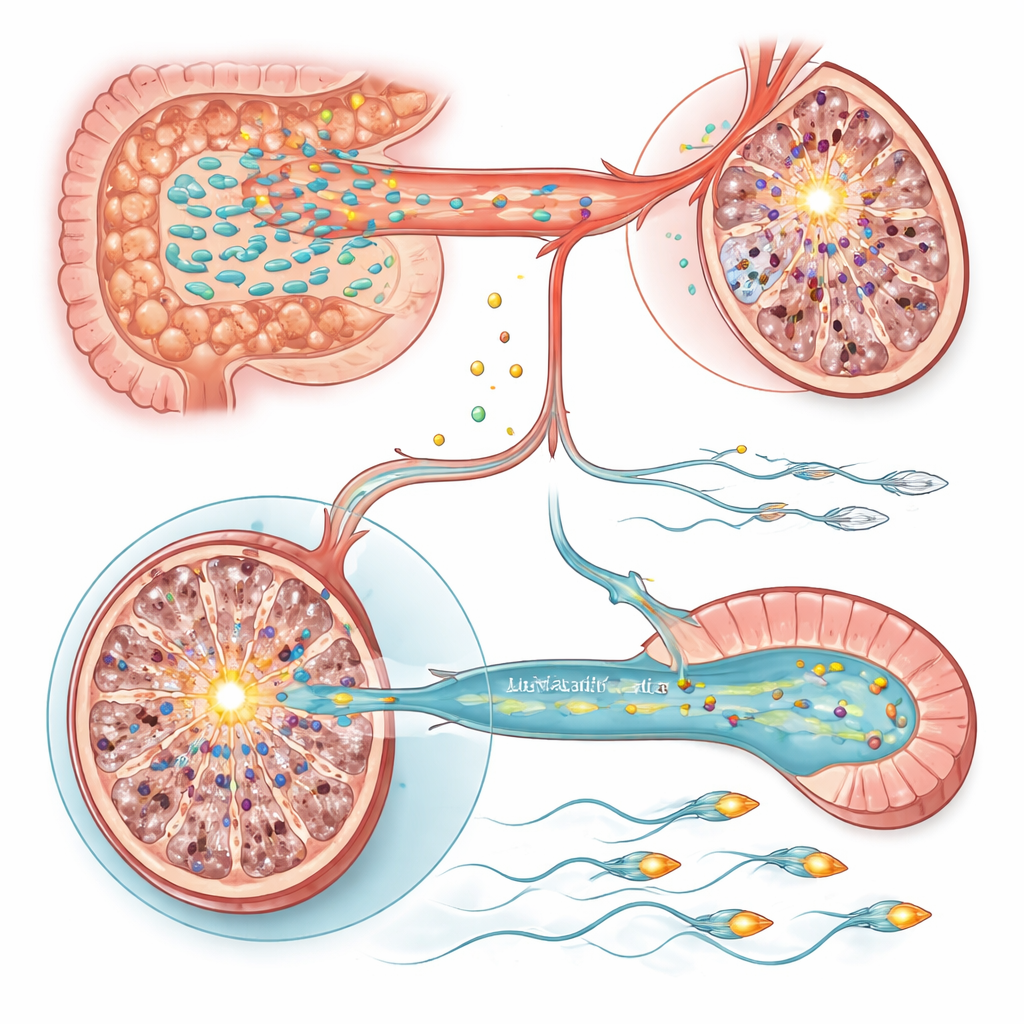
Два молекулярных переключателя в яичках и сперме
Чтобы понять, как эти метаболические изменения влияют на клетки, команда изучила активность генов в яичках и придатке яичка, где созревают сперматозоиды. В яичках стрессовых крыс выделялся один ген: Sting1, главный переключатель в путях врождённого иммунитета и программируемой гибели клеток, был сильно активирован. Искусственное усиление Sting1 у относительно здоровых животных было достаточным, чтобы снизить продукцию спермы, тогда как приглушение этого гена у стрессовых крыс частично восстановило число сперматозоидов. И лечение Lactobacillus, и добавки витаминов A и E снижали активность Sting1, связывая микробно‑опосредованное нарушение витаминного баланса с этим воспалительным переключателем. Напротив, снижение подвижности спермы связано с придатком яичка, где ген Slc9c2, кодирующий специфичный для сперматозоидов ионный обменник NHE11, помогающий контролировать внутренний pH и работу хвоста, был подавлен стрессом. Низкий уровень NHE11 ассоциировался со слабым движением сперматозоидов и нарушением их способности проходить активационные этапы, необходимые для оплодотворения. Восстановление экспрессии Slc9c2 или приём Lactobacillus и добавок витаминов A/E улучшали подвижность, а экспериментальное подавление Slc9c2 аннулировало эти улучшения.
Что это значит для мужчин под давлением
В целом исследование описывает цепочку событий: от хронического психологического напряжения до уменьшения числа и активности сперматозоидов. Гормоны стресса ослабляют кишечный барьер и сокращают полезные популяции Lactobacillus, что в свою очередь нарушает баланс желчных кислот и витаминов A и E. Эти нутритивные сдвиги активируют путь клеточной смерти в яичках через Sting1, сокращая сперматогенез, и ослабляют активность NHE11 в придатке яичка, замедляя работу хвостов сперматозоидов. Хотя работа проведена на крысах и требуется больше исследований на людях, это меняет представление о некоторых случаях мужского бесплодия как о состоянии всего организма, включающем мозг, кишечные микробы, питательные вещества и репродуктивные органы. Также это наводит на мысль, что тщательно подобранные пробиотические и витаминные стратегии в сочетании с управлением стрессом в будущем могли бы помочь защитить или восстановить фертильность у мужчин, живущих с хроническим психологическим стрессом.
Цитирование: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
Ключевые слова: мужское бесплодие, хронический стресс, микробиота кишечника, витамины A и E, подвижность сперматозоидов