Clear Sky Science · ja
慢性ストレスは腸内細菌—ビタミン—Sting1/Slc9c2軸を介して乏精子無力症を引き起こす
ストレスが生殖系に及ぶとき
慢性的なストレスが体力を奪い、睡眠を乱し、気分を曇らせることは多くの人が知っていますが、それが男性の生殖能力を静かに損なう可能性があることに気づく人は少ないでしょう。本研究はラットを用いて、持続する心理的ストレスがホルモンだけでなく、腸内微生物とそれらが供給を助けるビタミンを乱すことで精子数と運動性を減らしうる仕組みを明らかにします。この仕事は脳、腸、精巣の間に隠れた連絡経路があることを示し、有益な細菌と重要な栄養素を支えることが、いつかストレスを抱える男性の生殖能力を守る助けになるかもしれないことを示唆します。
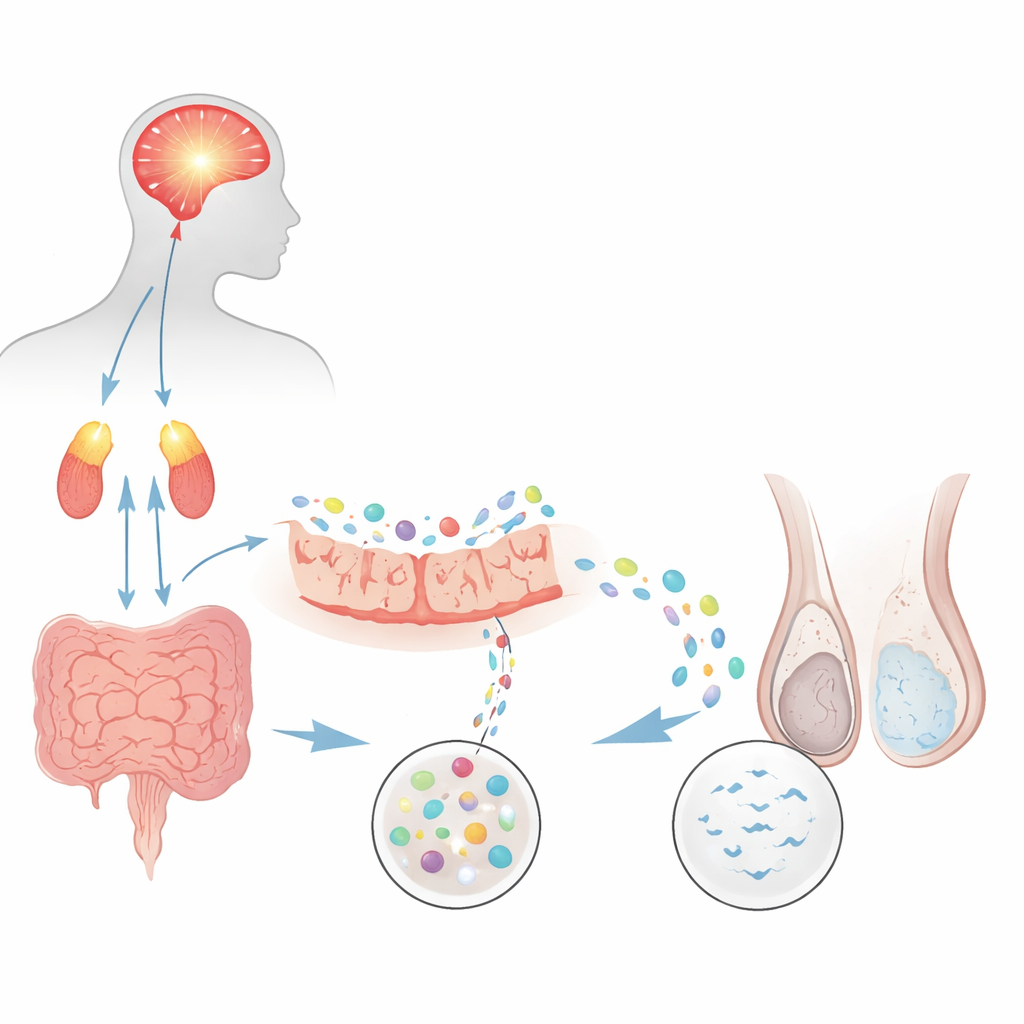
精神的負担から精子減少へ
研究者たちはまず、確立されたラットの慢性心理的ストレスモデルが、精子数が少なく運動性が低いという男性不妊の一般的な形態である乏精子無力症を再現できるかを調べました。強制泳法を繰り返し与えられたラットは不安や抑うつの強い兆候を示し、脳—副腎系からのストレスホルモンが上昇しました。自動化された解析で精液を調べると、ストレス群の精子濃度は対照のほぼ半分で、運動性も著しく低下していました。精巣内の精子形成のマーカーも低下し、交配試験では妊娠数と子犬数が減少しました。これらの結果は、持続的なストレスだけで精子の産生と機能を損なえることを示しています。
仲介者としての腸
腸管はストレスホルモンに非常に敏感であることから、研究チームは次に腸に着目しました。ストレスを受けたラットでは、腸粘膜を通常締めるタンパク質の結合が弱まり、「リーキー(漏れやすい)」バリアが示唆されました。ストレスホルモンの主要な受容体であるグルココルチコイド受容体を薬物で遮断すると、腸の完全性と精子の質が大きく回復し、損傷がホルモンシグナル伝達に結びつくことが示されました。腸内微生物自体が問題に関与しているかを確かめるために、研究者らはストレス群または対照群のドナーから糞便微生物を移植し、抗生物質で自分の微生物を消した新しいラットに移しました。ストレス由来の微生物を受け取った動物は、本人がストレスにさらされていないにもかかわらず、同様の低い精子数、運動性低下、受胎率低下を示し、障害された腸内群集が遠隔的に生殖問題を引き起こしうることを明らかにしました。
有益な菌と欠乏するビタミン
微生物DNAプロファイリングは、慢性ストレスが小腸の全体的な多様性を減らし、特に腸と生殖の健康に関連することが多いLactobacillus(ラクトバチルス)を枯渇させることを示しました。これらの微生物の豊富さは精子数と運動性と強く相関しました。ストレス期間を通じて経口でラクトバチルスを投与したところ、精液の質と精巣マーカーは改善し、受胎結果も正常に近づきました。同時に、腸内容物、血液、精巣の化学解析は、ストレスが胆汁酸や脂溶性ビタミン、特に生殖細胞の発生や酸化的ダメージからの保護に重要なビタミンAとEを攪乱することを明らかにしました。いくつかの胆汁酸とこれらのビタミンのレベルは循環と精巣組織で低下し、これらの低下はラクトバチルスの喪失および悪化する精子パラメーターと密接に結びついていました。
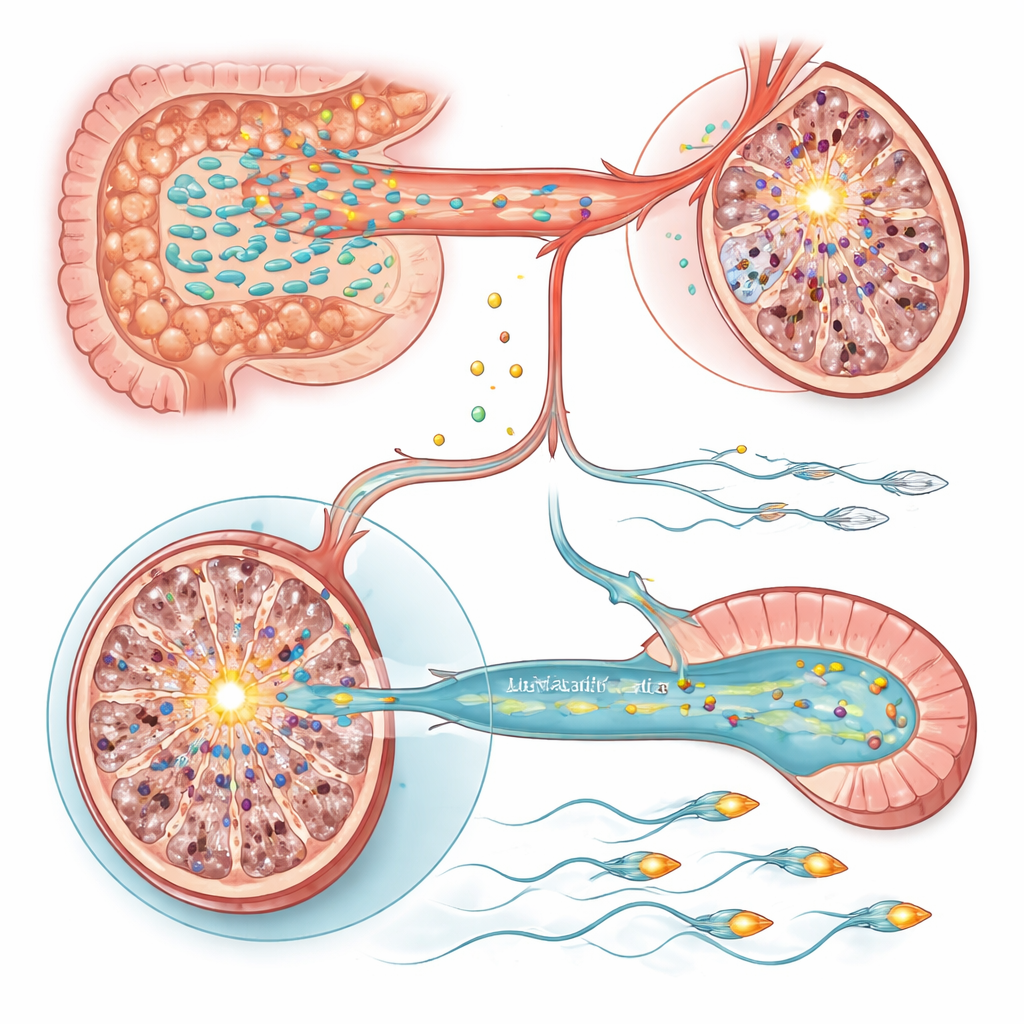
精巣と精子における二つの分子スイッチ
これらの代謝変化が細胞にどのように影響するかを理解するため、チームは精巣と精子が成熟する副睾丸での遺伝子発現を調べました。ストレスを受けたラットの精巣では、ひとつの遺伝子が際立っていました:自然免疫や細胞死経路のマスタースイッチであるSting1が強く活性化していました。Sting1を人工的に上げた健康な動物でも精子産生は減少し、ストレス群でSting1をサイレンシングすると精子数が部分的に回復しました。ラクトバチルス療法とビタミンA・Eの補給はいずれもSting1の活性を低下させ、微生物によるビタミンバランスとこの炎症性スイッチを結びつけました。一方、精子運動性の低下は副睾丸に由来し、精子特異的なイオン交換タンパク質NHE11をコードするSlc9c2という遺伝子がストレスによって抑制されていました。NHE11の低下は精子運動の弱化や受精に必要な活性化段階の障害と関連しました。Slc9c2の発現回復、あるいはラクトバチルスやビタミンA/Eの補給は運動性を改善し、実験的にSlc9c2をノックダウンするとこれらの改善効果は消失しました。
プレッシャー下の男性にとっての意味
総じて、この研究は慢性的な心理的ストレスから始まり、より少なく活動的な精子で終わる一連の事象を描きます。ストレスホルモンは腸のバリアを弱め、有益なラクトバチルスの集団を縮小させ、それが胆汁酸やビタミンA・Eを乱します。これらの栄養変化はSting1を介して精巣の細胞死経路をオンにして精子産生を削ぎ、同時に副睾丸でのNHE11活性を低下させて精子尾部の働きを鈍らせます。本研究はラットで行われたものでありヒトでのさらなる研究が必要ですが、ある種の男性不妊を脳、腸内微生物、栄養、そして生殖器を含む全身的な状態として再定義する観点を提供します。また、適切に設計されたプロバイオティクスやビタミン投与戦略とストレス管理を組み合わせることで、慢性的な心理的ストレスに晒される男性の生殖能力を保護・回復する可能性を示唆しています。
引用: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
キーワード: 男性不妊, 慢性ストレス, 腸内細菌叢, ビタミンAとE, 精子運動性