Clear Sky Science · pl
Przewlekły stres powoduje oligoasthenozoospermię poprzez oś mikrobiota jelitowa‑witamina‑Sting1/Slc9c2
Kiedy stres sięga układu rozrodczego
Większość ludzi wie, że przewlekły stres potrafi wyniszczyć energię, zaburzyć sen i psuć nastrój, ale niewielu zdaje sobie sprawę, że może on także podstępnie osłabiać męską płodność. Badanie na szczurach odkrywa, jak długotrwały stres psychologiczny może zmniejszać liczbę i ruchliwość plemników — nie tylko poprzez hormony, lecz także przez zaburzenia mikrobioty jelitowej i witamin, które mikroby pomagają dostarczać. Praca wskazuje na ukrytą linię komunikacji między mózgiem, jelitami a jądrami — i sugeruje, że wspieranie korzystnych bakterii oraz kluczowych składników odżywczych może w przyszłości pomóc chronić płodność u zestresowanych mężczyzn.
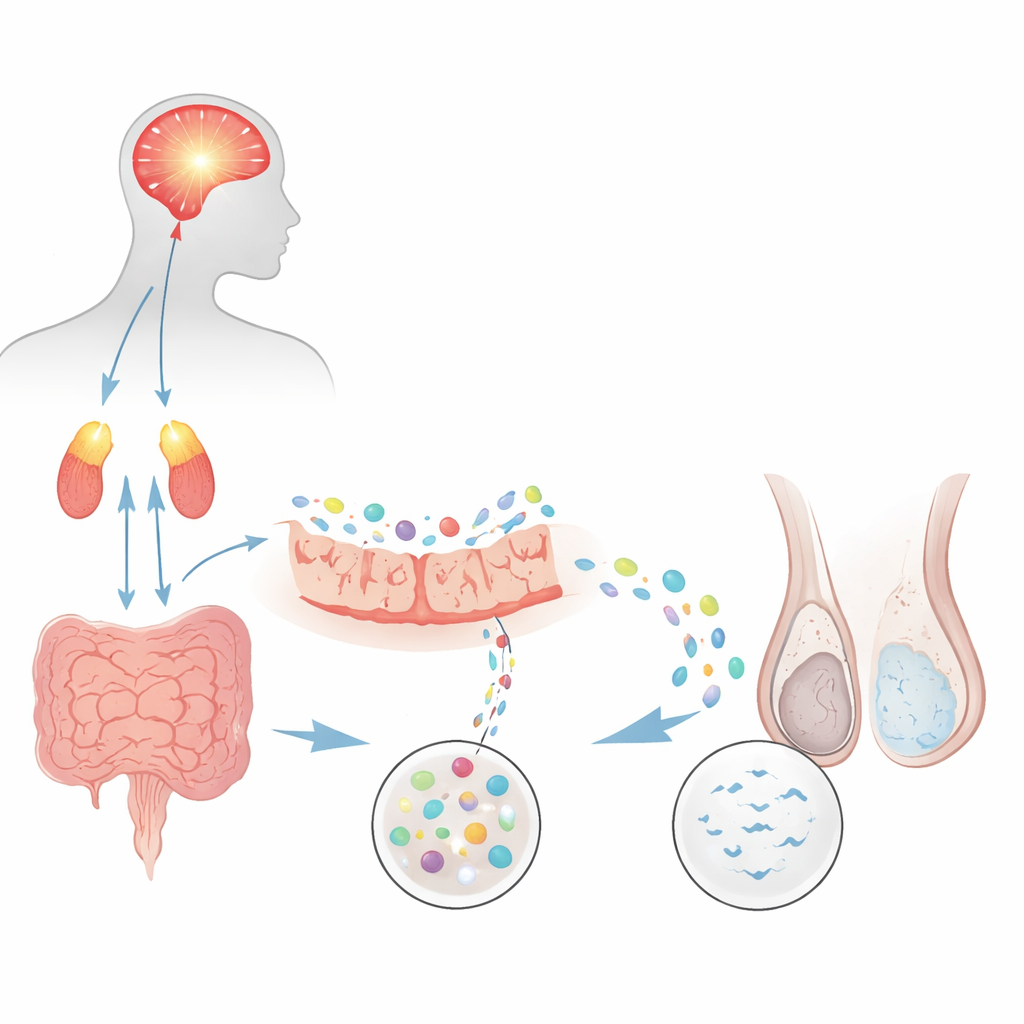
Od napięcia psychicznego do mniejszej liczby plemników
Naukowcy najpierw sprawdzili, czy dobrze ustalony model przewlekłego stresu psychologicznego u szczurów odwzorowuje powszechną postać męskiej niepłodności zwaną oligoasthenozoospermią, w której plemników jest za mało i są one zbyt słabo ruchliwe. Szczury wielokrotnie wystawiane na przymusowe pływanie rozwinęły silne objawy lęku i depresji oraz podwyższone hormony stresu z osi mózg‑nadnercza. Po badaniu nasienia za pomocą narzędzi zautomatyzowanych okazało się, że zwierzęta zestresowane miały mniej więcej o połowę mniejsze stężenie plemników i wyraźnie niższą ruchliwość w porównaniu do grupy kontrolnej. Markerzy rozwoju plemników w jądrach również spadły, a próby z kojarzeniem wykazały mniej ciąż i mniejsze mioty. W sumie wyniki te pokazały, że przewlekły stres sam w sobie może upośledzać produkcję i funkcję plemników.
Jelito jako pośrednik
Ponieważ przewód pokarmowy jest wysoce wrażliwy na hormony stresu, badacze przyjrzeli się następnie jelitom. U szczurów zestresowanych osłabły białkowe zamki normalnie uszczelniające wyściółkę jelitową, co sugerowało „przeciekającą” barierę. Zablokowanie receptora glukokortykoidowego — głównego miejsca wiązania hormonów stresu — za pomocą leku w dużej mierze przywróciło zarówno integralność jelit, jak i jakość nasienia, łącząc uszkodzenie z sygnalizacją hormonalną. Aby sprawdzić, czy same mikroby jelitowe są częścią problemu, naukowcy przeszczepili kałowe bakterie od dawców zestresowanych lub kontrolnych do nowych szczurów, których własna mikrobiota została zniesiona przez antybiotyki. Zwierzęta otrzymujące mikroby od dawców zestresowanych rozwinęły te same niskie liczby plemników, obniżoną ruchliwość i zmniejszoną płodność, chociaż nigdy nie były poddane stresowi, co ujawniło, że zaburzone społeczności bakteryjne mogą zdalnie wywoływać problemy rozrodcze.
Pomocna bakteria i brakujące witaminy
Profilowanie DNA mikrobioty wykazało, że przewlekły stres zmniejsza ogólną różnorodność w jelicie cienkim i w szczególności wyczerpuje populacje Lactobacillus, grupy bakterii często kojarzonej ze zdrowiem jelit i układu rozrodczego. Obecność tych mikroorganizmów silnie korelowała z liczbą plemników i ich ruchliwością. Gdy szczury zestresowane otrzymywały doustnie Lactobacillus przez cały okres stresu, jakość nasienia i markery jądrowe poprawiły się, a wyniki płodności wróciły w kierunku normy. Równocześnie analizy chemiczne treści jelitowej, krwi i jąder wykazały, że stres zakłócił kwasy żółciowe i rozpuszczalne w tłuszczach witaminy, zwłaszcza witaminy A i E, które są ważne dla rozwoju komórek zarodkowych i ochrony przed stresem oksydacyjnym. Poziomy kilku kwasów żółciowych i tych witamin spadły w krążeniu i w tkance jądra, a te spadki były ściśle powiązane zarówno z utratą Lactobacillus, jak i z pogorszeniem parametrów nasienia.
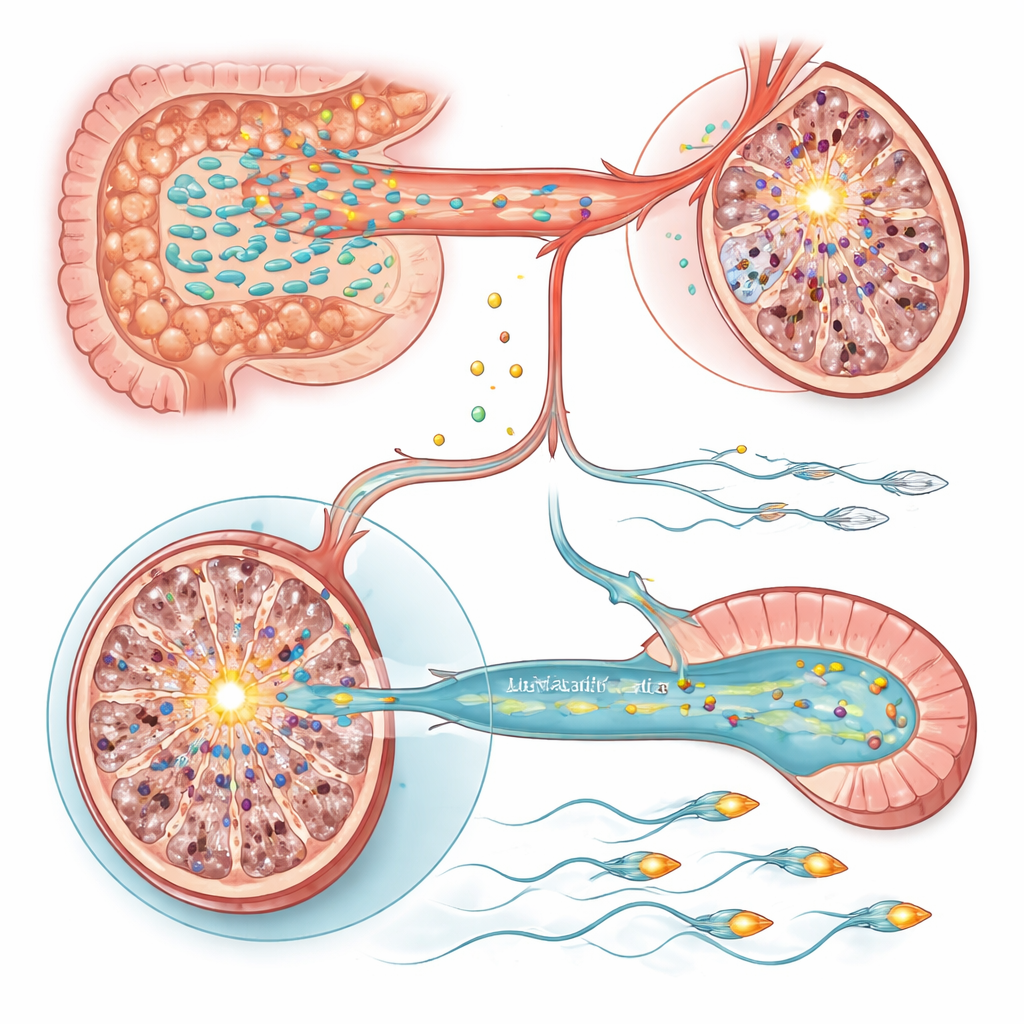
Dwa molekularne przełączniki w jądrze i plemniku
Aby zrozumieć, jak te zmiany metaboliczne wpływają na komórki, zespół zbadał aktywność genów w jądrach i najądrzu, gdzie plemniki dojrzewają. W jądrach szczurów zestresowanych wyróżniał się jeden gen: Sting1, główny przełącznik w szlakach odporności wrodzonej i apoptozy, był silnie aktywowany. Sztuczne zwiększenie aktywności Sting1 u inaczej zdrowych zwierząt wystarczyło, by zmniejszyć produkcję plemników, podczas gdy wyciszenie go u szczurów zestresowanych częściowo przywróciło liczbę plemników. Zarówno leczenie Lactobacillus, jak i suplementacja witaminami A i E obniżały aktywność Sting1, łącząc równowagę witamin zależnych od mikrobioty z tym zapalnym przełącznikiem. Natomiast zmniejszona ruchliwość plemników wiązała się z najądrzem, gdzie gen Slc9c2, kodujący specyficzny dla plemników wymiennik jonowy NHE11, pomagający kontrolować wewnętrzne pH i funkcję witki, był tłumiony przez stres. Niższy poziom NHE11 korelował ze słabszym ruchem plemników i upośledzoną zdolnością do przejścia etapów aktywacji niezbędnych do zapłodnienia. Przywrócenie ekspresji Slc9c2, albo podanie Lactobacillus lub witamin A/E, poprawiało ruchliwość, a eksperymentalne wyciszenie Slc9c2 niweczyło te korzyści.
Co to znaczy dla mężczyzn pod presją
Podsumowując, badanie przedstawia łańcuch zdarzeń rozpoczynający się od przewlekłego napięcia psychicznego i kończący się mniejszą liczbą oraz mniejszą aktywnością plemników. Hormony stresu osłabiają barierę jelitową i zmniejszają populacje korzystnych Lactobacillus, co z kolei zaburza kwasy żółciowe oraz witaminy A i E. Te zmiany odżywcze uruchamiają ścieżkę śmierci komórkowej w jądrach za pośrednictwem Sting1, ograniczając produkcję plemników, oraz osłabiają aktywność NHE11 w najądrzu, spowalniając ruch witki. Chociaż praca została przeprowadzona na szczurach i potrzebne są dalsze badania u ludzi, nadaje to nową perspektywę niektórym przypadkom męskiej niepłodności jako schorzeniu ogólnoustrojowemu obejmującemu mózg, mikroby jelitowe, składniki odżywcze i organy rozrodcze. Wynika z tego również możliwość, że starannie zaprojektowane strategie probiotyczne i suplementacja witamin, wraz z zarządzaniem stresem, mogą pewnego dnia pomóc chronić lub przywrócić płodność u mężczyzn żyjących w przewlekłym stresie psychologicznym.
Cytowanie: Zheng, JC., Jin, ZR., Liu, BH. et al. Chronic stress drives oligoasthenozoospermia via gut microbiota-vitamin-Sting1/Slc9c2 axis. Nat Commun 17, 4108 (2026). https://doi.org/10.1038/s41467-026-72450-4
Słowa kluczowe: męska niepłodność, przewlekły stres, mikrobiota jelitowa, witamina A i E, ruchliwość plemników