Clear Sky Science · zh
部分占位的异四聚体结构揭示卡因酸受体的激活与脱敏机制
为何这些微小的脑内开关很重要
卡因酸受体是帮助神经元互相通信的微观蛋白开关。它们对神经递质谷氨酸有反应,参与从学习和记忆到疼痛与炎症等多种过程。当这些开关失常时,与癫痫和精神疾病等病症相关联。本研究前所未有地从结构层面探讨了一类主要卡因酸受体在仅部分亚基被类谷氨酸分子占位时如何被激活并随后“自我关闭”——这种情形很可能反映了许多真实突触中的实际状态。
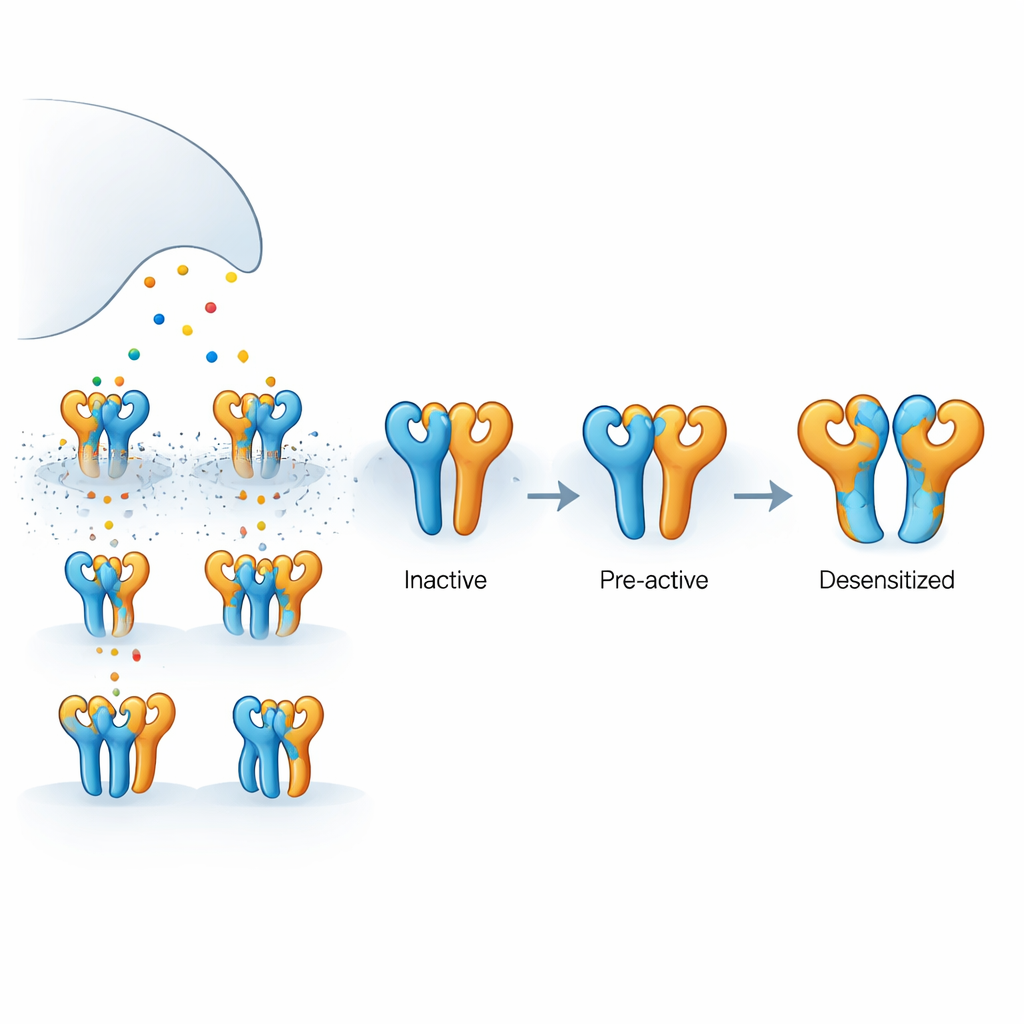
这种脑受体的构造
这里研究的受体由两种蛋白亚基构成,称为GluK2和GluK5,组装成四聚体复合物。GluK5对谷氨酸的结合尤其紧密,倾向于占据四聚体中的两个特定位置,而GluK2占据另外两个位置。每个亚基具有负责捕获谷氨酸的外层结构域和形成内孔以让离子流动、产生电信号的孔区。由于谷氨酸释放短暂且被迅速清除,四个亚基并不总是同时被占位。理解仅部分亚基被结合时发生的事情,是解释真实突触如何调节信号强度和时序的关键。
部分按下的触发器但不致卡死
通过对人细胞的电生理记录,作者显示一种选择性作用于GluK5的激动剂5-碘威拉立定(5-iodowillardiine)可以在GluK2/GluK5受体上维持稳定电流,而不诱导受体发生“脱敏”——即通常在激活后出现的自我保护性关闭。相比之下,天然递质谷氨酸会使相同受体快速开启然后迅速沉默。另一种激动剂AMPA也能激活这些受体,但只导致部分脱敏。这些行为表明,当仅GluK5亚基被占位时,受体可以打开或接近开启而不陷入长期的非活性状态,而更广泛的结合则会将受体推向更深的关闭构象。
动作部件的三维快照
为观测这些不同功能状态在三维中的样貌,研究团队用低温电子显微镜在精确控制的配体条件下捕捉了结构快照。在存在GluK5选择性激动剂时,他们观察到两种主要构象。一种构象中,四个配体结合域形成完整的配对,GluK5单元围绕配体闭合而GluK2单元保持开放。该“完整”状态显示成对结构之间的细微松动和旋转,以及内孔螺旋的可测扩张,这与一种预激活、准备开启的构型相一致,尽管离子通道仍处于关闭状态。在第二种“部分断裂”状态中,一对域已分离而另一对仍然完整,提示这是通向完全脱敏路径上的一个中间态,但尚未被锁定为不可逆的关闭态。
调节时序的隐秘铰链
通过将这些结构与先前解析的完全活化和完全脱敏的卡因酸受体进行比较,作者追踪了外层域运动如何传递到孔区。他们识别出域内和域对之间的关键接触区域,这些区域充当铰链与支撑,尤其集中在复合物中相对而坐的两个GluK5亚基周围。这些位点的细微位移改变了域之间的结合强度以及它们对拉动孔开启的连接子产生的牵引力。当研究者在这些界面置换某些氨基酸时,可以使受体失活更快或更慢,并改变其脱敏的倾向。这有助于解释为何含GluK5的受体在短暂的谷氨酸冲击后仍能异常地长时间保持活性。
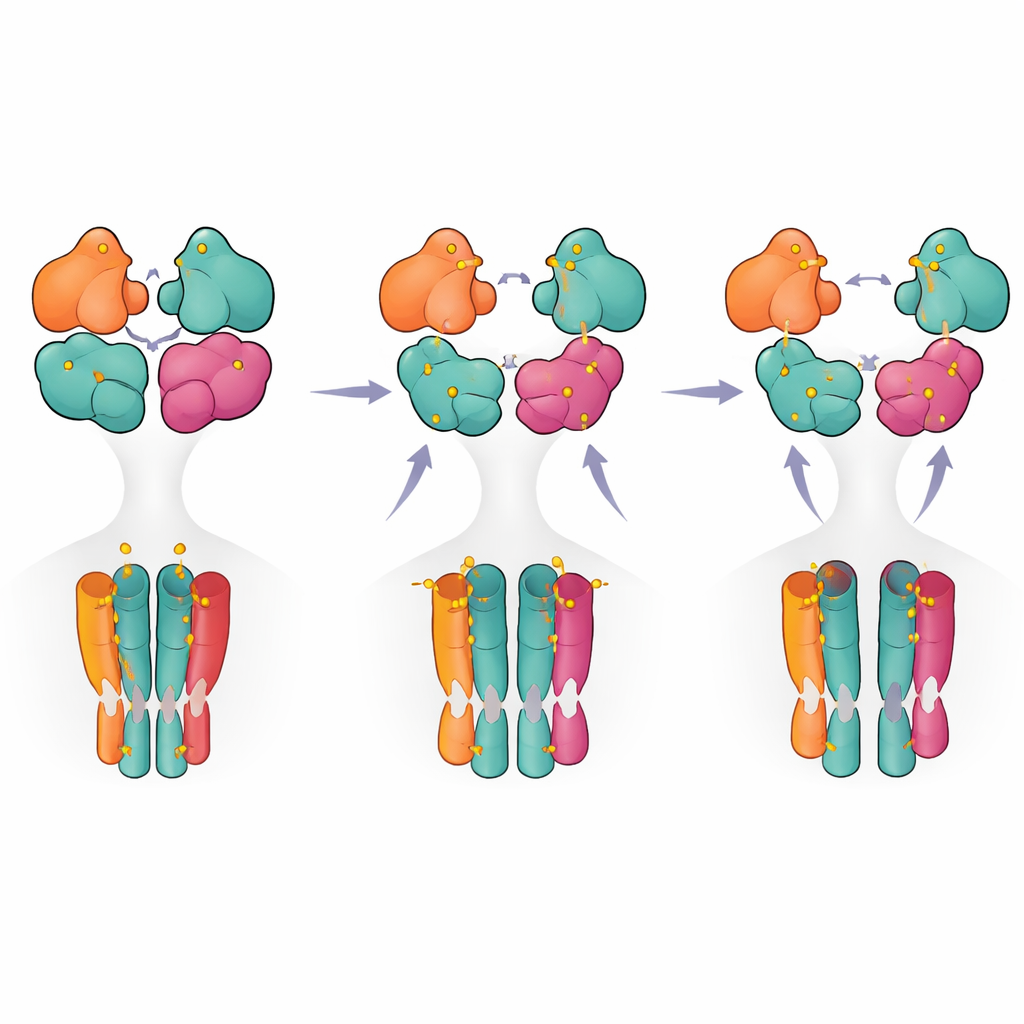
从激活到关闭的分步路线图
结合结构快照和功能测量结果,作者提出了一个分步模型:当仅有两个亚基(通常是GluK5对)被占位时,受体由静息态转入预激活态。更多配体结合会促使一对域部分断裂,而只有当三或四个亚基被占位时,受体才达到与长期脱敏相关的完全断裂构象。对非专业读者而言,这意味着该受体不像简单的开—关开关,而更像多步调光器,不同的占位模式和内部接触调节信号的强度和持续时间。这些见解不仅澄清了这一关键脑受体的基本工作原理,还突出了可被未来药物针对以在疾病中精细调控卡因酸受体活性的结构热点。
引用: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
关键词: 卡因酸受体, 谷氨酸信号传导, 突触传输, 冷冻电镜结构, 受体脱敏