Clear Sky Science · de
Strukturen teilweise besetzter Hetero-Tetramere geben Einblick in Aktivierung und Desensitivierung von Kainat-Rezeptoren
Warum winzige Schalter im Gehirn wichtig sind
Kainat-Rezeptoren sind mikroskopische Proteinschalter, die Nervenzellen helfen, miteinander zu kommunizieren. Sie sprechen auf den Neurotransmitter Glutamat an und sind an Prozessen von Lernen und Gedächtnis bis hin zu Schmerz und Entzündung beteiligt. Wenn diese Schalter fehlreguliert werden, stehen sie im Zusammenhang mit Erkrankungen wie Epilepsie und psychiatrischen Störungen. Diese Studie untersucht in beispielloser struktureller Detailtiefe, wie ein wichtiger Typ von Kainat-Rezeptoren anschaltet und sich dann „selbst abschaltet“, wenn nur einige seiner Untereinheiten von glutamatähnlichen Molekülen besetzt sind — eine Situation, die wahrscheinlich dem entspricht, was an vielen echten Synapsen tatsächlich passiert.
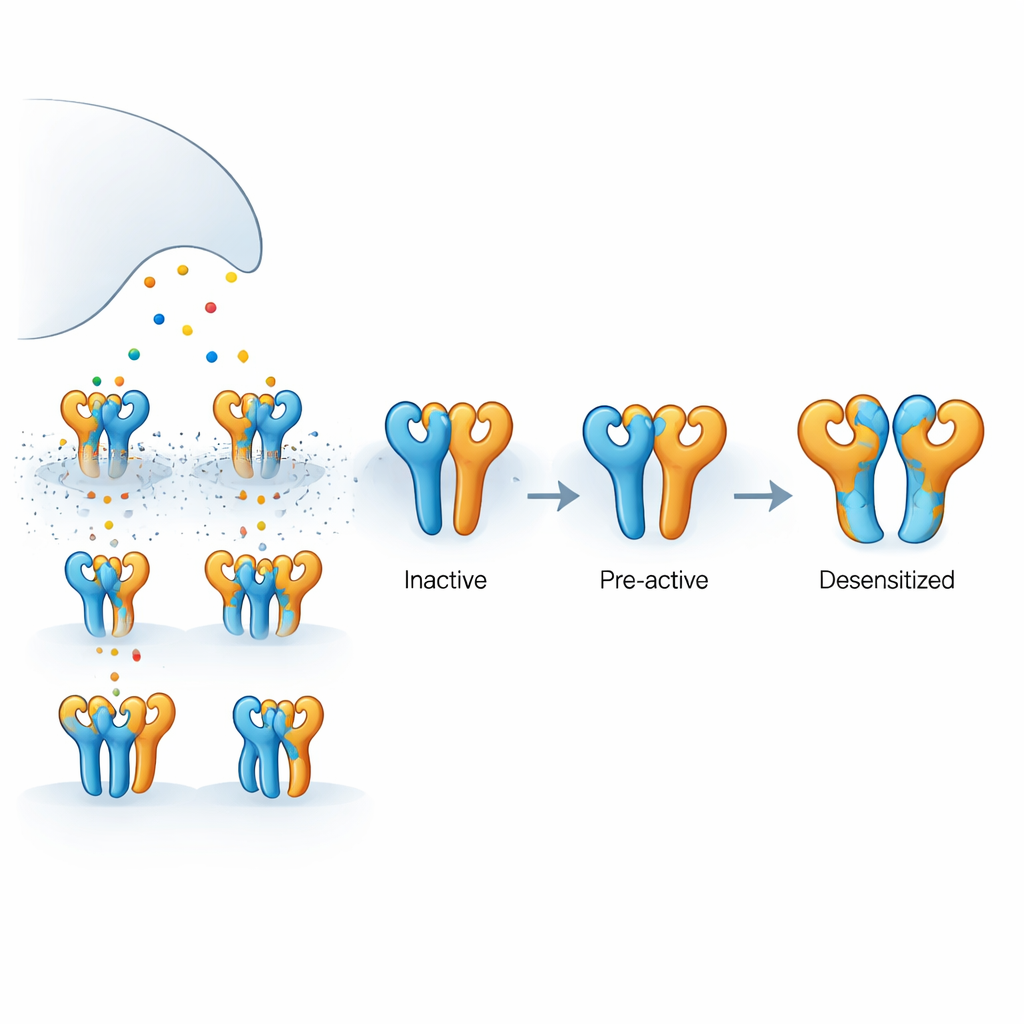
Wie dieser Hirnrezeptor aufgebaut ist
Der hier untersuchte Rezeptor ist ein Kainat-Rezeptor, der aus zwei Arten von Proteinsubeinheiten besteht, GluK2 und GluK5, die zu einem vierteiligen Komplex zusammengesetzt sind. GluK5 bindet Glutamat besonders fest und belegt typischerweise zwei spezifische Positionen im Tetramer, während GluK2 die anderen beiden einnimmt. Jede Untereinheit besitzt eine äußere Domäne, die Glutamat einfängt, und einen inneren, porebildenden Bereich, der Ionenfluss zulässt und elektrische Signale erzeugt. Da Glutamat nur kurz freigesetzt und schnell wieder aufgenommen wird, sind nicht immer alle vier Untereinheiten gleichzeitig besetzt. Zu verstehen, was passiert, wenn nur einige besetzt sind, ist entscheidend, um zu erklären, wie echte Synapsen Signalstärke und -timing modulieren.
Teilweise gedrückte Auslöser, die nicht blockieren
Mithilfe elektrischer Aufzeichnungen aus humanen Zellen zeigten die Autoren, dass ein GluK5-selektives Wirkstoff, 5-Iodowillardin, einen gleichmäßigen Strom durch GluK2/GluK5-Rezeptoren antreibt, ohne dass diese „desensitivieren“ — das selbstschützende Abschalten, das normalerweise auf die Aktivierung folgt. Im Gegensatz dazu sorgt der natürliche Transmitter Glutamat dafür, dass dieselben Rezeptoren sich ein- und dann sehr schnell wieder stummschalten. Ein anderer Wirkstoff, AMPA, aktiviert diese Rezeptoren ebenfalls, führt aber nur zu teilweiser Desensitivierung. Dieses Verhalten deutet darauf hin, dass der Rezeptor geöffnet werden kann oder sich einer Öffnung nähert, wenn nur die GluK5-Untereinheiten besetzt sind, ohne in einen langanhaltenden inaktiven Zustand zu verfallen, während eine weiter verbreitete Bindung den Rezeptor in eine tiefere Abschaltkonfiguration treibt.
Schnappschüsse bewegter Teile in Aktion
Um zu sehen, wie diese unterschiedlichen funktionellen Zustände dreidimensional aussehen, nutzte das Team kryogene Elektronenmikroskopie, um strukturelle Schnappschüsse unter genau kontrollierten Ligandbedingungen einzufangen. Mit dem GluK5-selektiven Agonisten beobachteten sie zwei Hauptkonformationen. In einer bildeten alle vier Ligandenbindedomänen intakte Paare, wobei die GluK5-Einheiten um das Ligand geschlossen waren und die GluK2-Einheiten offen blieben. Dieser „intakte“ Zustand zeigte subtile Lockerung und Rotation zwischen den gepaarten Domänen sowie eine messbare Expansion der inneren Pore-Helices, konsistent mit einer voraktiven, bereit-zu-öffnen-Konfiguration, obwohl der Ionenkanal noch geschlossen war. Im zweiten, „teilweise aufgebrochenen“ Zustand hatte sich ein Domänenpaar auseinandergezogen, während das andere intakt blieb, was auf ein Zwischenstadium auf dem Weg zur vollständigen Desensitivierung hindeutet, das noch nicht fest einsperrt.
Versteckte Scharniere, die das Timing feinjustieren
Durch den Vergleich dieser Strukturen mit zuvor gelösten vollständig aktiven und vollständig desensitivierten Kainat-Rezeptoren verfolgten die Autoren, wie Bewegungen in der äußeren Domänenschicht auf die Pore übertragen werden. Sie identifizierten zentrale Kontaktregionen innerhalb und zwischen Domänenpaaren, die als Scharniere und Verstrebungen fungieren, besonders um die beiden GluK5-Untereinheiten, die sich einander gegenüber im Komplex befinden. Subtile Verschiebungen an diesen Stellen veränderten, wie stark die Domänen zusammengehalten werden und wie sie an den Verbindungsstücken ziehen, die die Pore aufziehen. Als die Forscher bestimmte Aminosäuren an diesen Schnittstellen austauschten, konnten sie bewirken, dass der Rezeptor sich schneller oder langsamer deaktiviert und wie leicht er desensitiviert. Das hilft zu erklären, warum GluK5-haltige Rezeptoren insbesondere ungewöhnlich lange aktiv bleiben nach kurzen Glutamatstößen.
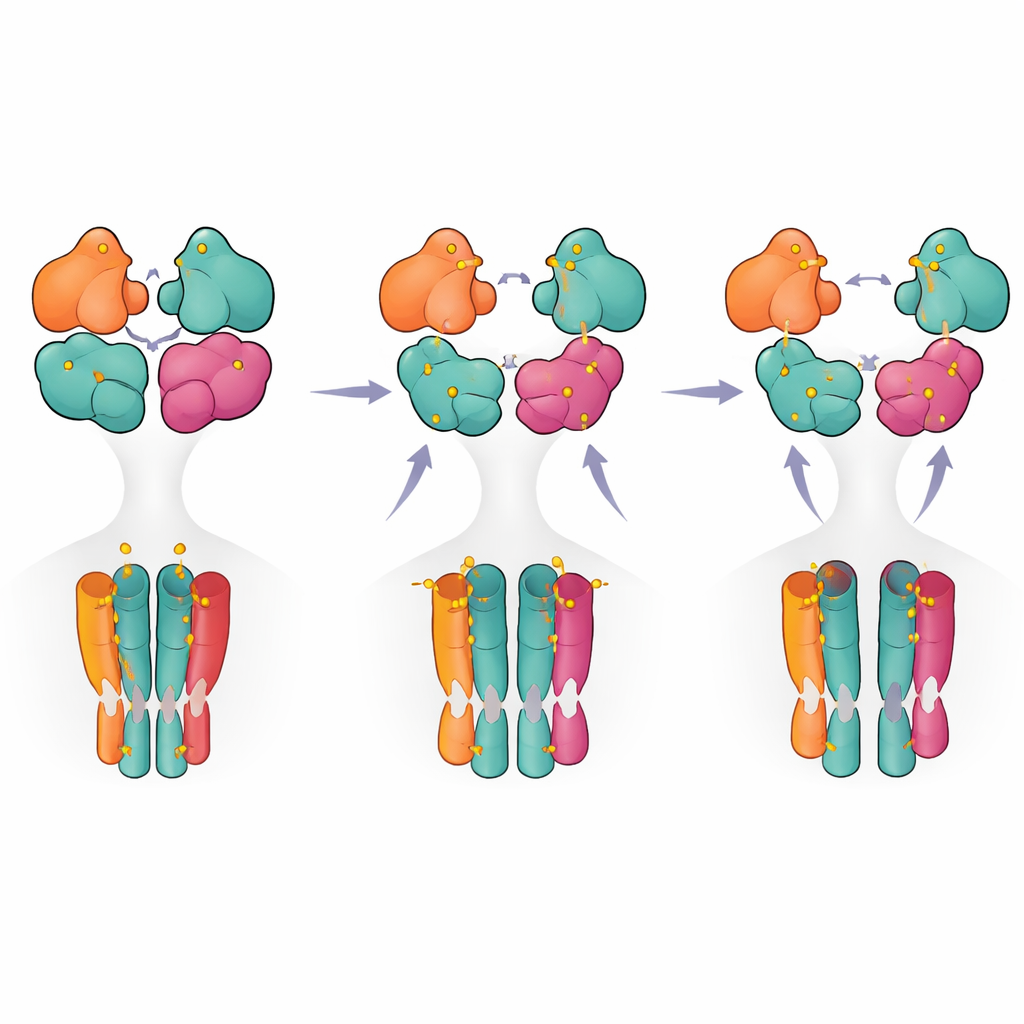
Eine schrittweise Roadmap von Aktivierung bis Abschaltung
Zusammenführend schlagen die Autoren auf Basis der strukturellen Schnappschüsse und funktionellen Messungen ein schrittweises Modell vor, in dem der Rezeptor vom Ruhezustand in einen voraktiven Zustand übergeht, wenn nur zwei Untereinheiten (typischerweise das GluK5-Paar) besetzt sind. Zusätzliche Ligandbindung fördert das partielle Aufbrechen eines Domänenpaares, und erst wenn drei oder vier Untereinheiten besetzt sind, erreicht der Rezeptor eine vollständig aufgebrochene Konfiguration, die mit langanhaltender Desensitivierung verbunden ist. Für Nicht-Spezialisten bedeutet das, dass der Rezeptor sich weniger wie ein einfacher Ein-/Ausschalter verhält und eher wie ein mehrstufiger Dimmer, bei dem unterschiedliche Besetzungsmuster und innere Kontakte die Stärke und Dauer des Signals abstimmen. Diese Erkenntnisse klären nicht nur die grundlegende Funktionsweise eines wichtigen Hirnrezeptors, sondern heben auch strukturelle Hotspots hervor, die künftig von Medikamenten angepeilt werden könnten, um die Aktivität von Kainat-Rezeptoren bei Krankheiten fein zu regulieren.
Zitation: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
Schlüsselwörter: Kainat-Rezeptoren, Glutamatsignalgebung, synaptische Übertragung, cryo-EM-Strukturen, Rezeptor-Desensitivierung