Clear Sky Science · fr
Structures d'hétérotétramères partiellement occupés donnant un aperçu de l'activation et de la désensibilisation des récepteurs aux kainates
Pourquoi de minuscules interrupteurs cérébraux comptent
Les récepteurs aux kainates sont de minuscules interrupteurs protéiques qui permettent aux neurones de communiquer. Ils répondent au neurotransmetteur glutamate et participent à des processus allant de l'apprentissage et la mémoire à la douleur et l'inflammation. Lorsque ces interrupteurs fonctionnent mal, ils ont été associés à des troubles tels que l'épilepsie et des pathologies psychiatriques. Cette étude explore, avec un niveau de détail structural sans précédent, comment un type majeur de récepteur aux kainates s'active puis se « coupe » lorsque seules certaines de ses sous-unités sont occupées par des molécules semblables au glutamate — une situation qui reflète probablement ce qui se passe réellement à de nombreuses synapses.
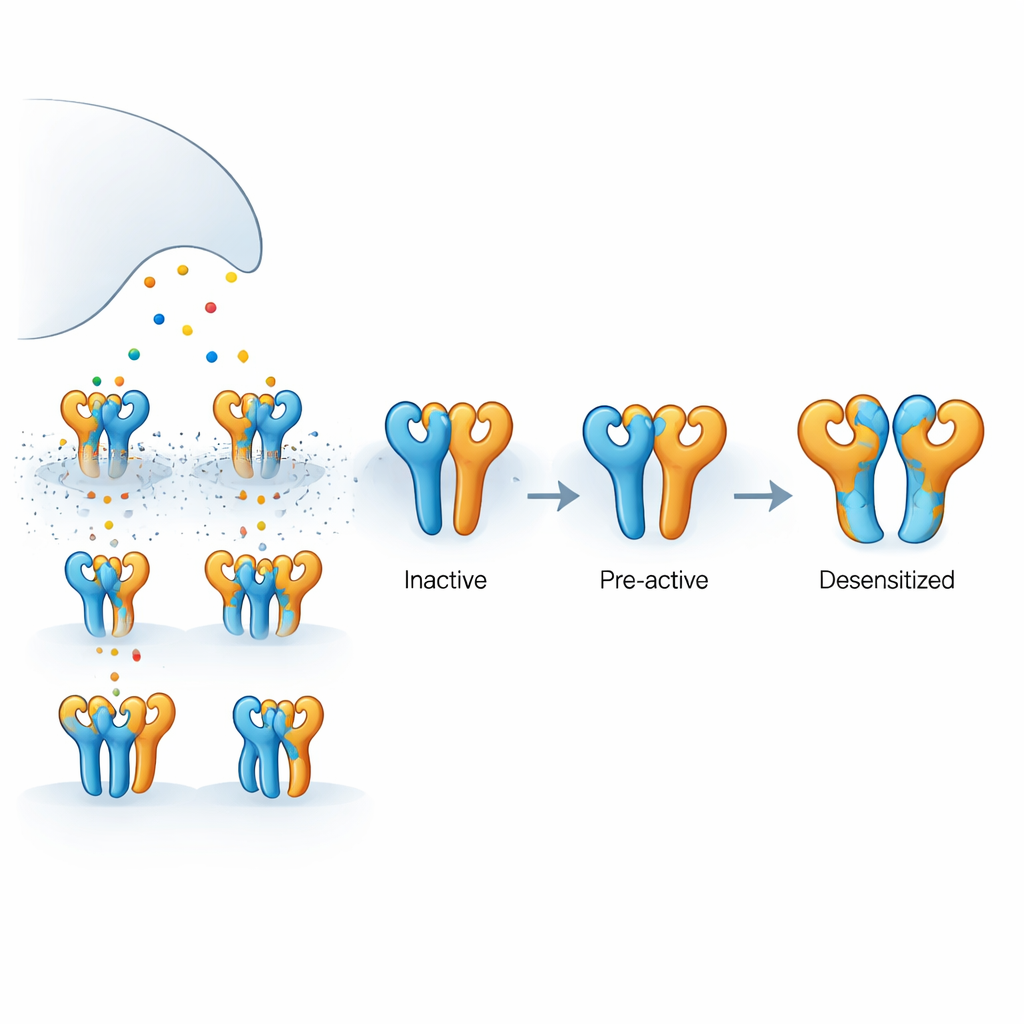
Comment ce récepteur cérébral est construit
Le récepteur étudié ici est un récepteur aux kainates composé de deux types de sous-unités protéiques, appelées GluK2 et GluK5, assemblées en complexe à quatre éléments. GluK5 lie le glutamate de manière particulièrement forte et tend à occuper deux positions spécifiques du tétramère, tandis que GluK2 occupe les deux autres. Chaque sous-unité possède un domaine externe qui capte le glutamate et une région interne formant un pore qui laisse passer les ions, générant des signaux électriques. Parce que le glutamate est libéré brièvement puis rapidement recapté, les quatre sous-unités ne sont pas toujours occupées en même temps. Comprendre ce qui se passe lorsque seules certaines d'entre elles sont liées est essentiel pour expliquer comment les synapses réelles modulent l'intensité et le timing du signal.
Des déclencheurs partiellement enfoncés qui n'enrayent pas
À l'aide d'enregistrements électriques effectués sur des cellules humaines, les auteurs ont montré qu'un médicament sélectif de GluK5, la 5-iodowillardine, provoque un courant stable à travers les récepteurs GluK2/GluK5 sans leur faire subir une « désensibilisation » — la coupure protectrice qui suit habituellement l'activation. En revanche, le neurotransmetteur naturel glutamate active ces mêmes récepteurs puis les fait s'éteindre très rapidement. Un autre composé, l'AMPA, active aussi ces récepteurs mais n'entraîne qu'une désensibilisation partielle. Ces comportements suggèrent que lorsque seules les sous-unités GluK5 sont occupées, le récepteur peut s'ouvrir ou se préparer à s'ouvrir sans basculer dans un état inactif de longue durée, alors qu'une occupation plus étendue pousse le récepteur vers une configuration d'arrêt plus profonde.
Instantanés de pièces en mouvement
Pour voir à quoi ressemblent ces différents états fonctionnels en trois dimensions, l'équipe a utilisé la cryo-microscopie électronique pour capturer des instantanés structuraux sous des conditions de ligands soigneusement contrôlées. En présence de l'agoniste sélectif de GluK5, ils ont observé deux conformations principales. Dans l'une, les quatre domaines de liaison au ligand formaient des paires intactes, avec les unités GluK5 en position fermée autour du ligand et les unités GluK2 restant ouvertes. Cet état « intact » présentait un léger relâchement et une rotation entre les domaines appariés ainsi qu'une expansion mesurable des hélices du pore interne, cohérente avec une configuration pré-active prête à s'ouvrir bien que le canal ionique soit encore fermé. Dans le second état, dit « partiellement rompu », une paire de domaines s'était séparée tandis que l'autre restait intacte, suggérant un intermédiaire sur la voie vers la désensibilisation complète mais pas encore verrouillé.
Charnières cachées qui ajustent le timing
En comparant ces structures avec des récepteurs aux kainates complètement actifs ou complètement désensibilisés résolus précédemment, les auteurs ont retracé comment les mouvements dans la couche de domaines externes sont transmis au pore. Ils ont identifié des régions de contact clés à l'intérieur et entre les paires de domaines qui agissent comme des charnières et des renforts, en particulier autour des deux sous-unités GluK5 qui se trouvent en vis‑à‑vis dans le complexe. De légers déplacements à ces sites modifiaient la force des interactions entre domaines et la manière dont ils tirent sur les liaisons qui ouvrent le pore. Lorsque les chercheurs ont remplacé certains acides aminés à ces interfaces, ils ont pu rendre la désactivation du récepteur plus rapide ou plus lente et modifier sa propension à se désensibiliser. Cela aide à expliquer pourquoi les récepteurs contenant GluK5 restent, en particulier, actifs plus longtemps après de brèves rafales de glutamate.
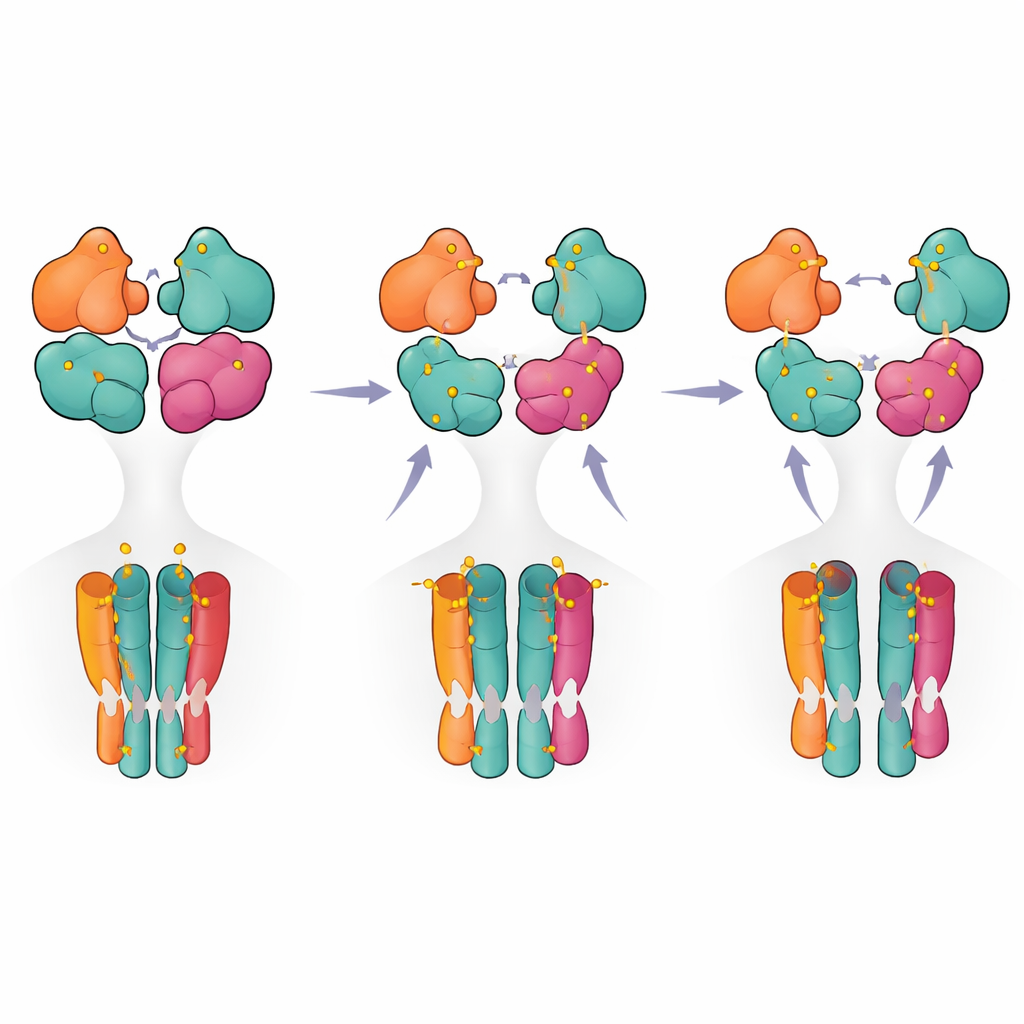
Une feuille de route étape par étape de l'activation à l'arrêt
En rassemblant les instantanés structuraux et les mesures fonctionnelles, les auteurs proposent un modèle étape par étape dans lequel le récepteur passe d'un état de repos à un état pré‑actif lorsque seules deux sous-unités (généralement la paire GluK5) sont occupées. Une liaison de ligand supplémentaire favorise la rupture partielle d'une paire de domaines, et ce n'est que lorsque trois ou quatre sous-unités sont occupées que le récepteur atteint une configuration entièrement rompue associée à une désensibilisation de longue durée. Pour les non-spécialistes, cela signifie que le récepteur se comporte moins comme un simple interrupteur marche/arrêt et davantage comme un variateur à plusieurs étapes, avec différents schémas d'occupation et contacts internes qui réglent l'intensité et la durée du signal. Ces informations clarifient non seulement le fonctionnement de base d'un récepteur cérébral clé, mais mettent aussi en lumière des points structuraux cibles potentiels pour de futurs médicaments visant à ajuster finement l'activité des récepteurs aux kainates dans les maladies.
Citation: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
Mots-clés: récepteurs aux kainates, signalisation glutamatergique, transmission synaptique, structures cryo-EM, désensibilisation des récepteurs