Clear Sky Science · nl
Structuren van gedeeltelijk bezette hetero-tetrameren geven inzicht in activering en desensitisatie van kainaatreceptoren
Waarom kleine schakelaars in de hersenen ertoe doen
Kainaatreceptoren zijn microscopische eiwitschakelaars die helpen dat hersencellen met elkaar communiceren. Ze reageren op de neurotransmitter glutamaat en zijn betrokken bij processen variërend van leren en geheugen tot pijn en ontsteking. Wanneer deze schakelaars slecht functioneren, worden ze in verband gebracht met aandoeningen zoals epilepsie en psychiatrische ziekten. Deze studie onderzoekt, met ongekende structurele fijnmazigheid, hoe één belangrijk type kainaatreceptor aan gaat en vervolgens "zichzelf uitschakelt" wanneer slechts een deel van de subunits bezet is door glutamaat-achtige moleculen — een situatie die waarschijnlijk weerspiegelt wat er in veel echte synapsen gebeurt.
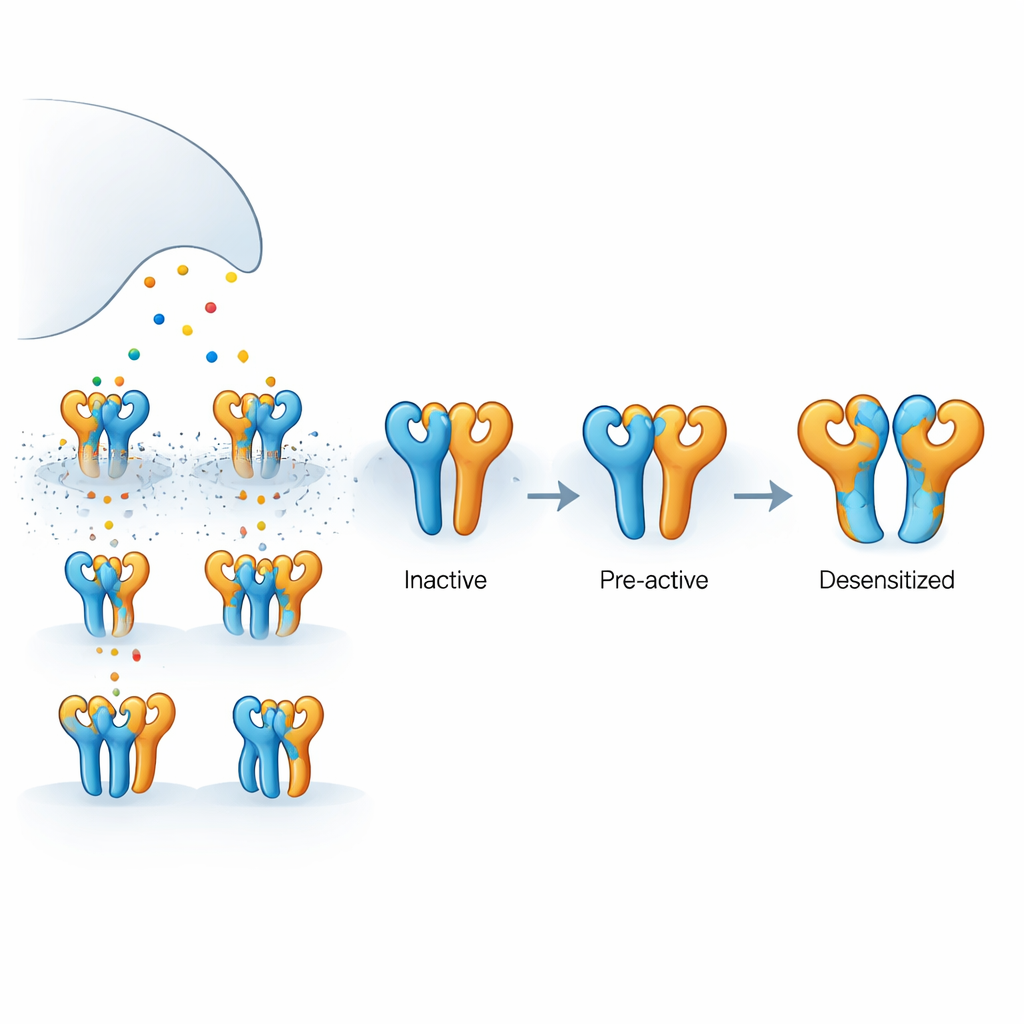
Hoe deze hersenreceptor is opgebouwd
De hier onderzochte receptor is een kainaatreceptor opgebouwd uit twee soorten eiwit-subunits, genaamd GluK2 en GluK5, geassembleerd tot een viervoudig complex. GluK5 bindt glutamaat bijzonder sterk en heeft de neiging twee specifieke posities in het tetramere complex in te nemen, terwijl GluK2 de andere twee bezet. Elke subunit heeft een buitenste domein dat glutamaat opvangt en een binnenste porievormende regio die ionen doorlaat en zo elektrische signalen genereert. Omdat glutamaat kort wordt vrijgegeven en snel wordt verwijderd, zijn niet altijd alle vier subunits tegelijk bezet. Begrijpen wat er gebeurt wanneer slechts sommige subunits bezet zijn, is essentieel om uit te leggen hoe echte synapsen signaalsterkte en -timing moduleren.
Gedeeltelijk ingedrukte triggers die niet blokkeren
Middels elektrische opnames uit menselijke cellen toonden de auteurs aan dat een GluK5-selectief middel, 5-iodowillardiine, een aanhoudende stroom door GluK2/GluK5-receptoren veroorzaakt zonder dat deze "desensitiseren" — de zelfbeschermende uitschakeling die gewoonlijk op activering volgt. Daarentegen zet de natuurlijke transmitter glutamaat dezelfde receptoren aan die vervolgens zeer snel stilvallen. Een ander middel, AMPA, activeert deze receptoren ook, maar veroorzaakt slechts gedeeltelijke desensitisatie. Deze gedragingen suggereren dat wanneer alleen de GluK5-subunits bezet zijn, de receptor kan openen of de opening kan naderen zonder in een langdurige inactieve toestand te vervallen, terwijl uitgebreider bezetten de receptor in een diepere uitschakelingsconfiguratie duwt.
Snelkoppelingen van bewegende delen in actie
Om te zien hoe deze verschillende functionele toestanden er driedimensionaal uitzien, gebruikte het team cryogene elektronenmicroscopie om structurele momentopnamen vast te leggen onder zorgvuldig gecontroleerde ligandcondities. Met de GluK5-selectieve agonist aanwezig observeerden ze twee hoofdkonformaties. In de ene vorm vormden alle vier de ligandbindende domeinen intacte paren, waarbij de GluK5-eenheden om het ligand gesloten waren en de GluK2-eenheden open bleven. Deze "intacte" toestand toonde subtiele lossering en rotatie tussen de gepaarde domeinen en een meetbare uitzetting van de binnenste porieelhelen, consistent met een pre-actieve, klaar-om-te-openen configuratie hoewel het ionenkanaal nog gesloten was. In de tweede, "gedeeltelijk gescheurde" toestand, was één domeinpaar uit elkaar gevallen terwijl het andere intact bleef, wat wijst op een tussenstadium op weg naar volledige desensitisatie maar nog niet vergrendeld.
Verborgen scharnieren die de timing afstellen
Door deze structuren te vergelijken met eerder opgeloste volledig actieve en volledig desensitiseerde kainaatreceptoren, volgden de auteurs hoe bewegingen in de buitenste domeinlaag naar de pore worden overgebracht. Ze identificeerden belangrijke contactzones binnen en tussen domeinparen die als scharnieren en stutten fungeren, vooral rond de twee GluK5-subunits die tegenover elkaar in het complex liggen. Subtiele verschuivingen op deze plaatsen veranderden hoe stevig de domeinen bijeenhouden en hoe sterk ze trekken aan de verbindingsketens die de porie openen. Toen de onderzoekers bepaalde aminozuren op deze interfaces verwisselden, konden ze de receptor sneller of langzamer laten deactiveren en beïnvloeden hoe gemakkelijk deze desensitiseerde. Dit helpt verklaren waarom GluK5-bevattende receptoren, in het bijzonder, ongewoon lang actief blijven na korte glutamaatafwezingen.
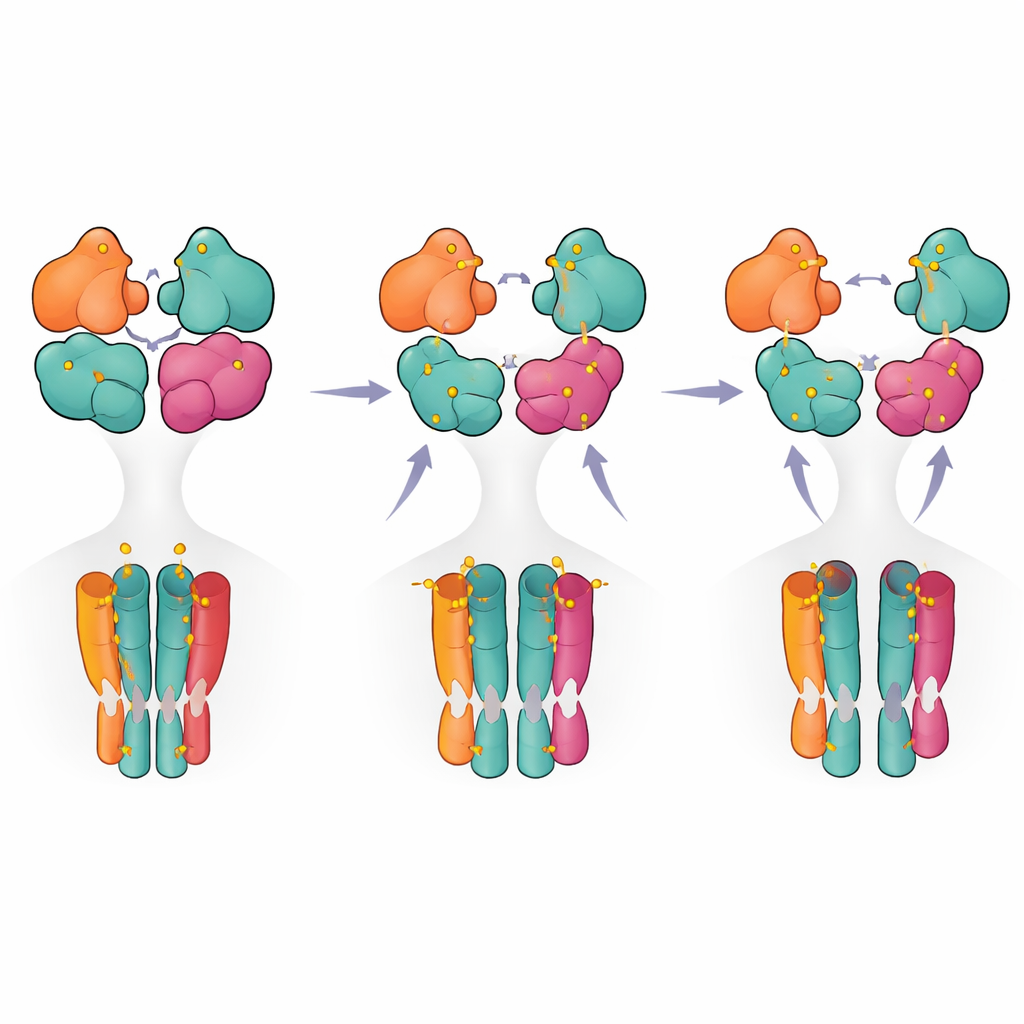
Een stapsgewijze routekaart van activering naar uitschakeling
Door de structurele momentopnamen en functionele metingen te combineren, stellen de auteurs een stapsgewijs model voor waarin de receptor beweegt van een rusttoestand naar een pre-actieve staat wanneer slechts twee subunits (meestal het GluK5-paar) bezet zijn. Additionele ligandbinding bevordert de gedeeltelijke ruptuur van één domeinpaar, en pas wanneer drie of vier subunits bezet zijn bereikt de receptor een volledig gescheurde configuratie die geassocieerd is met langdurige desensitisatie. Voor niet-specialisten betekent dit dat de receptor zich minder gedraagt als een eenvoudige aan/uit-schakelaar en meer als een meertraps dimmer, waarbij verschillende bezettingspatronen en interne contacten bepalen hoe krachtig en hoe lang het signaal is. Deze inzichten verduidelijken niet alleen het basiswerkingsmechanisme van een belangrijke hersenreceptor, maar benadrukken ook structurele hotspots die in toekomstige geneesmiddelontwikkeling gericht kunnen worden om de activiteit van kainaatreceptoren bij ziekte fijn af te stemmen.
Bronvermelding: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
Trefwoorden: kainaatreceptoren, glutamaat-signalering, synaptische transmissie, cryo-EM-structuren, receptor-desensitisatie