Clear Sky Science · es
Estructuras de heterotetrámeros parcialmente ocupados ofrecen información sobre la activación y desensibilización de los receptores kainato
Por qué importan estos pequeños interruptores cerebrales
Los receptores kainato son diminutos interruptores proteicos que ayudan a las neuronas a comunicarse. Responden al neurotransmisor glutamato y participan en procesos que van desde el aprendizaje y la memoria hasta el dolor y la inflamación. Cuando estos interruptores funcionan mal, se los ha asociado con trastornos como la epilepsia y enfermedades psiquiátricas. Este estudio explora, con un detalle estructural sin precedentes, cómo un tipo principal de receptor kainato se activa y después "se apaga" cuando solo algunos de sus subunidades están ocupados por moléculas similares al glutamato —una situación que probablemente refleja lo que ocurre realmente en muchas sinapsis.
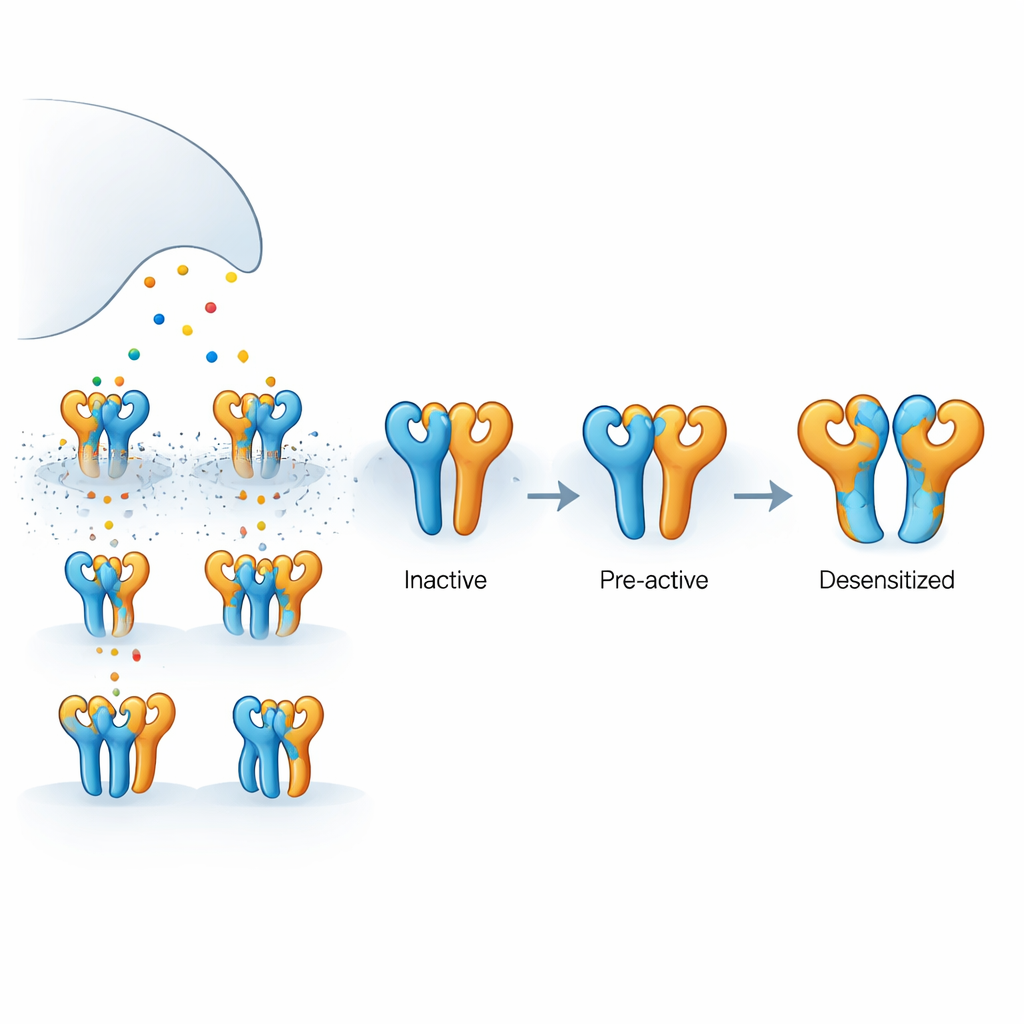
Cómo está construido este receptor cerebral
El receptor examinado aquí es un receptor kainato formado por dos tipos de subunidades proteicas, llamadas GluK2 y GluK5, ensambladas en un complejo de cuatro partes. GluK5 une el glutamato de forma especialmente fuerte y tiende a ocupar dos posiciones específicas en el tetrámero, mientras que GluK2 ocupa las otras dos. Cada subunidad tiene un dominio externo que capta el glutamato y una región interna que forma el poro y permite el flujo de iones, generando señales eléctricas. Dado que el glutamato se libera de forma breve y se elimina rápidamente, no siempre las cuatro subunidades están ocupadas al mismo tiempo. Entender qué sucede cuando solo algunas lo están es clave para explicar cómo las sinapsis reales modulan la intensidad y el tiempo de la señal.
Disparadores parcialmente apretados que no encallan
Mediante registros eléctricos en células humanas, los autores mostraron que un fármaco selectivo para GluK5, la 5-iodowillardina, provoca una corriente sostenida a través de receptores GluK2/GluK5 sin inducir su "desensibilización" —el cierre autoprotectivo que suele seguir a la activación. En contraste, el transmisor natural glutamato activa esos mismos receptores y luego provoca que queden silenciosos muy rápidamente. Otro fármaco, el AMPA, también activa estos receptores pero produce solo una desensibilización parcial. Estos comportamientos sugieren que cuando únicamente las subunidades GluK5 están ocupadas, el receptor puede abrirse o acercarse a la apertura sin caer en un estado inactivo de larga duración, mientras que una unión más extensa empuja al receptor hacia una configuración de cierre más profunda.
Instantáneas de piezas en movimiento
Para ver cómo lucen en tres dimensiones estos diferentes estados funcionales, el equipo usó microscopía crioelectrónica para capturar instantáneas estructurales bajo condiciones controladas de ligando. Con el agonista selectivo de GluK5 presente, observaron dos conformaciones principales. En una, los cuatro dominios de unión al ligando formaban pares intactos, con las unidades GluK5 cerradas alrededor del ligando y las unidades GluK2 permaneciendo abiertas. Este estado "intacto" mostraba un aflojamiento y rotación sutil entre los dominios emparejados y una expansión medible de las hélices del poro interno, coherente con una configuración preactiva, lista para abrirse aunque el canal iónico aún estuviera cerrado. En la segunda, estado "parcialmente fracturado", un par de dominios se había separado mientras el otro permanecía intacto, lo que sugiere un intermedio en el camino hacia la desensibilización completa pero aún no bloqueado.
Bisagras ocultas que afinan el tiempo
Al comparar estas estructuras con receptores kainato previamente resueltos en estados totalmente activos y totalmente desensibilizados, los autores trazaron cómo los movimientos en la capa de dominios externos se transmiten al poro. Identificaron regiones de contacto clave dentro y entre pares de dominios que actúan como bisagras y refuerzos, especialmente alrededor de las dos subunidades GluK5 que se sitúan enfrentadas en el complejo. Desplazamientos sutiles en estos sitios cambiaron la fuerza con la que los dominios se mantienen unidos y cómo tiran de los conectores que abren el poro. Cuando los investigadores intercambiaron ciertos aminoácidos en estas interfaces, pudieron hacer que el receptor se inactivara más rápido o más lento y alterar con qué facilidad se desensibilizaba. Esto ayuda a explicar por qué los receptores que contienen GluK5, en particular, permanecen activos inusualmente tiempo tras breves estallidos de glutamato.
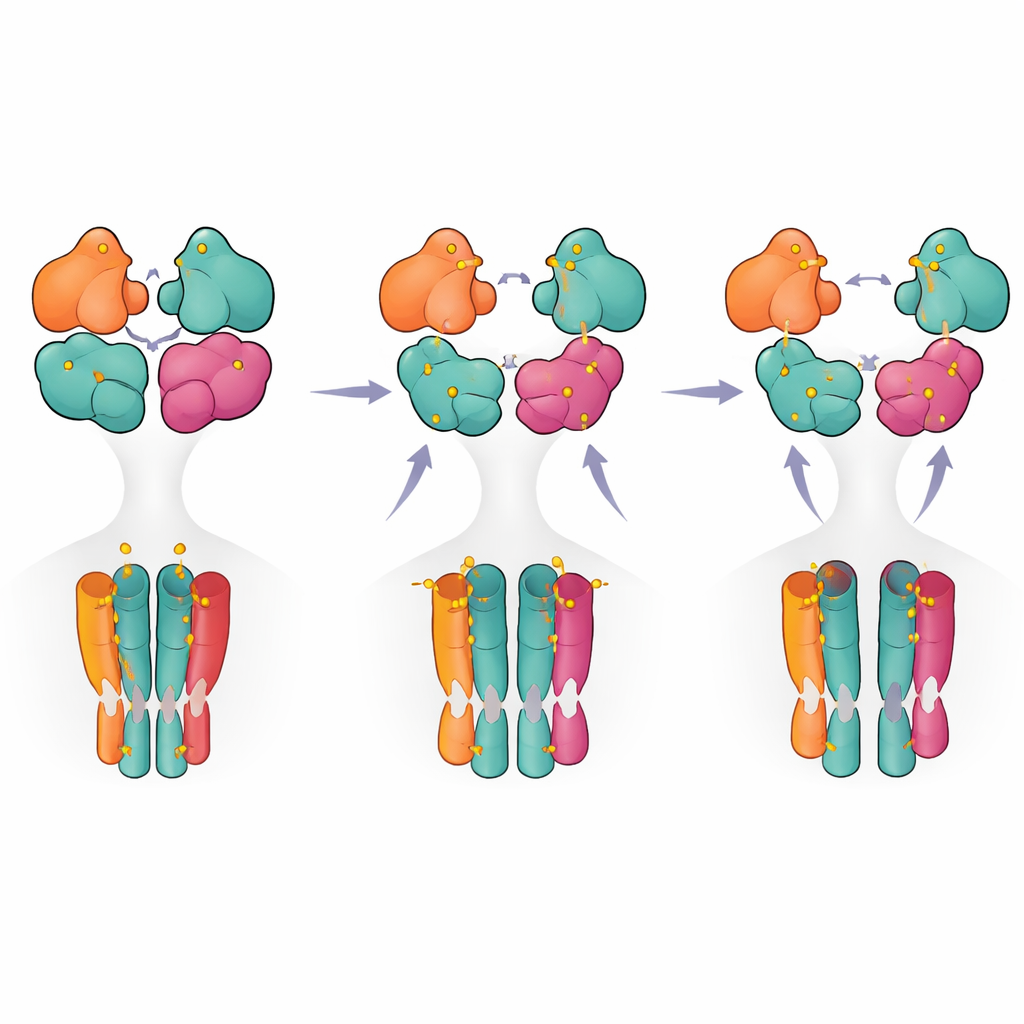
Una hoja de ruta escalonada desde la activación hasta el apagado
Poniendo juntas las instantáneas estructurales y las medidas funcionales, los autores proponen un modelo escalonado en el que el receptor pasa de un estado de reposo a un estado preactivo cuando solo dos subunidades (normalmente el par GluK5) están ocupadas. La unión adicional de ligando promueve la ruptura parcial de un par de dominios, y solo cuando tres o cuatro subunidades están ocupadas el receptor alcanza una configuración totalmente fracturada asociada con desensibilización de larga duración. Para los no especialistas, esto significa que el receptor se comporta menos como un simple interruptor de encendido/apagado y más como un atenuador de varios pasos, con distintos patrones de ocupación y contactos internos que afinan la intensidad y la duración de la señal. Estos conocimientos no solo aclaran el funcionamiento básico de un receptor cerebral clave, sino que también destacan puntos estructurales que podrían ser objetivo de futuros fármacos destinados a ajustar la actividad de los receptores kainato en enfermedades.
Cita: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
Palabras clave: receptores kainato, señalización por glutamato, transmisión sináptica, estructuras por crio-ME, desensibilización del receptor