Clear Sky Science · pt
Estruturas de hetero-tetâmeros parcialmente ocupados oferecem visão sobre ativação e dessensibilização de receptores de kainato
Por que pequenos interruptores cerebrais importam
Receptores de kainato são interruptores proteicos microscópicos que ajudam as células cerebrais a se comunicarem. Eles respondem ao neurotransmissor glutamato e participam de processos que vão desde aprendizagem e memória até dor e inflamação. Quando esses interruptores falham, já foram associados a distúrbios como epilepsia e doenças psiquiátricas. Este estudo explora, com detalhe estrutural sem precedentes, como um tipo principal de receptor de kainato é ativado e depois “desliga-se” quando apenas alguns de seus subunidades estão ligados por moléculas semelhantes ao glutamato — uma situação que provavelmente reflete o que realmente acontece em muitas sinapses.
Como este receptor cerebral é construído
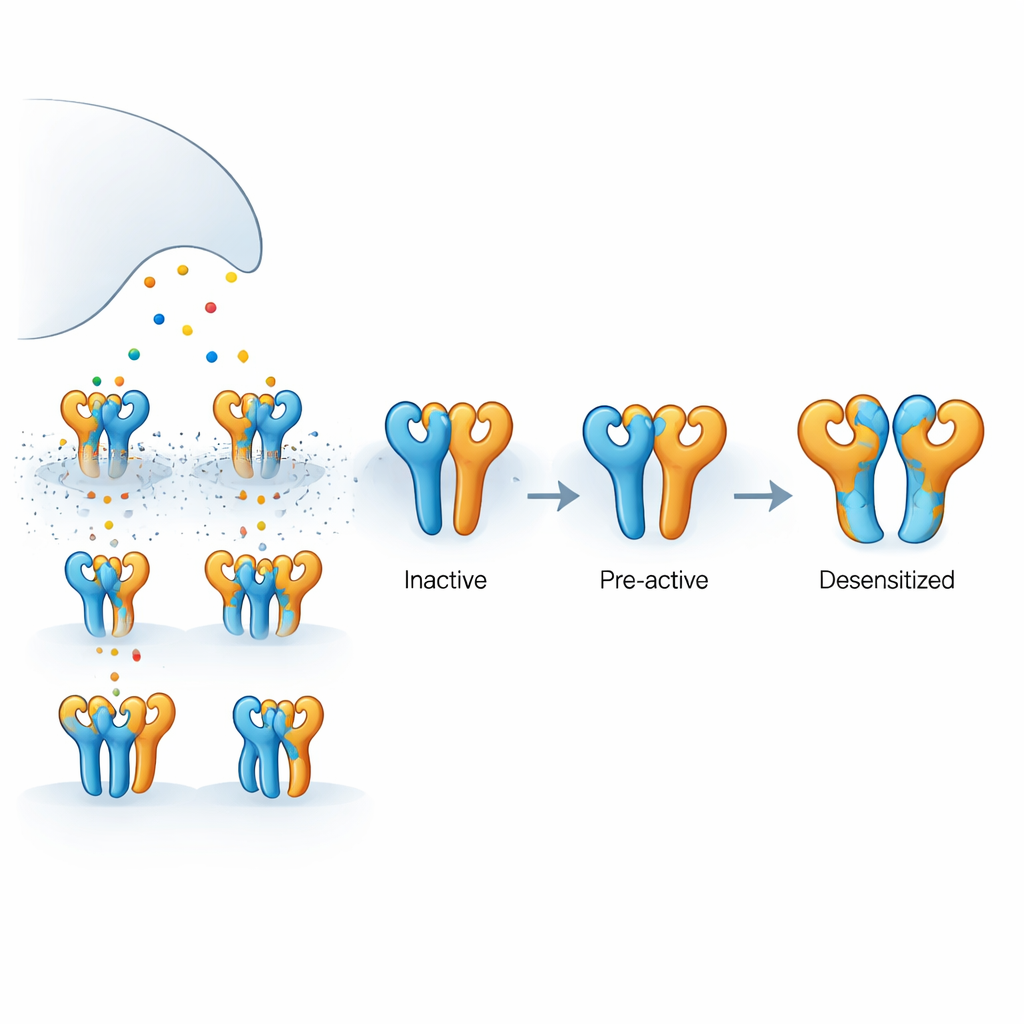
O receptor examinado aqui é um receptor de kainato formado por dois tipos de subunidades proteicas, chamadas GluK2 e GluK5, montadas em um complexo de quatro partes. GluK5 liga-se ao glutamato com afinidade especialmente alta e tende a ocupar duas posições específicas no tetrâmero, enquanto GluK2 ocupa as outras duas. Cada subunidade tem um domínio externo que captura o glutamato e uma região interna que forma o poro e permite o fluxo de íons, gerando sinais elétricos. Como o glutamato é liberado brevemente e rapidamente captado, nem sempre as quatro subunidades estão ocupadas ao mesmo tempo. Entender o que acontece quando apenas algumas estão ligadas é fundamental para explicar como sinapses reais modulam a intensidade e o tempo dos sinais.
Gatilhos parcialmente pressionados que não emperram
Usando registros elétricos em células humanas, os autores mostraram que um fármaco seletivo para GluK5, o 5-iodowillardina, gera uma corrente estável através de receptores GluK2/GluK5 sem provocar sua “dessensibilização” — o desligamento autorregulatório que normalmente segue a ativação. Em contraste, o transmissor natural glutamato faz com que esses mesmos receptores liguem-se e logo em seguida se tornem silenciosos. Outro agonista, AMPA, também ativa esses receptores, mas produz apenas dessensibilização parcial. Esses comportamentos sugerem que, quando apenas as subunidades GluK5 estão ocupadas, o receptor pode abrir ou se aproximar da abertura sem entrar em um estado inativo de longa duração, enquanto uma ligação mais ampla empurra o receptor para uma configuração de desligamento mais profunda.
Instantâneos de peças em movimento em ação
Para ver como esses estados funcionais distintos se apresentam em três dimensões, a equipe utilizou microscopia eletrônica crio (crio-EM) para capturar instantâneos estruturais sob condições de ligante cuidadosamente controladas. Na presença do agonista seletivo para GluK5, observaram duas conformações principais. Em uma delas, os quatro domínios de ligação ao ligante formaram pares intactos, com as unidades GluK5 fechadas ao redor do ligante e as unidades GluK2 permanecendo abertas. Esse estado “intacto” mostrou um afrouxamento e rotação sutis entre os domínios pareados e uma expansão mensurável das hélices do poro interno, consistente com uma configuração pré-ativa, pronta para abrir, embora o canal iônico ainda estivesse fechado. Na segunda conformação, “parcialmente rompida”, um par de domínios havia se separado enquanto o outro permanecia intacto, sugerindo um intermediário no caminho rumo à dessensibilização completa, mas ainda não travado nessa configuração.
Dobradiças ocultas que afinam o tempo
Ao comparar essas estruturas com receptores de kainato previamente resolvidos em estados totalmente ativos e totalmente dessensibilizados, os autores traçaram como movimentos na camada de domínios externos são transmitidos ao poro. Identificaram regiões de contato-chave tanto dentro quanto entre pares de domínios que atuam como dobradiças e escoras, especialmente ao redor das duas subunidades GluK5 que se opõem no complexo. Mudanças sutis nesses sítios alteraram a força com que os domínios se mantêm unidos e como eles puxam os conectores que abrem o poro. Quando os pesquisadores substituíram certos aminoácidos nessas interfaces, foram capazes de fazer o receptor desativar mais rápido ou mais devagar e alterar sua tendência à dessensibilização. Isso ajuda a explicar por que receptores contendo GluK5, em particular, permanecem ativos por tempo incomumente longo após rajadas breves de glutamato.
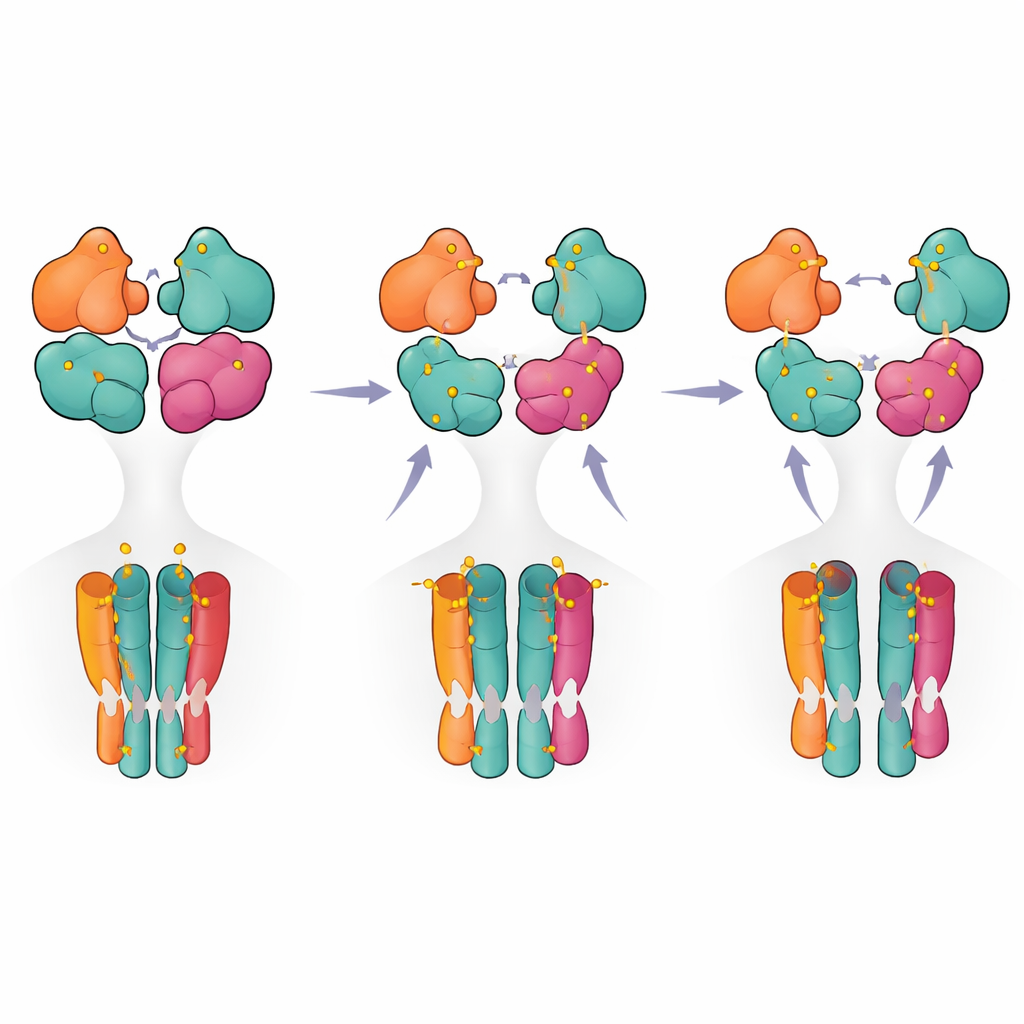
Um roteiro em etapas da ativação ao desligamento
Ao reunir os instantâneos estruturais e as medições funcionais, os autores propõem um modelo em etapas no qual o receptor passa de um estado de repouso para um estado pré-ativo quando apenas duas subunidades (tipicamente o par GluK5) estão ocupadas. A ligação adicional de ligante promove a ruptura parcial de um par de domínios, e somente quando três ou quatro subunidades estão ocupadas o receptor atinge uma configuração totalmente rompida associada a dessensibilização de longa duração. Para não especialistas, isso significa que o receptor se comporta menos como um simples interruptor liga/desliga e mais como um dimmer com vários passos, com diferentes padrões de ocupação e contatos internos modulando a intensidade e a duração do sinal. Esses insights não só esclarecem o funcionamento básico de um receptor cerebral-chave, como também destacam pontos estruturais que poderiam ser alvos de futuros fármacos destinados a ajustar finamente a atividade de receptores de kainato em doenças.
Citação: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
Palavras-chave: receptores de kainato, sinalização por glutamato, transmissão sináptica, estruturas por crio-ME, dessensibilização de receptores