Clear Sky Science · sv
Strukturer av delvis ockuperade hetero-tetramerer ger insikt i aktivering och desensitisering av kainatreceptorer
Varför små hjärnbrytare betyder något
Kainatreceptorer är mikroskopiska proteinknappar som hjälper hjärnceller att kommunicera. De reagerar på neurotransmittorn glutamat och är involverade i processer som sträcker sig från inlärning och minne till smärta och inflammation. När dessa brytare inte fungerar som de ska har de kopplats till störningar såsom epilepsi och psykiatriska sjukdomar. Denna studie undersöker, med en aldrig tidigare skådad strukturell detaljrikedom, hur en huvudtyp av kainatreceptor slås på och sedan ”stänger av sig själv” när endast några av dess subenheter binder glutamatliknande molekyler — en situation som sannolikt speglar vad som faktiskt händer vid många verkliga synapser.
Hur denna hjärnreceptor är uppbyggd
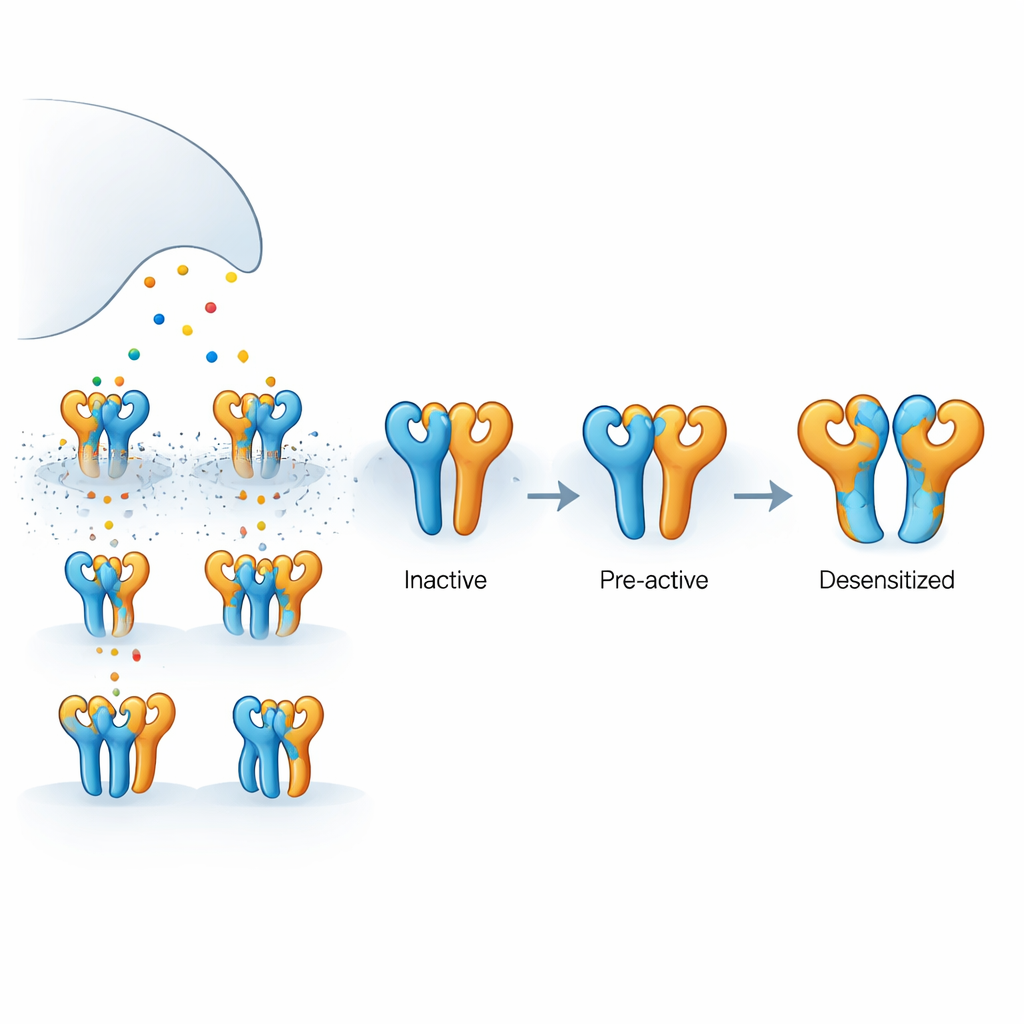
Receptorn som undersöktes här är en kainatreceptor sammansatt av två slags proteinenheter, kallade GluK2 och GluK5, som bildar ett fyrdelat komplex. GluK5 binder glutamat särskilt hårt och tenderar att inta två specifika positioner i tetrameren, medan GluK2 upptar de andra två. Varje subenhet har en yttre domän som fångar glutamat och en inre porbildande region som tillåter joner att flöda och generera elektriska signaler. Eftersom glutamat frisätts kortvarigt och snabbt tas upp är inte alltid alla fyra subenheter ockuperade samtidigt. Att förstå vad som händer när endast några av dem är bundna är avgörande för att förklara hur verkliga synapser reglerar signalstyrka och timing.
Delvis nedtryckta avtryckare som inte fastnar
Genom elektriska inspelningar från humana celler visade författarna att ett GluK5-selektivt läkemedel, 5-jodwillardiin, driver en stabil ström genom GluK2/GluK5-receptorer utan att få dem att ”desensitisera” — den självskyddande avstängning som vanligtvis följer aktivering. I kontrast får den naturliga transmittorn glutamat samma receptorer att slå på och sedan mycket snabbt bli tysta. Ett annat läkemedel, AMPA, aktiverar också dessa receptorer men ger endast partiell desensitisering. Dessa beteenden tyder på att när endast GluK5-subenheterna är ockuperade kan receptorn öppnas eller närma sig öppning utan att falla in i ett långvarigt inaktivt tillstånd, medan mer utbredd bindning pressar receptorn in i en djupare avstängningskonfiguration.
Ögonblicksbilder av rörliga delar i arbete
För att se hur dessa olika funktionella tillstånd ser ut i tre dimensioner använde teamet kryogen elektronmikroskopi för att fånga strukturella ögonblicksbilder under noggrant kontrollerade ligandförhållanden. Med den GluK5-selektiva agonisten närvarande observerade de två huvudsakliga konformationer. I den ena bildade alla fyra ligandbindande domäner intakta par, där GluK5-enheterna var stängda runt liganden medan GluK2-enheterna förblev öppna. Detta ”intakta” tillstånd visade subtil uppluckring och rotation mellan de parade domänerna samt en mätbar expansion av de inre pore-helixernas avstånd, förenlig med en pre-aktiv, redo-att-öppna-konfiguration även om jonkanalen fortfarande var stängd. I det andra, ”delvis brustna” tillståndet hade ett par domäner splittrats medan det andra förblev intakt, vilket tyder på ett mellanläge på vägen mot full desensitisering men ännu inte låst i den.
Dolda gångjärn som finjusterar tidpunkten
Genom att jämföra dessa strukturer med tidigare lösta fullt aktiva och fullt desensitiserade kainatreceptorer följde författarna hur rörelser i det yttre domänlagret överförs till poren. De identifierade viktiga kontaktregioner både inom och mellan domänpar som fungerar som gångjärn och stag, särskilt runt de två GluK5-subenheterna som sitter mittemot varandra i komplexet. Subtila skift vid dessa platser ändrade hur starkt domänerna höll ihop och hur de drog i länkarna som öppnar poren. När forskarna bytte vissa aminosyror vid dessa gränssnitt kunde de göra så att receptorn deaktiverade snabbare eller långsammare och ändrade hur lätt den desensitiserades. Detta hjälper till att förklara varför GluK5-innehållande receptorer, i synnerhet, förblir aktiva ovanligt länge efter korta glutamatskutt.
En stegvis färdplan från aktivering till avstängning
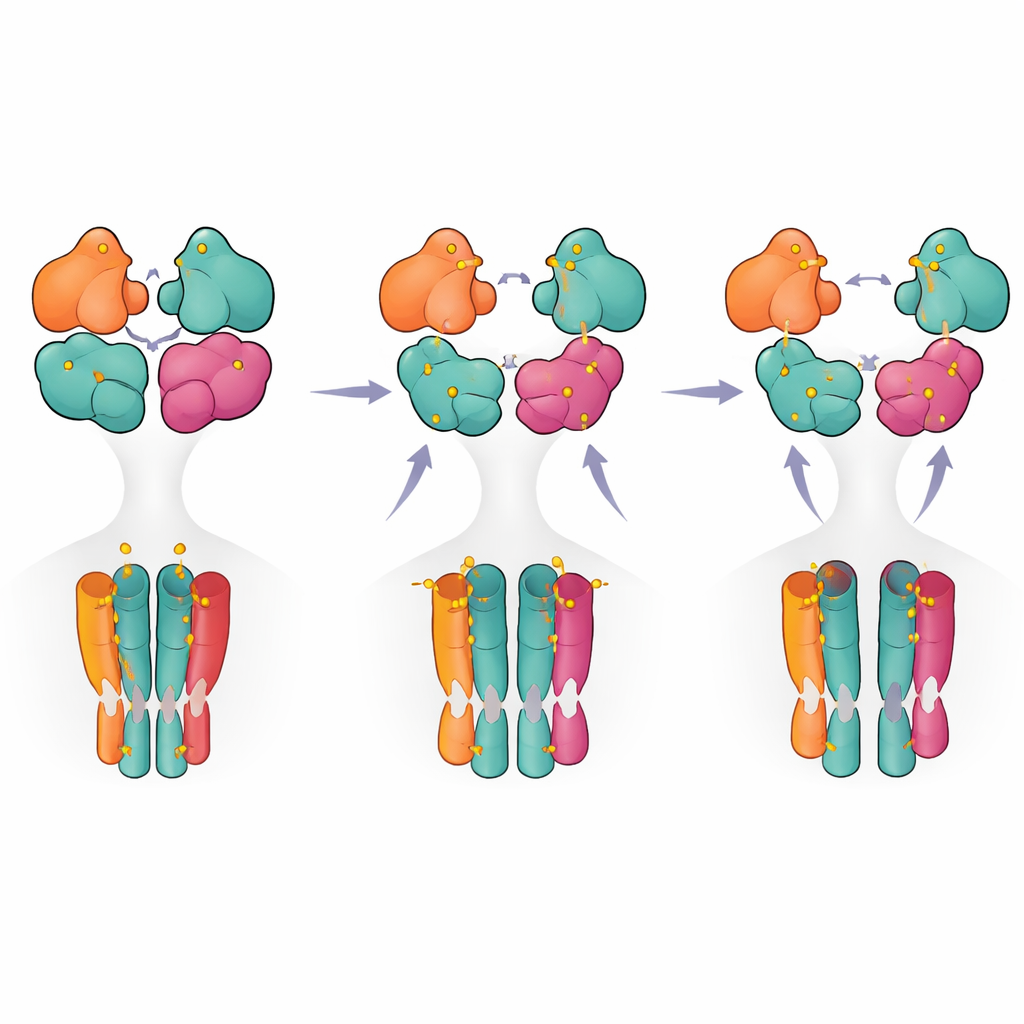
Genom att sammanföra de strukturella ögonblicksbilderna och de funktionella mätningarna föreslår författarna en stegvis modell där receptorn rör sig från ett vilotillstånd till ett pre-aktivt tillstånd när endast två subenheter (vanligen GluK5-paret) är ockuperade. Ytterligare ligandbindning främjar delvis ruptur av ett domänpar, och först när tre eller fyra subenheter är ockuperade når receptorn en fullt brustet konfiguration som är förknippad med långvarig desensitisering. För icke-specialister innebär detta att receptorn beter sig mindre som en enkel på–av-strömbrytare och mer som en flerstegs-dimmer, där olika ockupationsmönster och interna kontakter ställer in hur starkt och hur länge den signalerar. Dessa insikter klargör inte bara grundläggande funktioner hos en nyckelreceptor i hjärnan utan lyfter också fram strukturella hotspotar som skulle kunna riktas med framtida läkemedel för att finjustera kainatreceptoraktivitet vid sjukdom.
Citering: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
Nyckelord: kainatreceptorer, glutamatsignalering, synaptisk transmission, kryo-EM-strukturer, receptordesensitisering