Clear Sky Science · ru
Структуры частично занятых гетеро-тетрамеров дают представление об активации и десенситизации каинадных рецепторов
Почему важны крошечные мозговые переключатели
Каинадные рецепторы — это микроскопические белковые переключатели, которые помогают нейронам обмениваться сигналами. Они реагируют на нейротрансмиттер глутамат и участвуют в процессах от обучения и памяти до боли и воспаления. Нарушения работы этих переключателей связывают с такими расстройствами, как эпилепсия и психические заболевания. В этом исследовании в беспрецедентных деталях показано, как один из основных типов каинадных рецепторов включается, а затем «выключает себя», когда только некоторые его субъединицы связаны с молекулами, похожими на глутамат — ситуация, которая, вероятно, отражает то, что происходит в реальных синапсах.
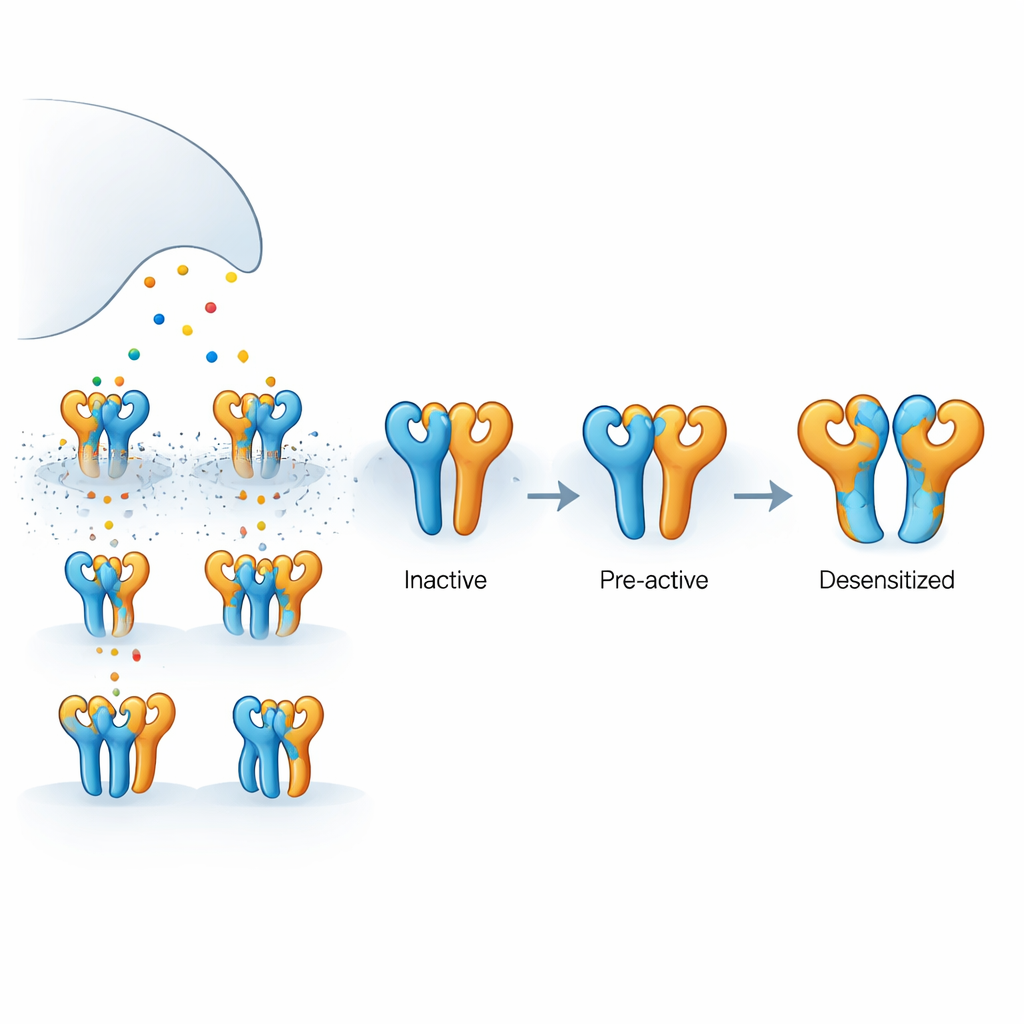
Как устроен этот мозговой рецептор
Исследуемый рецептор — каинадный рецептор, собранный из двух типов белковых субъединиц, называемых GluK2 и GluK5, в четырехзвенную комплексную структуру. GluK5 связывает глутамат особенно прочно и, как правило, занимает два определённых положения в тетрамере, тогда как GluK2 размещается в оставшихся двух. Каждая субъединица имеет наружный домен, улавливающий глутамат, и внутреннюю порообразующую часть, через которую проходят ионы, формируя электрические сигналы. Поскольку глутамат высвобождается кратковременно и быстро захватывается, не все четыре субъединицы всегда заняты одновременно. Понимание того, что происходит, когда связаны лишь некоторые из них, ключ к объяснению того, как реальные синапсы регулируют силу и временные характеристики сигнала.
Частично нажатые триггеры, которые не заклинивают
С помощью электрических записей из человеческих клеток авторы показали, что селективный для GluK5 агонист 5-йодовиллaридин вызывает устойчивый ток через рецепторы GluK2/GluK5, не приводя к их «десенситизации» — самозащитному отключению, которое обычно следует за активацией. Напротив, природный трансмиттер глутамат вызывает включение тех же рецепторов, за которым очень быстро следует молчание. Другой препарат, AMPA, также активирует эти рецепторы, но вызывает только частичную десенситизацию. Такое поведение указывает на то, что при занятии только субъединиц GluK5 рецептор может открываться или приближаться к открытию, не переходя в долгое неактивное состояние, тогда как более широкое связывание толкает рецептор в более глубокую конфигурацию выключения.
Снимки движущихся частей в действии
Чтобы увидеть, как эти различные функциональные состояния выглядят в трех измерениях, команда использовала криогенную электронную микроскопию, делая структурные «снимки» при строго контролируемых условиях лиганда. В присутствии селективного агониста GluK5 они наблюдали две основные конформации. В одной все четыре домена связывания лиганда образовывали целые пары: субъединицы GluK5 были закрыты вокруг лиганда, а GluK2 оставались открытыми. Это «целое» состояние демонстрировало тонкое ослабление и поворот между спаренными доменами и измеримое расширение внутренних спиралей поры, что согласуется с предактивной, готовой к открытию конфигурацией, хотя ионный канал оставался закрыт. Во втором, «частично разорванном» состоянии одна пара доменов разделилась, в то время как другая осталась целой, что указывает на промежуточное состояние на пути к полной десенситизации, но ещё не зафиксированное в ней.
Скрытые шарниры, которые настраивают время
Сравнивая эти структуры с ранее решёнными полностью активными и полностью десенситизированными каинадными рецепторами, авторы проследили, как движения в наружном слое доменов передаются к поре. Они выявили ключевые контактные области как внутри пар доменов, так и между ними, действующие как шарниры и распорки, особенно вокруг двух субъединиц GluK5, стоящих напротив друг друга в комплексе. Тонкие сдвиги в этих местах меняли прочность сцепления доменов и то, как они тянут за связки, открывающие пору. Когда исследователи заменяли определённые аминокислоты на этих интерфейсах, они могли ускорять или замедлять деактивацию рецептора и изменять его склонность к десенситизации. Это помогает объяснить, почему рецепторы, содержащие GluK5, в частности, остаются активными необычно долго после кратких всплесков глутамата.
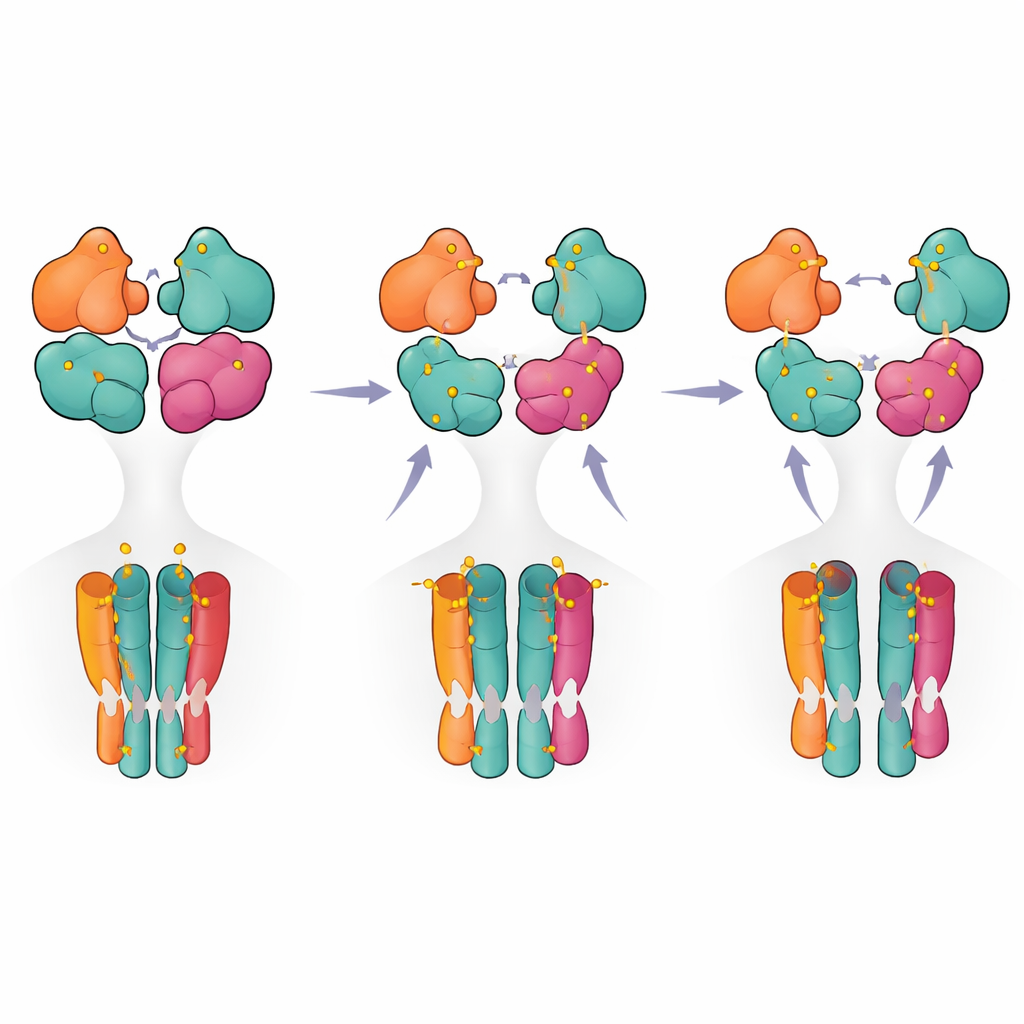
Пошаговая дорожная карта от активации к отключению
Объединив структурные снимки и функциональные измерения, авторы предлагают пошаговую модель, в которой рецептор переходит от состояния покоя к предактивному состоянию, когда заняты только две субъединицы (обычно пара GluK5). Дополнительное связывание лиганда способствует частичному разрыву одной пары доменов, и только при занятии трёх или четырёх субъединиц рецептор достигает полностью разорванной конфигурации, связанной с длительной десенситизацией. Для неспециалистов это означает, что рецептор ведёт себя не как простой выключатель «вкл/выкл», а скорее как многоступенчатый диммер: разные схемы занятости и внутренние контакты регулируют силу и продолжительность сигнала. Эти результаты не только проясняют базовые механизмы ключевого мозгового рецептора, но и выделяют структурные «горячие точки», которые могут стать мишенями для будущих препаратов, направленных на тонкую настройку активности каинадных рецепторов при заболеваниях.
Цитирование: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
Ключевые слова: каинадные рецепторы, глутаматная сигнализация, синаптическая передача, структуры крио-ЭМ, десенситизация рецепторов