Clear Sky Science · tr
Kısmen dolu hetero-tetramer yapılandırmaları kainat reseptör aktivasyonu ve desensitizasyonu hakkında içgörü sağlar
Neden küçük beyin anahtarları önemli?
Kainat reseptörleri, beyin hücrelerinin birbirleriyle iletişim kurmasına yardımcı olan mikroskobik protein anahtarlarıdır. Nörotransmitter glutamata yanıt verirler ve öğrenme ve hafızadan ağrı ve iltihaba kadar geniş bir yelpazedeki süreçlerde rol oynarlar. Bu anahtarlar arızalandığında epilepsi ve psikiyatrik hastalıklar gibi bozukluklarla ilişkilendirilmiştir. Bu çalışma, bir kainat reseptör türünün yalnızca bazı alt birimleri glutamat-benzeri moleküller tarafından bağlandığında nasıl açıldığı ve ardından kendini nasıl “kapatmaya” geçtiğini eşi benzeri görülmemiş yapısal ayrıntıyla inceliyor — bu durum birçok gerçek sinapsta gerçekte olanı muhtemelen yansıtır.
Bu beyin reseptörü nasıl inşa edilmiş?
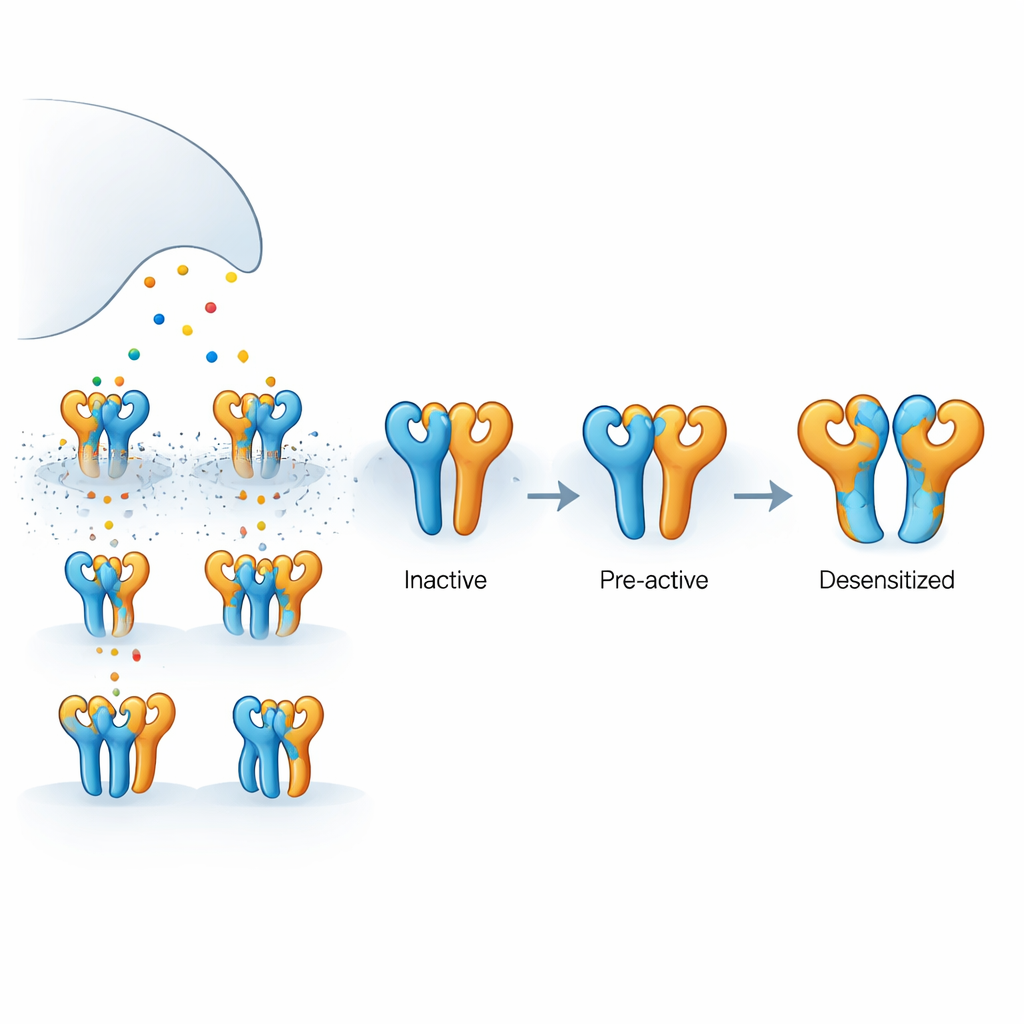
Burada incelenen reseptör, GluK2 ve GluK5 adı verilen iki tip protein alt biriminden oluşan ve dört parçalı bir kompleks halinde bir araya gelen bir kainat reseptörüdür. GluK5 glutamati özellikle sıkı bağlar ve tetramerin iki belirli konumunu işgal etme eğilimindedir; GluK2 ise diğer iki konumu doldurur. Her alt birimde glutamatı yakalayan dış bir yapı ve iyon akışına izin vererek elektrik sinyalleri üreten iç bir gözenek oluşturan bölge bulunur. Glutamat kısa süreli salındığı ve hızla uzaklaştırıldığı için her zaman dört alt birimin hepsi aynı anda dolu olmaz. Yalnızca bazı alt birimler bağlandığında ne olduğunun anlaşılması, gerçek sinapsların sinyal gücünü ve zamanlamasını nasıl düzenlediğini açıklamak için anahtardır.
Tamponlanmış tetikleyiciler ama takılmayan mekanizma
İnsan hücrelerinden yapılan elektriksel kayıtlar kullanılarak, yazarlar GluK5-seçici bir ilaç olan 5-iyodovillardin'in GluK2/GluK5 reseptörleri üzerinden sürekli bir akım yönlendirdiğini ve bunların genellikle aktivasyondan sonra gelen kendini koruyucu kapatılması olan “desensitize” olmalarına yol açmadığını gösterdiler. Buna karşılık, doğal iletici glutamat aynı reseptörleri açar ve ardından çok hızlı bir şekilde sessizleşmelerine neden olur. Başka bir ilaç olan AMPA da bu reseptörleri aktive eder ama yalnızca kısmi desensitizasyona yol açar. Bu davranışlar, yalnızca GluK5 alt birimlerinin dolu olduğu durumlarda reseptörün uzun ömürlü bir inaktif duruma düşmeden açılabildiğini veya açılışa yaklaşabildiğini, oysa daha yaygın bağlanmanın reseptörü daha derin bir kapatma konfigürasyonuna ittiğini düşündürür.
Hareket eden parçaların eylem anına ait fotoğrafları
Bu farklı işlevsel durumların üç boyutta nasıl göründüğünü görmek için ekip, dikkatle kontrol edilen ligand koşulları altında yapısal anlık görüntüler yakalamak üzere kriyo-elektron mikroskopisini kullandı. GluK5-seçici agonistin varlığında iki ana konformasyon gözlemlediler. Birinde, dört ligand-bağlayıcı domenin tamamı sağlam eşler oluşturmuştu; GluK5 birimleri ligand etrafında kapanmışken GluK2 birimleri açık kaldı. Bu “tam” durum, eşleştirilmiş domenler arasında hafif bir gevşeme ve dönme ile iç gözenek helikslerinde ölçülebilir bir genişleme gösteriyordu; bu, iyon kanal hâlâ kapalı olmasına rağmen ön-aktif, açılmaya hazır bir konfigürasyonla tutarlıdır. İkinci, “kısmen kopmuş” durumda ise bir domen çifti ayrılmışken diğeri sağlam kalmıştı; bu, tam desensitizasyona giden yol üzerinde bir ara adımı fakat henüz kilitlenmiş olmayan bir durumu önerir.
Zamanlamayı ayarlayan gizli menteşeler
Bu yapıları daha önce çözülen tam aktif ve tam desensitize olmuş kainat reseptörleriyle karşılaştırarak, yazarlar dış domen katmanındaki hareketlerin gözenek bölgesine nasıl iletildiğini izlediler. Kompleks içinde karşılıklı duran iki GluK5 alt birimi etrafında özellikle menteşe ve destek görevi gören, hem domen çiftleri içindeki hem de çiftler arasındaki temel temas bölgelerini tanımladılar. Bu noktalardaki ince kaymalar, domenlerin birbirine ne kadar sıkı tutunduğunu ve gözenek açmak için bağlantı elemanlarını ne kadar çektiğini değiştirdi. Ara yüzlerdeki belirli amino asitleri değiştirince, araştırmacılar reseptörün deaktivasyon hızını hızlandırıp yavaşlatabildiler ve desensitizasyona gitme eğilimini değiştirebildiler. Bu, özellikle GluK5 içeren reseptörlerin kısa glutamat patlamalarından sonra alışılmadık şekilde uzun süre aktif kalmasını açıklamaya yardımcı olur.
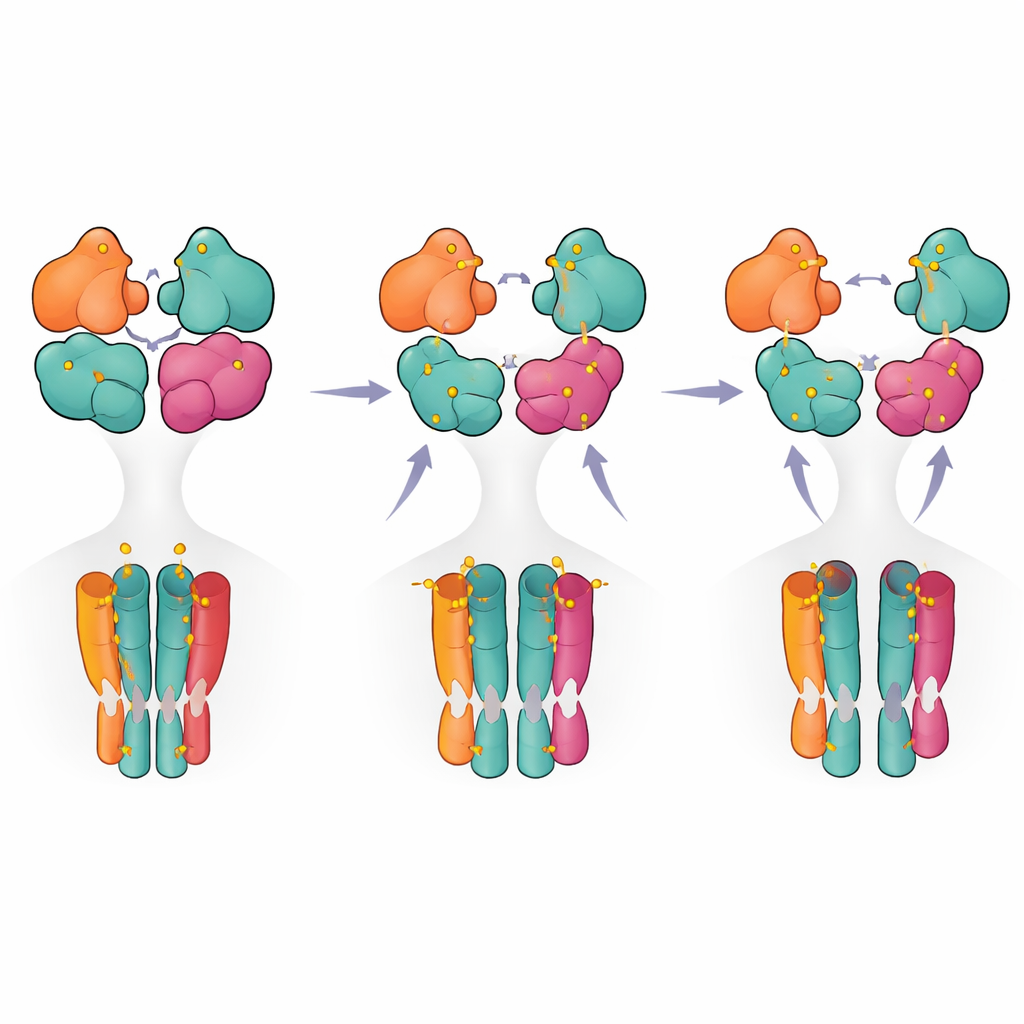
Aktivasyondan kapanmaya adım adım bir yol haritası
Yapısal anlık görüntüleri ve fonksiyonel ölçümleri bir araya getiren yazarlar, reseptörün dinlenme durumundan yalnızca iki alt birim (genellikle GluK5 çifti) dolu olduğunda ön-aktif bir duruma geçtiği adım adım bir model öneriyor. Ek ligand bağlanması bir domen çiftinin kısmi kopuşunu teşvik eder ve yalnızca üç veya dört alt birim dolu olduğunda reseptör, uzun süreli desensitizasyonla ilişkili tamamen kopmuş bir konfigürasyona ulaşır. Uzman olmayanlar için bu, reseptörün basit bir açma-kapama anahtarı gibi değil, farklı doluluk desenleri ve iç temasların sinyalin gücünü ve süresini ayarladığı çok adımlı bir karartıcı (dimmer) gibi davrandığı anlamına gelir. Bu bulgular, önemli bir beyin reseptörünün temel işleyişini netleştirmekle kalmaz, aynı zamanda gelecekteki ilaçların hastalıkta kainat reseptör aktivitesini hassas biçimde ayarlamak üzere hedefleyebileceği yapısal sıcak noktaları da vurgular.
Atıf: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
Anahtar kelimeler: kainat reseptörleri, glutamat sinyalleşmesi, sinaptik iletim, kriyo-EM yapıları, reseptör desensitizasyonu