Clear Sky Science · it
Strutture di eterotetrameri parzialmente occupati offrono indicazioni sull'attivazione e la desensibilizzazione dei recettori kainato
Perché contano i piccoli interruttori del cervello
I recettori kainato sono microscopici interruttori proteici che aiutano le cellule cerebrali a comunicare. Rispondono al neurotrasmettitore glutammato e partecipano a processi che vanno dall’apprendimento e dalla memoria al dolore e all’infiammazione. Quando questi interruttori non funzionano correttamente, sono stati associati a patologie come l’epilessia e disturbi psichiatrici. Questo studio esplora, con dettaglio strutturale senza precedenti, come un importante tipo di recettore kainato si attivi e poi «si spenga» quando solo alcuni dei suoi subunità sono legati da molecole simili al glutammato — una situazione che probabilmente riflette ciò che avviene realmente in molte sinapsi.
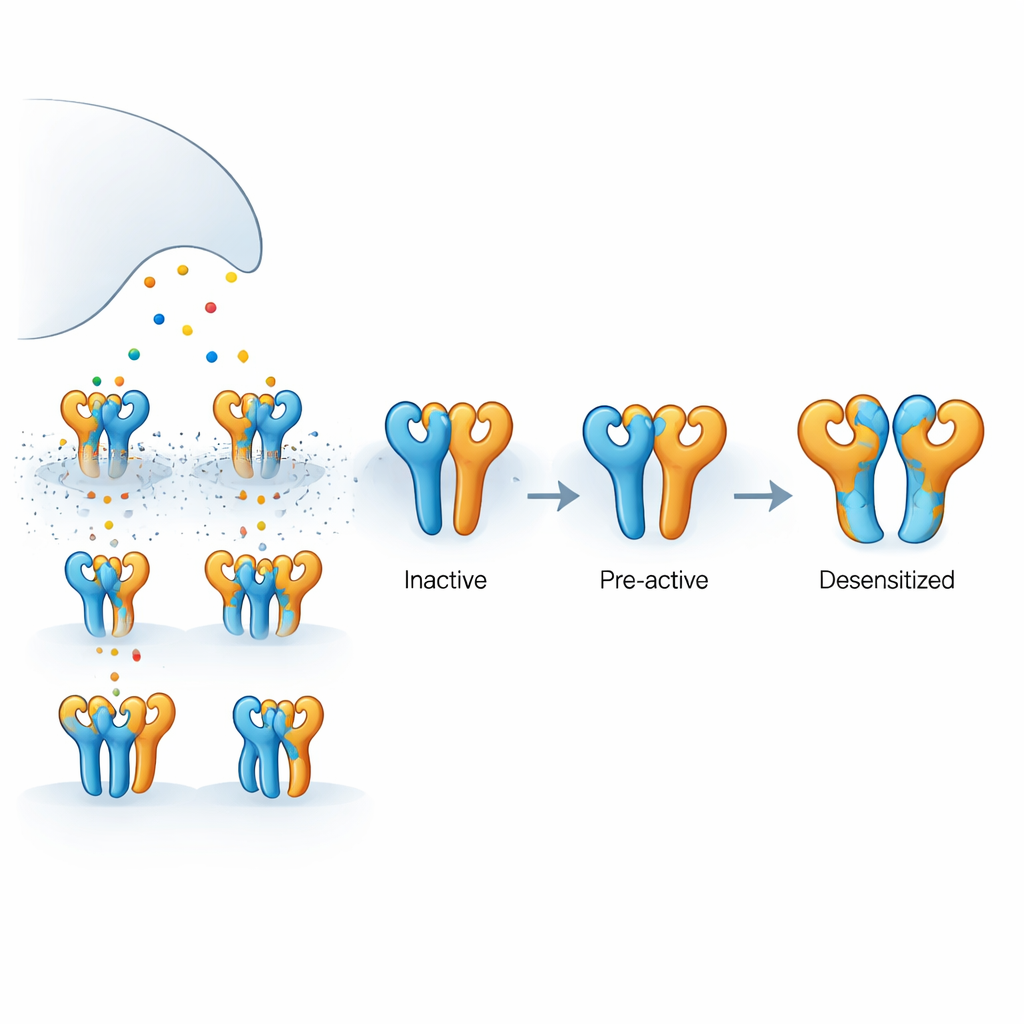
Com’è costruito questo recettore cerebrale
Il recettore esaminato è un recettore kainato composto da due tipi di subunità proteiche, chiamate GluK2 e GluK5, assemblate in un complesso a quattro parti. GluK5 lega il glutammato in modo particolarmente stretto e tende a occupare due posizioni specifiche nel tetramero, mentre GluK2 occupa le altre due. Ciascuna subunità ha un dominio esterno che cattura il glutammato e una regione interna che forma il poro e permette il passaggio degli ioni, generando segnali elettrici. Poiché il glutammato viene rilasciato brevemente ed è rapidamente rimosso, non sempre tutte e quattro le subunità sono occupate contemporaneamente. Capire cosa succede quando sono legate solo alcune di esse è fondamentale per spiegare come le sinapsi reali modulano l’intensità e la durata del segnale.
Inneschi parzialmente premuti che non bloccano
Attraverso registrazioni elettriche su cellule umane, gli autori hanno mostrato che un farmaco selettivo per GluK5, il 5-iodowillardiina, induce una corrente costante attraverso i recettori GluK2/GluK5 senza provocarne la «desensibilizzazione» — lo spegnimento autoprotettivo che segue in genere l’attivazione. Al contrario, il trasmettitore naturale glutammato accende gli stessi recettori per poi farli rapidamente tacere. Un altro agonista, l’AMPA, attiva anch’esso questi recettori ma provoca solo una desensibilizzazione parziale. Questi comportamenti suggeriscono che quando sono occupate soltanto le subunità GluK5, il recettore può aprirsi o avvicinarsi all’apertura senza cadere in uno stato inattivo prolungato, mentre un legame più diffuso spinge il recettore verso una configurazione di spegnimento più profonda.
Istanti degli elementi in movimento in azione
Per vedere come appaiono in tre dimensioni questi diversi stati funzionali, il gruppo ha utilizzato la microscopia elettronica criogenica per catturare istantanee strutturali sotto condizioni di ligando controllate. Con l’agonista selettivo per GluK5 presente, hanno osservato due conformazioni principali. In una, tutti e quattro i domini leganti il ligando formavano coppie integre, con le unità GluK5 chiuse intorno al ligando e le unità GluK2 rimaste aperte. Questo stato «integro» mostrava un leggero allentamento e una rotazione tra i domini accoppiati e un’espansione misurabile delle eliche del poro interno, coerente con una configurazione pre-attiva pronta ad aprirsi anche se il canale ionico risultava ancora chiuso. Nella seconda conformazione, «parzialmente rotta», una coppia di domini si era separata mentre l’altra rimaneva integra, suggerendo un intermedio sul percorso verso la desensibilizzazione completa ma non ancora bloccato in essa.
Cerniere nascoste che regolano i tempi
Confrontando queste strutture con recettori kainato precedentemente risolti in stato totalmente attivo e totalmente desensibilizzato, gli autori hanno tracciato come i movimenti nello strato dei domini esterni siano trasmessi al poro. Hanno identificato regioni di contatto chiave sia all’interno sia tra le coppie di domini che fungono da cerniere e rinforzi, soprattutto attorno alle due subunità GluK5 che si trovano l’una di fronte all’altra nel complesso. Piccoli spostamenti in questi siti modificano la forza con cui i domini si tengono insieme e il modo in cui tirano i legami che aprono il poro. Quando i ricercatori hanno sostituito alcuni amminoacidi in queste interfacce, hanno potuto rendere il recettore più rapido o più lento nella disattivazione e alterare la sua propensione alla desensibilizzazione. Ciò aiuta a spiegare perché i recettori contenenti GluK5, in particolare, restano attivi per tempi insolitamente lunghi dopo brevi esplosioni di glutammato.
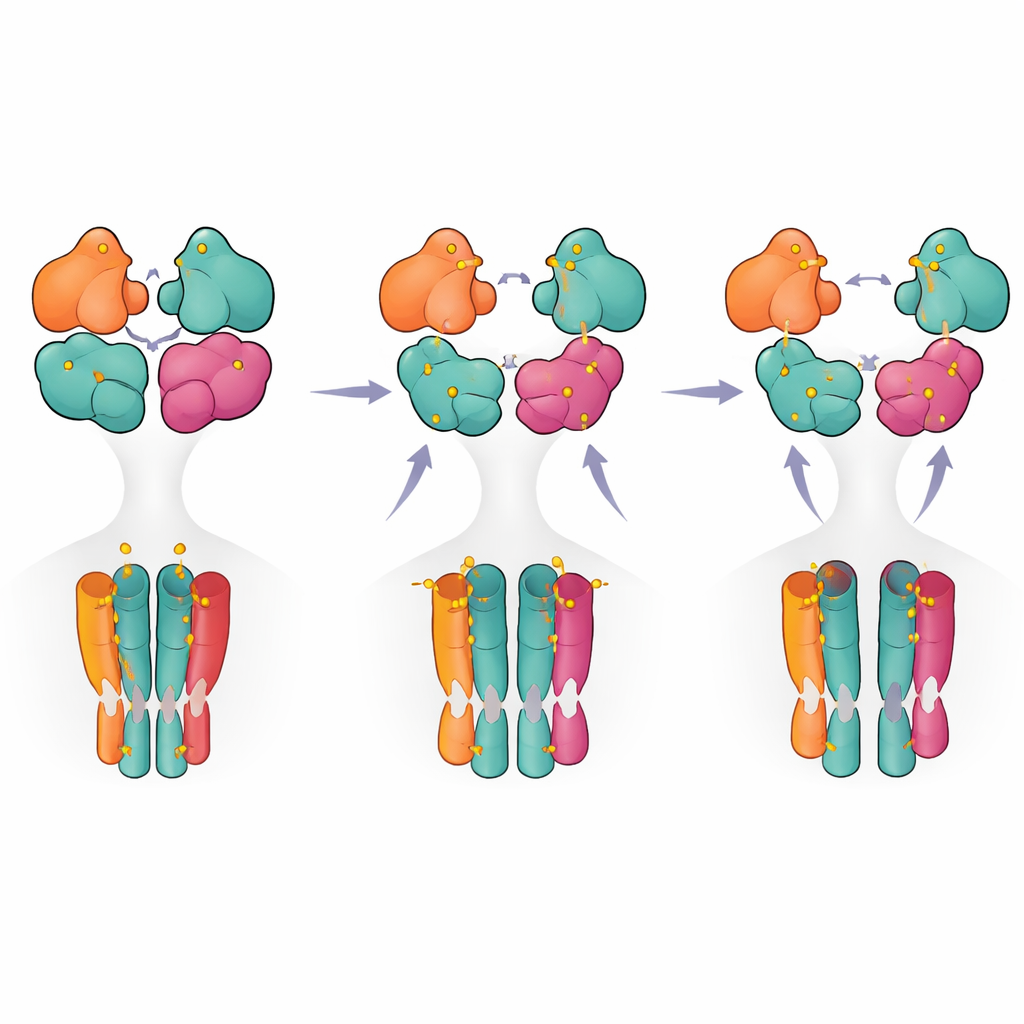
Una mappa passo dopo passo dall’attivazione allo spegnimento
Unendo le istantanee strutturali e le misure funzionali, gli autori propongono un modello graduale in cui il recettore passa da uno stato di riposo a uno stato pre-attivo quando sono occupate solo due subunità (tipicamente la coppia GluK5). Il legame di ulteriori ligandi favorisce la rottura parziale di una coppia di domini e solo quando sono occupate tre o quattro subunità il recettore raggiunge una configurazione completamente rotta associata a una desensibilizzazione di lunga durata. Per i non specialisti, ciò significa che il recettore si comporta meno come un semplice interruttore acceso/spento e più come un dimmer a più fasi, con diversi modelli di occupazione e contatti interni che modulano intensità e durata del segnale. Queste intuizioni non solo chiariscono il funzionamento di base di un recettore cerebrale chiave, ma evidenziano anche punti strutturali sensibili che potrebbero essere bersagliati da futuri farmaci volti a modulare finemente l’attività dei recettori kainato nelle malattie.
Citazione: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
Parole chiave: recettori kainato, segnalazione del glutammato, trasmissione sinaptica, strutture cryo-EM, desensibilizzazione del recettore