Clear Sky Science · pl
Struktury częściowo obsadzonych heterotetramerów wyjaśniają aktywację i desensytyzację receptorów kainianowych
Dlaczego drobne przełączniki mózgowe mają znaczenie
Receptory kainianowe to mikroskopijne białkowe przełączniki, które umożliwiają komunikację między komórkami mózgu. Reagują na neuroprzekaźnik glutaminian i biorą udział w procesach od uczenia się i pamięci po ból i zapalenie. Gdy te przełączniki zawodzą, powiązano je z zaburzeniami takimi jak padaczka i choroby psychiczne. W tym badaniu, z niespotykaną dotąd szczegółowością strukturalną, analizuje się, jak jeden z głównych typów receptorów kainianowych włącza się, a potem „wyłącza się samoczynnie”, gdy tylko niektóre jego podjednostki są związane przez związki przypominające glutaminian — sytuacja, która prawdopodobnie odzwierciedla to, co dzieje się w wielu rzeczywistych synapsach.
Jak zbudowany jest ten receptor
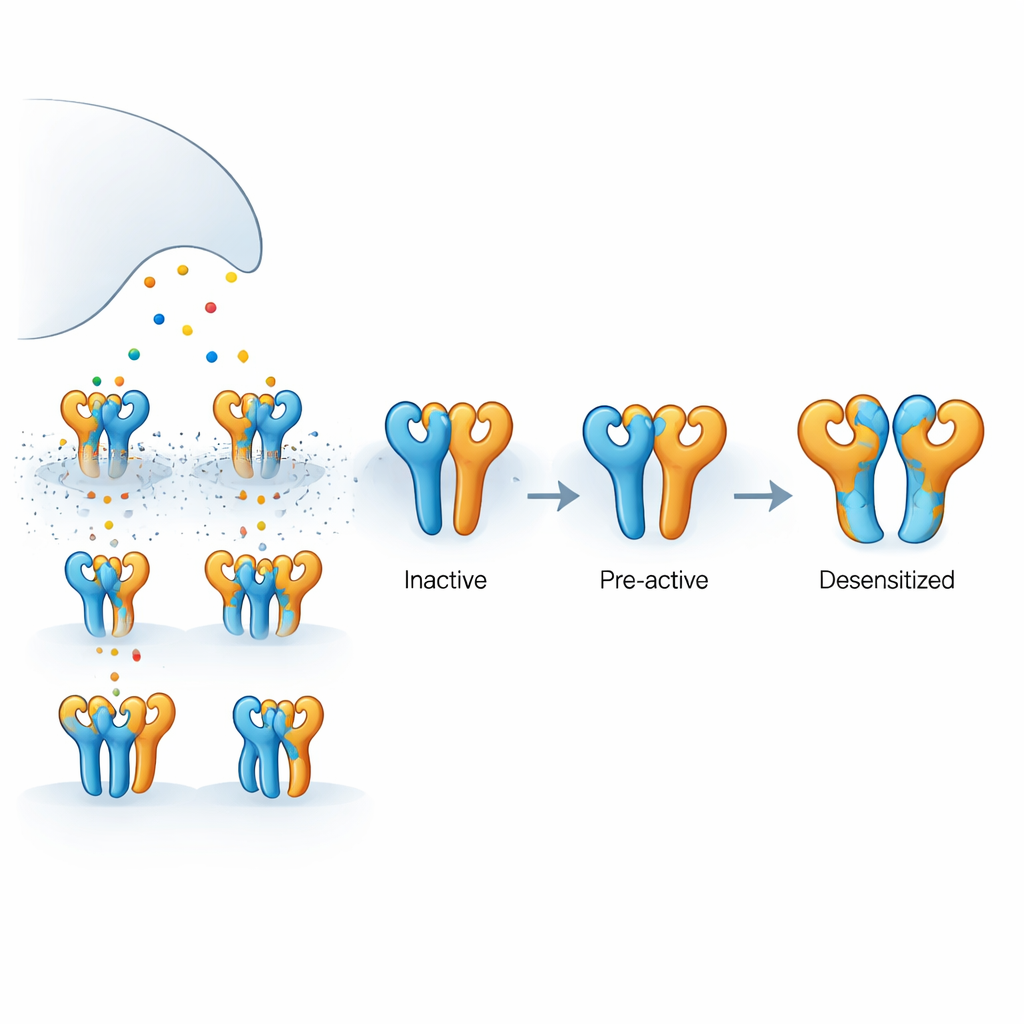
Badany tu receptor to receptor kainianowy złożony z dwóch rodzajów podjednostek białkowych, zwanych GluK2 i GluK5, zmontowanych w kompleks czteroczęściowy. GluK5 wiąże glutaminian szczególnie silnie i ma tendencję do zajmowania dwóch określonych pozycji w tetramerze, podczas gdy GluK2 zajmuje pozostałe dwie. Każda podjednostka ma zewnętrzną domenę chwytającą glutaminian oraz wewnętrzny region formujący por, który pozwala na przepływ jonów, generując sygnały elektryczne. Ponieważ glutaminian jest uwalniany krótko i szybko usuwany, nie wszystkie cztery podjednostki są zawsze zajęte jednocześnie. Zrozumienie, co się dzieje, gdy związane są tylko niektóre z nich, jest kluczowe dla wyjaśnienia, jak rzeczywiste synapsy modulują siłę i czas trwania sygnału.
Niecałkowicie wciśnięte spusty, które nie zacinają mechanizmu
Na podstawie pomiarów elektrofizjologicznych w ludzkich komórkach autorzy wykazali, że selektywny dla GluK5 agonista, 5-jodowillardyna, wywołuje stały prąd przez receptory GluK2/GluK5, nie powodując ich „desensytyzacji” — samoochronnego wyłączenia, które zwykle następuje po aktywacji. Dla porównania, naturalny przekaźnik glutaminian powoduje włączenie tych samych receptorów, a następnie bardzo szybkie ich wyciszenie. Inny agonista, AMPA, również aktywuje te receptory, lecz wywołuje jedynie częściową desensytyzację. Takie zachowania sugerują, że gdy zajęte są tylko podjednostki GluK5, receptor może się otworzyć lub być bliski otwarcia, nie przechodząc w długotrwały stan nieaktywności, podczas gdy bardziej rozległe wiązanie popycha receptor w głębszą konfigurację wyłączającą.
Ujęcia ruchomych elementów w akcji
Aby zobaczyć, jak te różne stany funkcjonalne wyglądają w trzech wymiarach, zespół zastosował kriogeniczną mikroskopię elektronową (cryo-EM), aby uchwycić strukturalne migawki przy starannie kontrolowanych warunkach ligandowych. W obecności selektywnego agonisty dla GluK5 zaobserwowano dwie główne konformacje. W jednej wszystkie cztery domeny wiążące ligand utworzyły nienaruszone pary, z jednostkami GluK5 zamkniętymi wokół liganda, podczas gdy domeny GluK2 pozostały otwarte. Ten „nienaruszony” stan wykazywał subtelne rozluźnienie i rotację między sparowanymi domenami oraz mierzalne rozszerzenie helis tworzących por wewnętrzny, zgodne z konfiguracją przedaktywną, gotową do otwarcia, mimo że kanał jonowy wciąż był zamknięty. W drugim, „częściowo rozerwanym” stanie jedna para domen rozdzieliła się, podczas gdy druga pozostała nienaruszona, co sugeruje pośredni etap na drodze do pełnej desensytyzacji, ale jeszcze niezablokowany.
Ukryte zawiasy regulujące czas
Porównując te struktury z uprzednio rozwiązanymi pełni aktywnymi i w pełni desensytyzowanymi receptorami kainianowymi, autorzy prześledzili, jak ruchy w zewnętrznej warstwie domen przenoszone są na por. Zidentyfikowali kluczowe obszary kontaktu zarówno w obrębie par domen, jak i między nimi, które działają jak zawiasy i wzmocnienia, szczególnie wokół dwóch podjednostek GluK5, które siedzą naprzeciw siebie w kompleksie. Subtelne przesunięcia w tych miejscach zmieniały siłę trzymania domen razem i sposób, w jaki pociągają one łączniki rozciągające por. Gdy badacze wymieniali niektóre aminokwasy na tych interfejsach, mogli przyspieszyć lub spowolnić deaktywację receptora oraz zmienić jego skłonność do desensytyzacji. To pomaga wyjaśnić, dlaczego receptory zawierające GluK5, w szczególności, pozostają aktywne niezwykle długo po krótkich impulsach glutaminianu.
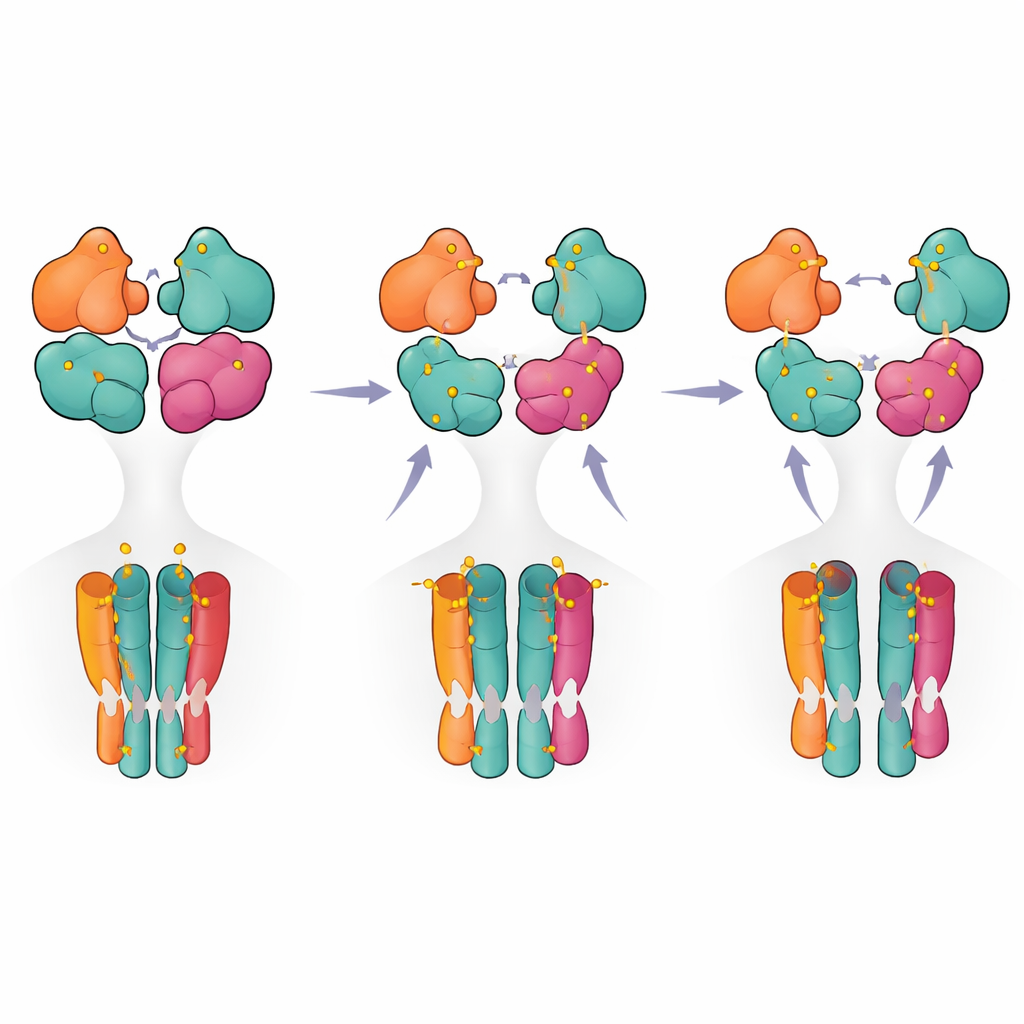
Krokowa mapa od aktywacji do wyłączenia
Łącząc strukturalne migawki i pomiary funkcjonalne, autorzy proponują model krokowy, w którym receptor przechodzi ze stanu spoczynkowego do stanu przedaktywnego, gdy zajęte są tylko dwie podjednostki (zwykle para GluK5). Dalsze wiązanie liganda sprzyja częściowemu rozerwaniu jednej pary domen, i dopiero gdy zajęte są trzy lub cztery podjednostki, receptor osiąga w pełni rozerwaną konfigurację związaną z długotrwałą desensytyzacją. Dla osób niebędących specjalistami oznacza to, że receptor zachowuje się mniej jak prosty włącznik on–off, a bardziej jak wielostopniowy ściemniacz, gdzie różne wzory obsadzenia i wewnętrzne kontakty regulują, jak mocno i jak długo sygnalizuje. Te spostrzeżenia nie tylko wyjaśniają podstawowe działanie kluczowego receptora mózgowego, ale także wskazują strukturalne „hotspoty”, które mogą być celem przyszłych leków mających na celu precyzyjne modulowanie aktywności receptorów kainianowych w chorobach.
Cytowanie: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
Słowa kluczowe: receptory kainianowe, sygnalizacja glutaminianowa, transmisja synaptyczna, struktury cryo-EM, desensytyzacja receptorów