Clear Sky Science · ja
部分的に占有されたヘテロ四量体の構造はカイナート受容体の活性化と脱感作の理解を深める
なぜ小さな脳のスイッチが重要なのか
カイナート受容体は、脳細胞同士の通信を助ける微小なタンパク質スイッチです。神経伝達物質グルタミン酸に応答し、学習や記憶から痛みや炎症に至るさまざまな過程に関与します。これらのスイッチが誤作動すると、てんかんや精神疾患などの病態と関連することがあります。本研究は、ある主要なカイナート受容体がどのようにオンになり、その後に「自らをオフにする」かを、構造学的に未曾有の詳細さで探ります。ここではサブユニットの一部だけがグルタミン酸様分子に結合している状況、すなわち多くの実際のシナプスで起きていると考えられる状態に着目しています。
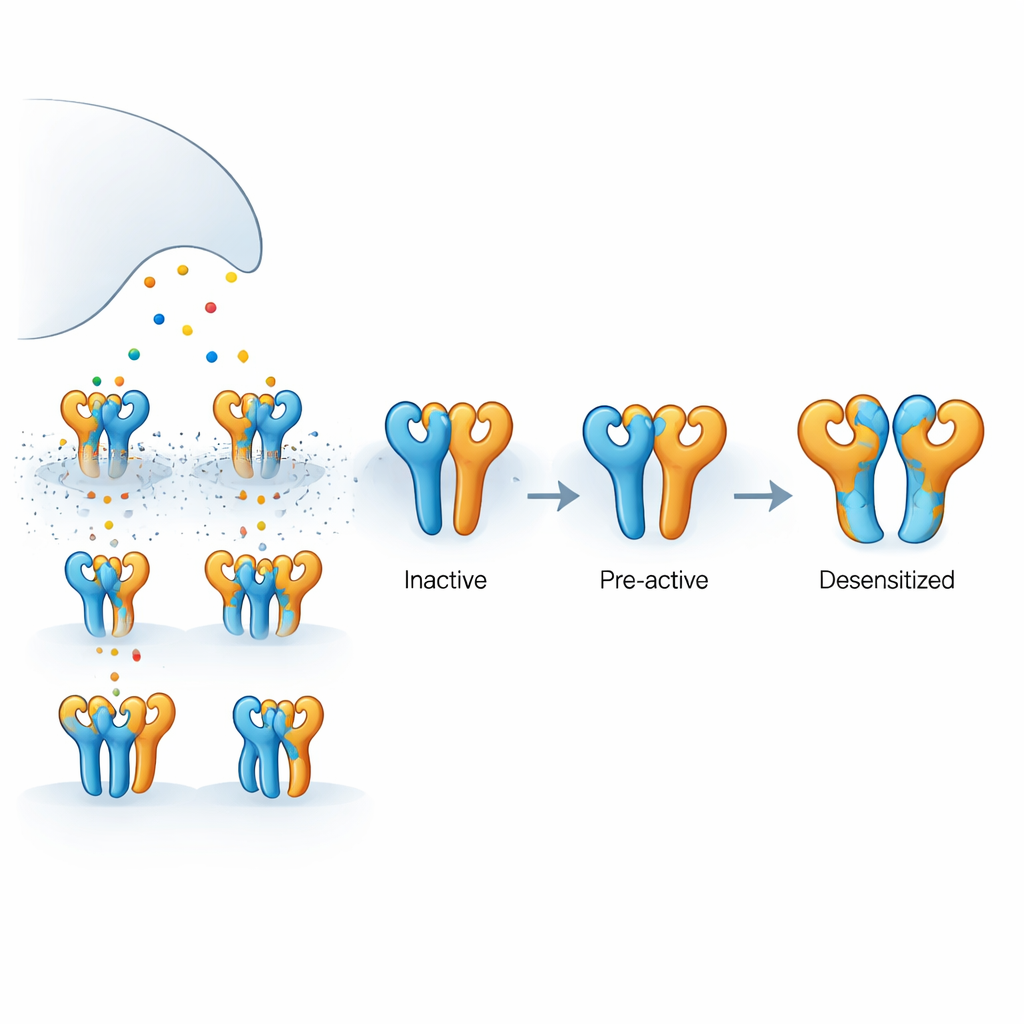
この脳受容体の構造
ここで調べられた受容体は、GluK2とGluK5と呼ばれる2種類のタンパク質サブユニットから構成されるカイナート受容体で、四つの部分が組み合わさって複合体を形成します。GluK5はグルタミン酸を特に強く結合し、四量体の中で特定の二つの位置を占める傾向があり、GluK2が残る二つを占めます。それぞれのサブユニットは外側にグルタミン酸を受け取るドメインと、内側にイオンを流すことで電気信号を生み出す孔を形成する領域を持ちます。グルタミン酸は短時間に放出され速やかに回収されるため、四つすべてのサブユニットが常に同時に占有されるわけではありません。一部だけが結合しているときに何が起きるかを理解することは、実際のシナプスが信号の強さやタイミングをどのように調整するかを説明する鍵です。
押されても詰まらない部分的なトリガー
ヒト細胞での電気生理計測により、著者らはGluK5選択的な作動薬である5-ヨードウィラルジンが、GluK2/GluK5受容体を持続的に流す電流を誘導する一方で、通常の活性化に続いて生じる自己保護的なシャットオフである「脱感作」を引き起こさないことを示しました。対照的に、自然の伝達物質であるグルタミン酸は同じ受容体を活性化した後、非常に速やかに静止状態に戻します。別の薬剤であるAMPAもこれらの受容体を活性化しますが、脱感作は部分的にしか生じません。これらの挙動は、GluK5サブユニットだけが占有されている場合、受容体が開口するか開口に近づくことができても長時間続く不活性状態に陥らないのに対し、より広範な結合が生じると受容体がより深いシャットオフ構成へ押し込まれることを示唆します。
動く部品のスナップショット
これらの異なる機能状態が三次元でどのように見えるかを明らかにするために、研究チームはクライオ電子顕微鏡を用いて、制御されたリガンド条件下で構造のスナップショットを撮影しました。GluK5選択的作動薬が存在する場合、彼らは主に二つのコンフォーメーションを観察しました。一つは、四つのリガンド結合ドメインがすべて完全なペアを形成し、GluK5ユニットはリガンドに閉じ、GluK2ユニットは開いたままである状態です。この「完全」状態では、対になったドメイン間のわずかな緩みや回転と、内側の孔を形成するヘリックスの測定可能な拡張が見られ、イオンチャネル自体は閉じたままでも開口準備が整った前駆的な構成に一致します。第二の「部分的に断裂した」状態では、一方のドメインペアが分離し、他方は保たれており、完全な脱感作への経路上の中間体を示唆するものの、まだロックされた状態には至っていませんでした。
タイミングを調節する隠れた蝶番
これらの構造を以前に解かれた完全活性状態や完全脱感作状態のカイナート受容体と比較することで、著者らは外側ドメイン層の運動がどのように孔に伝達されるかをたどりました。彼らは、ドメインペア内およびペア間の重要な接触領域を同定し、特に複合体内で互いに向かい合う二つのGluK5サブユニットの周りで蝶番や補強の役割を果たしていることを示しました。これらの部位での微妙な変化が、ドメイン同士の結合の強さや孔を引き開くリンカーへの牽引力を変化させます。研究者らがこれらの界面の特定のアミノ酸を置換すると、受容体が非活性化する速度や脱感作しやすさを速くしたり遅くしたりできました。これにより、特にGluK5を含む受容体が短いグルタミン酸の放出後にも異常に長く活性を維持する理由が説明されます。
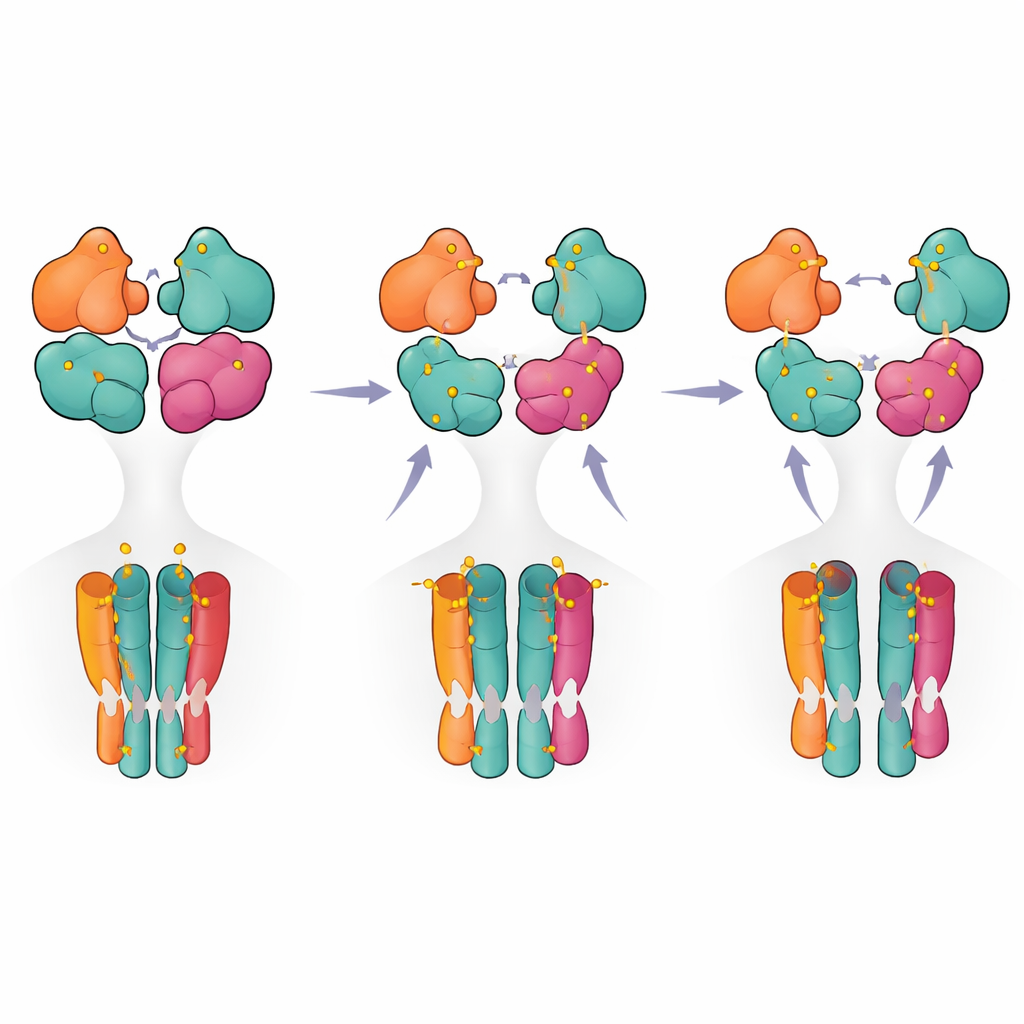
活性化からシャットダウンへの段階的ロードマップ
構造的スナップショットと機能測定を統合して、著者らは段階的モデルを提案します。受容体は安静状態から、通常はGluK5対である二つのサブユニットだけが占有されているときに前駆活性状態へ移行します。追加のリガンド結合は一つのドメインペアの部分的断裂を促進し、三つまたは四つのサブユニットが占有されるときにのみ、長時間続く脱感作と関連する完全断裂構成に到達します。非専門家向けに言えば、受容体は単純なオン・オフスイッチというよりも段階的なディマー(調光器)のように振る舞い、さまざまな占有パターンと内部接触が信号の強さと持続時間を調整します。これらの知見は、主要な脳受容体の基本的な働きを明らかにするだけでなく、将来の薬剤が疾患におけるカイナート受容体の活性を精密に調節するために標的にできる構造的ホットスポットを浮き彫りにします。
引用: Khanra, N.K., Strauss, A., Moreno Wasielewski, L. et al. Structures of partially occupied hetero-tetramers provide insight into kainate receptor activation and desensitization. Nat Commun 17, 3789 (2026). https://doi.org/10.1038/s41467-026-72226-w
キーワード: カイナート受容体, グルタミン酸シグナル伝達, シナプス伝達, クライオ電子顕微鏡構造, 受容体の脱感作