Clear Sky Science · zh
深度可视化蛋白组学揭示伤害感受器的多样性与疼痛靶点
为何微小的痛觉细胞至关重要
疼痛是机体最重要的警示系统之一,但并非所有感知疼痛的神经细胞都以相同方式工作。有些对热敏感,有些对捏压或压力有反应,还有一些在受伤或炎症将它们“唤醒”之前保持沉默。本研究深入分析了单个小鼠痛觉神经元内的实际蛋白质,以弄清它们彼此不同的原因——并确定可能用于缓解慢性疼痛的新分子开关。
更近距离地审视体内的痛觉传递者
位于脊柱的感觉神经细胞簇——背根节——将触觉、温度和损伤的信息传送到大脑。在这些簇中存在许多神经元亚型,包括专门检测有害刺激的伤害感受器。早期研究使用RNA(细胞的指令手册)来绘制这种多样性。但RNA只告诉我们一部分信息:它暗示了哪些蛋白可能存在,而不是哪些蛋白实际存在并且处于活跃状态。最终决定神经元如何放电以及我们如何感觉疼痛的是蛋白质,而不是基因。作者旨在构建不同感觉神经元类型的详细蛋白水平图谱,包括两个主要的痛觉亚群和对触觉敏感的机械感受器。
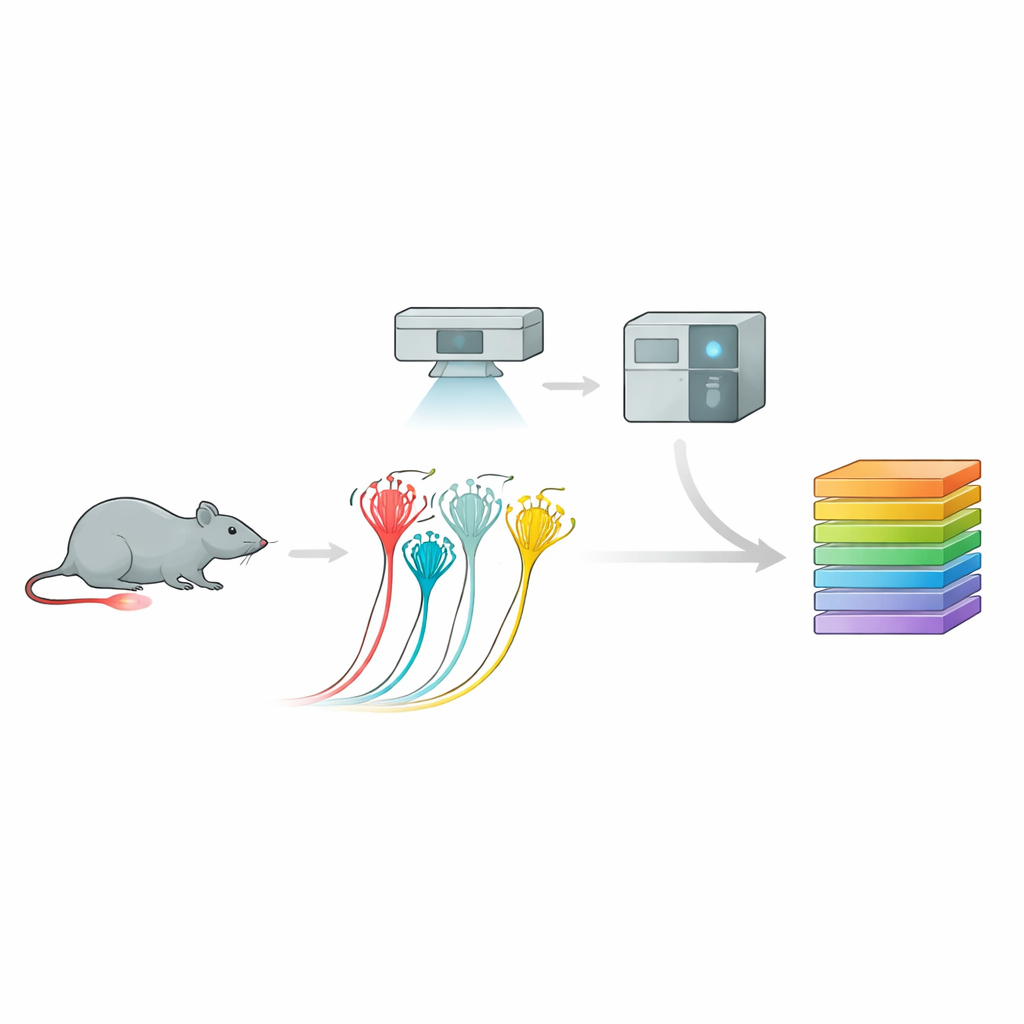
将图像转化为蛋白质目录
为此,团队使用了一套强大的流程,称为深度可视化蛋白组学。首先,他们在培养皿中培养小鼠感觉神经元并记录其对压力的电生理反应,基于行为和表面标志区分了含肽性伤害感受器、非含肽性伤害感受器以及较大的触觉敏感神经元。然后,借助人工智能引导的图像分析和激光显微切割,他们精确地切取出感兴趣的细胞。每个微小样本——小到单个神经元的一小部分——被送入超灵敏质谱仪,识别并定量了数千种蛋白质。这一方法为每种神经元亚型产生了丰富的蛋白谱,揭示出与此前基因表达图谱高度一致但又更加详尽的独特分子“指纹”。
用蛋白质书写的痛觉细胞多样性
研究者发现,每种伤害感受器亚型都携带一组稳定的核心蛋白,以及其独特的特征性标志。含肽性和非含肽性伤害感受器——两类长期被识别的痛觉细胞——在离子通道、信号分子和代谢通路方面表现出明显差异。许多已知的与疼痛相关的蛋白出现了,但也有一些不太熟悉的候选蛋白强烈标记了某一亚型。重要的是,当团队将培养神经元与仍嵌在脊髓组织中的神经元进行比较时,大多数蛋白具有重叠性。这表明培养神经元作为疼痛研究的常用模型,在蛋白水平上在很大程度上保留了体内特性,是探索疼痛通路工作机制的可靠模型。
炎症如何“解除沉默”痛觉纤维
随后研究聚焦于一个经典的疼痛情景:炎症致敏。在动物和人类中,一种称为神经生长因子(NGF)的生长因子可以使某些伤害感受器对机械刺激变得极度敏感,这一过程被认为有助于炎症皮肤或关节的触痛。作者通过在培养神经元中加入NGF和一种蛋白激酶激活剂来模拟这一过程,使先前沉默的含肽性伤害感受器转变为对机械压入有强烈反应的细胞。比较处理组与对照组的蛋白谱,他们检测到一小组蛋白在被致敏的含肽性神经元中特异性上调。其中一种帮助将糖链添加到其他分子上的酶——B3GNT2,成为一个尤其有力的候选者。
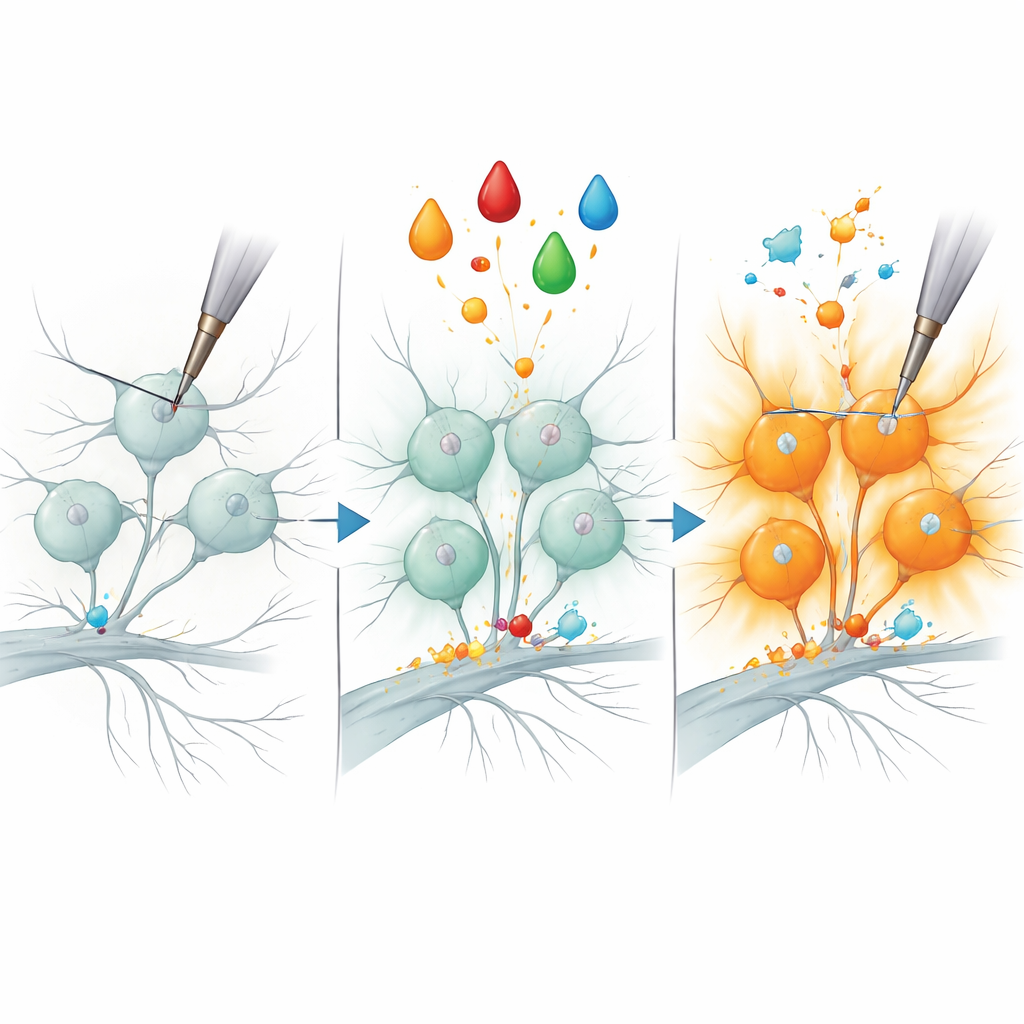
对疼痛的新的分子把柄
为检验B3GNT2是否不仅仅是旁观者,团队在伤害感受器中使用小干扰RNA降低了该酶的表达,然后重复了炎症性处理。值得注意的是,变得对机械刺激有反应的神经元显著减少,这提示该酶对某些痛觉纤维的“解除沉默”是必需的。尽管致敏的其他特征可能依赖于额外的蛋白,这一结果将特定的糖基修饰酶与机械性超敏的快速发生联系了起来。因为人类B3GNT2基因的变异已与疼痛性炎症疾病相关联,这项工作将该蛋白——以及其执行的糖基修饰——定位为理解并最终治疗慢性疼痛的有前景的新切入点。
引用: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
关键词: 伤害感受器, 蛋白质组学, 慢性疼痛, 感觉神经元, 神经生长因子