Clear Sky Science · ru
Глубокая визуальная протеомика выявляет разнообразие ноцицепторов и мишени боли
Почему имеют значение крошечные клетки, ощущающие боль
Боль — одна из важнейших предупредительных систем организма, однако не все болевые нервные клетки ведут себя одинаково. Некоторые реагируют на тепло, другие — на щипок или давление, а некоторые молчат, пока травма или воспаление не «разбудят» их. В этом исследовании детально изучены белки внутри отдельных болевых нейронов мыши, чтобы понять, что делает их разными, и выявить новые молекулярные переключатели, на которые можно нацелиться для облегчения хронической боли.
Ближе к посредникам боли в организме
Пучки сенсорных нервных клеток в позвоночнике, называемые дорсальными корешковыми ганглиями, передают в мозг информацию о прикосновениях, температуре и повреждениях. В этих пучках присутствуют многие подтипы нейронов, включая ноцицепторы, специализированные на обнаружении вредных раздражителей. Ранее разнообразие картировалось с помощью РНК, «инструкции» клетки. Но РНК даёт лишь часть картины: она указывает, какие белки могут существовать, но не говорит, какие из них действительно присутствуют и активны. Именно белки, а не гены, в конечном счёте определяют, как нейрон генерирует импульс и как мы ощущаем боль. Авторы поставили задачу создать подробную карту на уровне белков для различных типов сенсорных нейронов, включая две крупные подгруппы болевых нейронов и механорецепторы, чувствительные к прикосновениям.
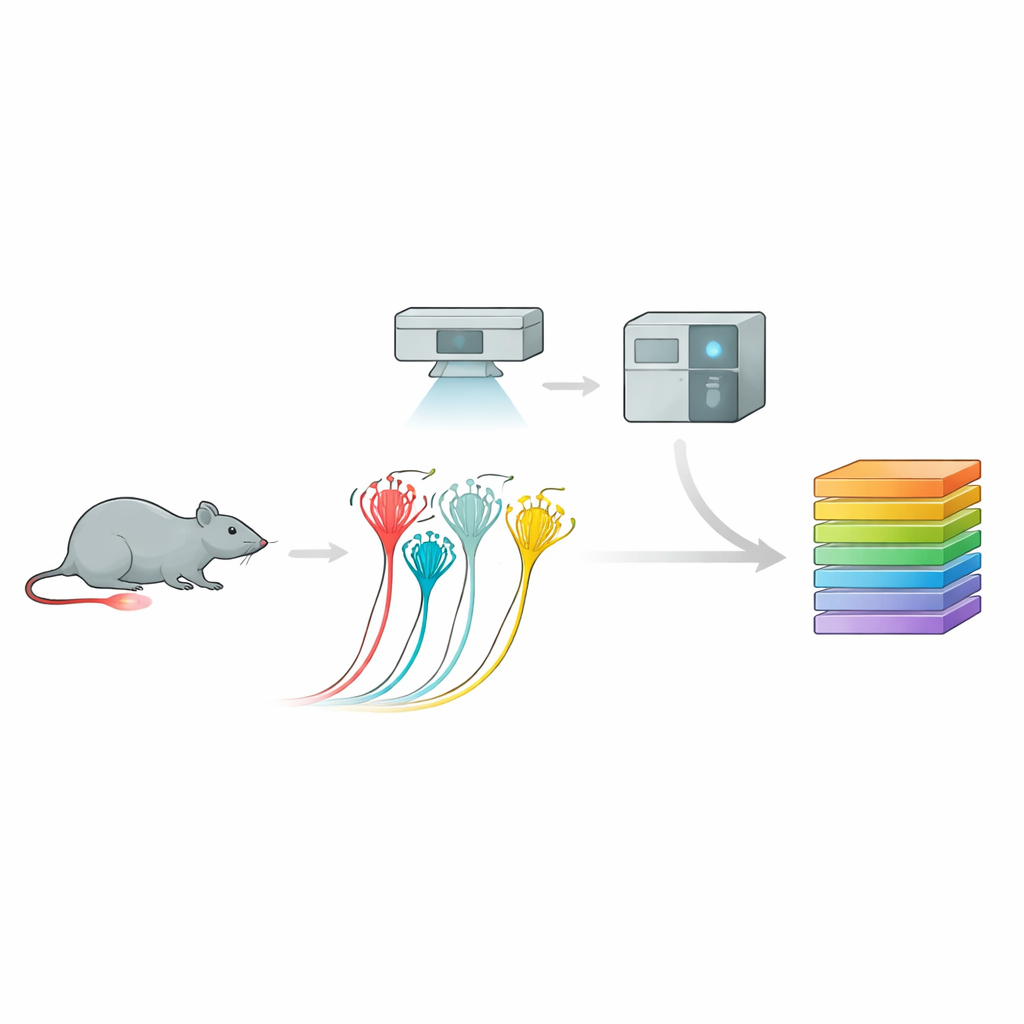
Преобразование изображений в каталоги белков
Для этого команда использовала мощный конвейер, который назвали глубокой визуальной протеомикой. Сначала они выращивали сенсорные нейроны мыши в культуре и регистрировали их электрические ответы на давление, различая пептидергические ноцицепторы, непептидергические ноцицепторы и более крупные чувствительные к прикосновению нейроны по их поведению и поверхностным маркерам. Затем с помощью анализа изображений на базе ИИ и лазерной микродисекции они точно вырезали только интересующие клетки. Каждый крошечный образец — вплоть до части одного нейрона — подавали в сверхчувствительный масс-спектрометр, который идентифицировал и количественно оценивал тысячи белков. Такой подход дал богатые белковые профили для каждого подтипа нейронов, выявив отличительные молекулярные «отпечатки», которые хорошо совпадали с, но и расширяли предыдущие карты экспрессии генов.
Разнообразие болевых клеток, записанное в белках
Исследователи обнаружили, что каждый подтип ноцицепторов несёт стабильный основной набор белков, а также собственную уникальную сигнатуру. Пептидергические и непептидергические ноцицепторы — два давно известных класса болевых клеток — демонстрировали явные различия в ионных каналах, сигнальных молекулах и метаболических путях. Появлялись многие известные белки, связанные с болью, но также и менее изученные кандидаты, которые чётко маркировали один подтип больше, чем другой. Важно, что при сравнении культивированных нейронов с нейронами, всё ещё встроенными в спинальную ткань, большинство белков совпадало. Это указывает на то, что культивированные нейроны, широко используемые в исследованиях боли, в значительной степени сохраняют свою внутритканевую идентичность на уровне белков, делая их надёжной моделью для изучения работы болевых путей.
Как воспаление «размолкает» болевые волокна
Дальше исследование сосредоточилось на классическом сценарии боли: воспалительной сенситизации. У животных и людей фактор роста NGF может значительно повышать чувствительность определённых ноцицепторов к механическим раздражителям — процесс, который, как полагают, способствует болезненности воспалённой кожи или суставов. Авторы смоделировали это, купая культуру нейронов в NGF вместе с активатором протеинкиназы, превращая ранее тихие пептидергические ноцицепторы в активных ответчиков на механическое вдавливание. Сравнивая белковые профили обработанных и необработанных клеток, они выявили небольшой набор белков, уровни которых повышались специфически в сенситизированных пептидергических нейронах. Одним из ферментов, B3GNT2, который участвует в присоединении сахарных цепей к другим молекулам, оказался особенно сильным кандидатом.
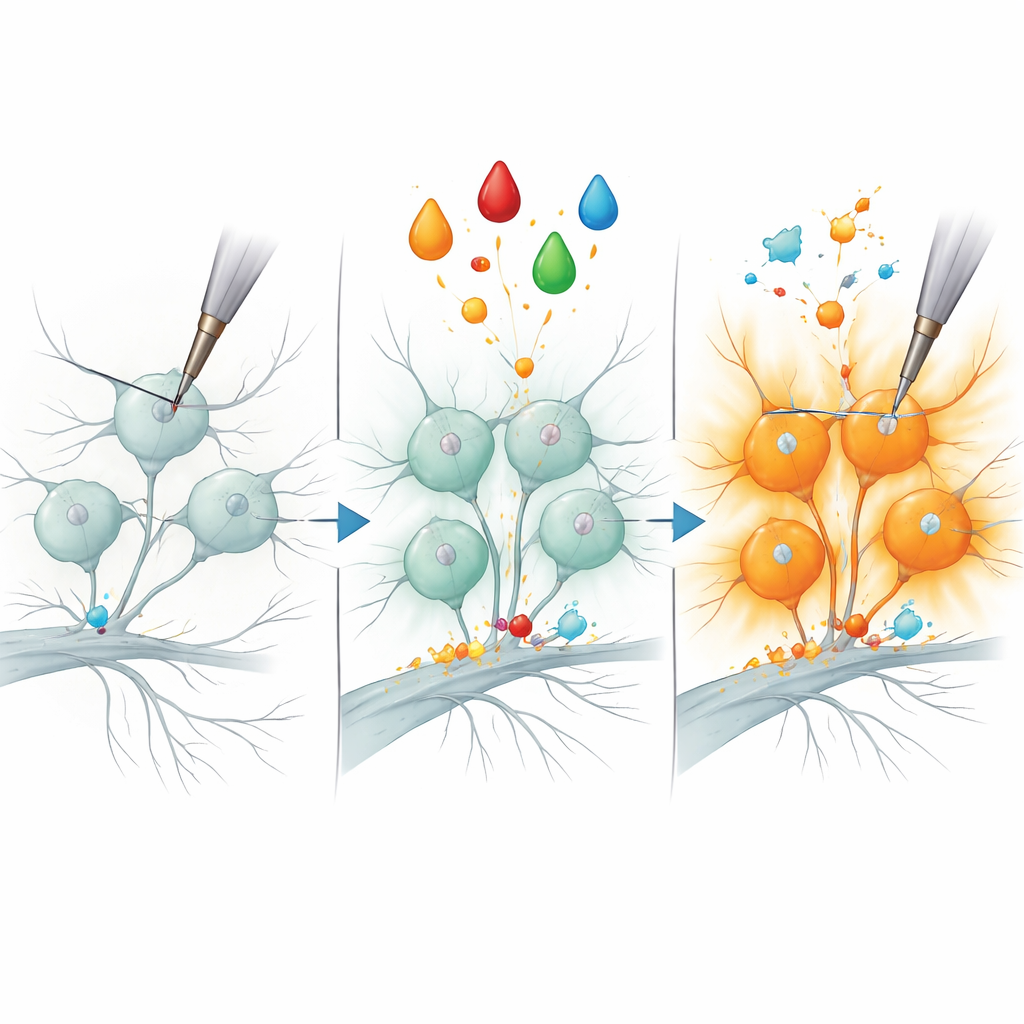
Новый молекулярный рычаг в боли
Чтобы проверить, является ли B3GNT2 не просто наблюдаемым маркером, команда снизила его продукцию в ноцицепторах с помощью малых интерферирующих РНК и затем повторила воспалительную обработку. Поразительно, гораздо меньше нейронов стали механически отзывчивыми, что предполагает, что этот фермент необходим для «размолкания» определённых болевых волокон. Хотя другие аспекты сенситизации, вероятно, зависят от дополнительных белков, этот результат связывает специфический фермент, модифицирующий сахара, с быстрым возникновением механической гиперчувствительности. Поскольку вариации гена B3GNT2 у людей ассоциировались с болезненными воспалительными состояниями, работа выделяет этот белок — и сахарные модификации, которые он осуществляет — как перспективное направление для понимания и, в перспективе, лечения хронической боли.
Цитирование: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
Ключевые слова: ноцицепторы, протеомика, хроническая боль, сенсорные нейроны, фактор роста нервов