Clear Sky Science · pt
Proteômica visual profunda revela diversidade de nociceptores e alvos para dor
Por que pequenas células que detectam dor importam
A dor é um dos sistemas de alerta mais importantes do corpo, mas nem todas as células nervosas que detectam dor se comportam da mesma forma. Algumas respondem ao calor, outras à pinça ou pressão, e algumas permanecem silenciosas até que uma lesão ou inflamação as “acorde”. Este estudo investiga profundamente as proteínas reais dentro de neurônios sensoriais de camundongo individualmente para entender o que os diferencia — e para identificar novos interruptores moleculares que possam ser alvo para aliviar a dor crônica.
Um olhar mais próximo aos mensageiros da dor do corpo
Feixes de células nervosas sensoriais na coluna, chamados gânglios da raiz dorsal, enviam informações sobre toque, temperatura e lesão ao cérebro. Dentro desses feixes existem muitos subtipos de neurônios, incluindo nociceptores especializados em detectar estímulos nocivos. Pesquisas anteriores usaram RNA, o manual de instruções da célula, para mapear essa diversidade. Mas o RNA conta apenas parte da história: ele sugere quais proteínas poderiam existir, não quais estão realmente presentes e ativas. São as proteínas, e não os genes, que em última instância determinam como um neurônio dispara e como sentimos dor. Os autores propuseram construir um mapa detalhado ao nível de proteínas dos diferentes tipos de neurônios sensoriais, incluindo dois grandes subgrupos que detectam dor e mecanorreceptores sensíveis ao toque.
Transformando imagens em catálogos de proteínas
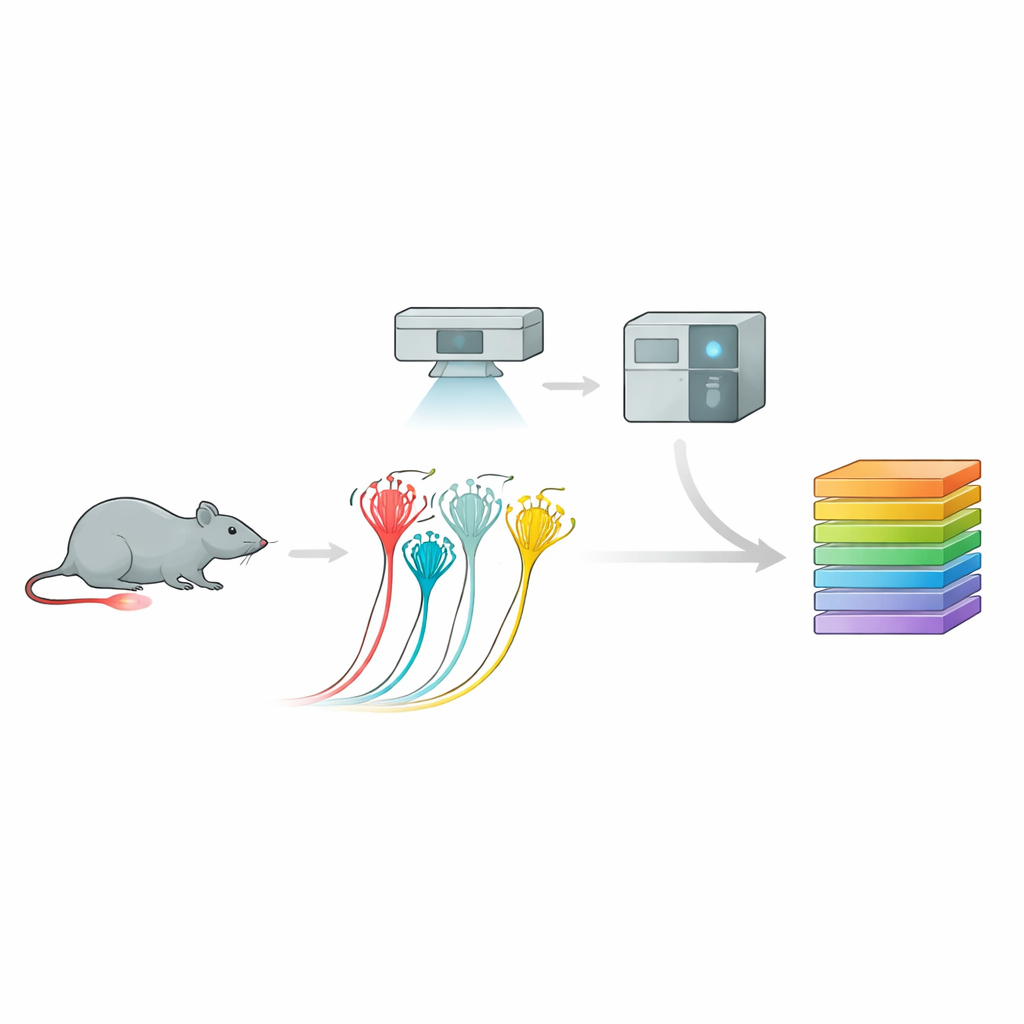
Para isso, a equipe usou um pipeline poderoso chamado proteômica visual profunda. Primeiro, cultivaram neurônios sensoriais de camundongo e registraram suas respostas elétricas à pressão, distinguindo nociceptores peptidérgicos, nociceptores não peptidérgicos e neurônios maiores sensíveis ao toque com base em seu comportamento e marcadores de superfície. Em seguida, usando análise de imagem guiada por IA e microdisseção a laser, cortaram com precisão apenas as células de interesse. Cada amostra minúscula — até uma fração de um único neurônio — foi processada em um espectrômetro de massa ultrasensível que identificou e quantificou milhares de proteínas. Essa abordagem produziu perfis proteicos ricos para cada subtipo de neurônio, revelando “impressões digitais” moleculares distintas que concordaram com, mas também ampliaram, mapas de expressão gênica anteriores.
Diversidade das células da dor escrita em proteínas
Os pesquisadores descobriram que cada subtipo de nociceptor carrega um conjunto central estável de proteínas, além de sua própria assinatura única. Nociceptores peptidérgicos e não peptidérgicos — duas classes de células de dor reconhecidas há muito tempo — mostraram diferenças claras em canais iônicos, moléculas de sinalização e vias metabólicas. Muitas proteínas já conhecidas por estarem relacionadas à dor apareceram, mas também surgiram candidatos menos familiares que marcaram fortemente um subtipo em relação ao outro. Importante, quando a equipe comparou neurônios em cultura com neurônios ainda embutidos no tecido espinhal, a maioria das proteínas se sobrepôs. Isso sugere que neurônios em cultura, um recurso comum na pesquisa da dor, preservam em grande parte sua identidade in vivo ao nível proteico, tornando-os um modelo confiável para explorar como as vias da dor funcionam.
Como a inflamação “dessilencia” fibras de dor
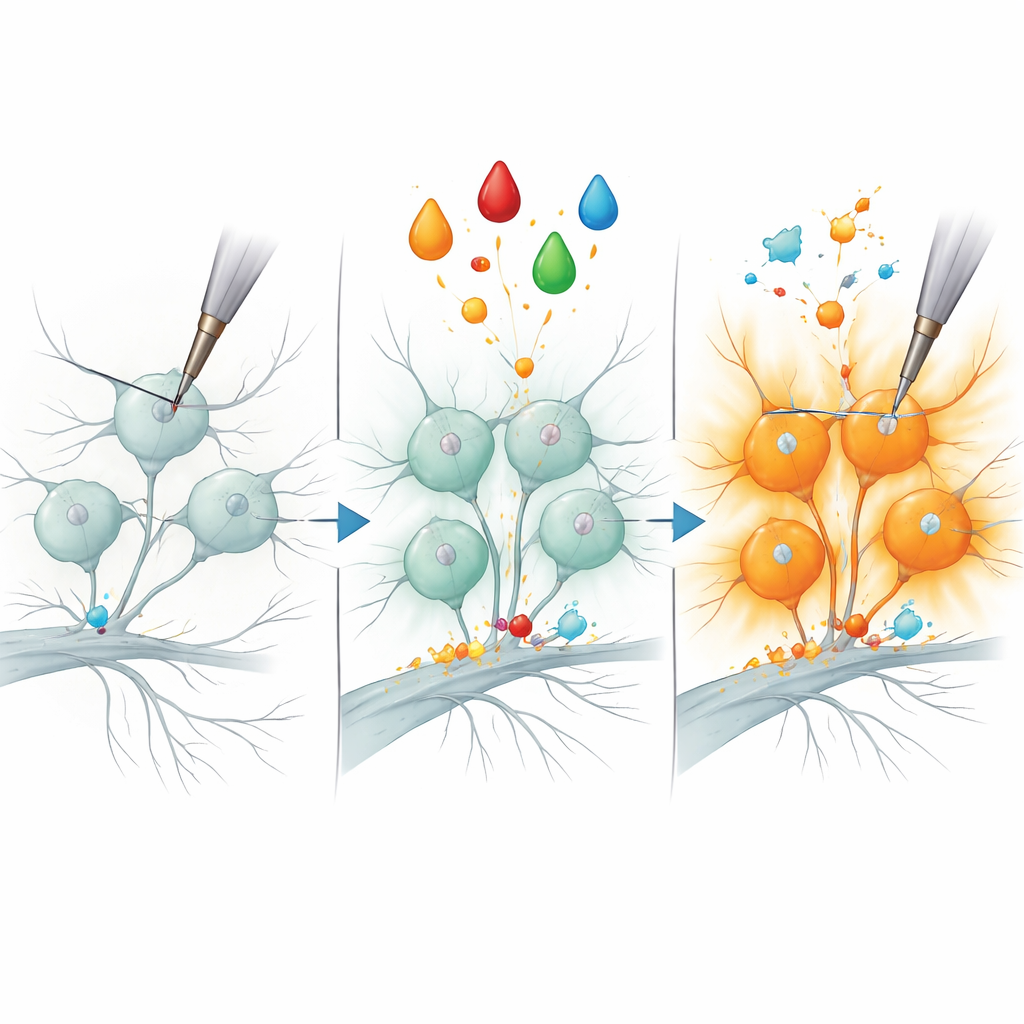
O estudo então se concentrou em um cenário clássico de dor: a sensibilização inflamatória. Em animais e humanos, um fator de crescimento chamado NGF pode tornar certos nociceptores dramaticamente mais sensíveis a estímulos mecânicos, um processo pensado para contribuir com a sensibilidade de pele ou articulações inflamadas. Os autores imitaram isso banhando neurônios em cultura com NGF mais um ativador de quinase de proteína, transformando nociceptores peptidérgicos previamente silenciosos em respondentes robustos à indentação mecânica. Comparando os perfis proteicos de células tratadas e não tratadas, detectaram um pequeno conjunto de proteínas cujos níveis aumentaram especificamente em nociceptores peptidérgicos sensibilizados. Uma enzima, B3GNT2, que ajuda a adicionar cadeias de açúcar a outras moléculas, despontou como uma candidata particularmente forte.
Uma nova alça molecular para a dor
Para testar se B3GNT2 é mais que um mero espectador, a equipe reduziu sua produção em nociceptores usando RNA interferente pequeno e então repetiu o tratamento inflamatório. Notavelmente, muito menos neurônios se tornaram mecanicamente responsivos, sugerindo que essa enzima é necessária para o “dessilenciamento” de certas fibras de dor. Embora outras características da sensibilização provavelmente dependam de proteínas adicionais, esse resultado liga uma enzima específica modificadora de açúcares ao início rápido da hipersensibilidade mecânica. Como variações no gene humano B3GNT2 têm sido associadas a condições inflamatórias dolorosas, o trabalho posiciona essa proteína — e as modificações de açúcar que ela realiza — como um novo e promissor ângulo para entender e, eventualmente, tratar a dor crônica.
Citação: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
Palavras-chave: nociceptores, proteômica, dor crônica, neurônios sensoriais, fator de crescimento nervoso