Clear Sky Science · it
La proteomica visiva profonda scopre la diversità dei nocicettori e bersagli del dolore
Perché contano le piccolissime cellule che avvertono il dolore
Il dolore è uno dei sistemi di allarme più importanti del corpo, eppure non tutte le cellule nervose che rilevano il dolore si comportano allo stesso modo. Alcune rispondono al calore, altre a pizzicamenti o pressione, e alcune rimangono silenti finché un danno o un’infiammazione non le “sveglia”. Questo studio esplora in profondità le proteine effettive presenti nei singoli neuroni nocicettivi di topo per capire cosa li distingue l’uno dall’altro — e per individuare nuovi interruttori molecolari che potrebbero essere bersagliati per alleviare il dolore cronico.
Uno sguardo ravvicinato ai messaggeri del dolore del corpo
Fasci di cellule nervose sensoriali nella colonna vertebrale, chiamati gangli della radice dorsale, inviano al cervello informazioni su tatto, temperatura e danno. All’interno di questi fasci esistono molti sottotipi neuronali, inclusi i nocicettori specializzati nel rilevare stimoli dannosi. Ricerche precedenti avevano utilizzato l’RNA, il manuale d’istruzioni della cellula, per mappare questa diversità. Ma l’RNA racconta solo una parte della storia: suggerisce quali proteine potrebbero esistere, non quali siano effettivamente presenti e attive. Sono le proteine, non i geni, a determinare come un neurone spara e come percepiamo il dolore. Gli autori si sono posti l’obiettivo di costruire una mappa dettagliata a livello proteico dei diversi tipi di neuroni sensoriali, includendo due grandi sottogruppi nocicettivi e i meccanorecettori sensibili al tatto.
Trasformare le immagini in cataloghi di proteine
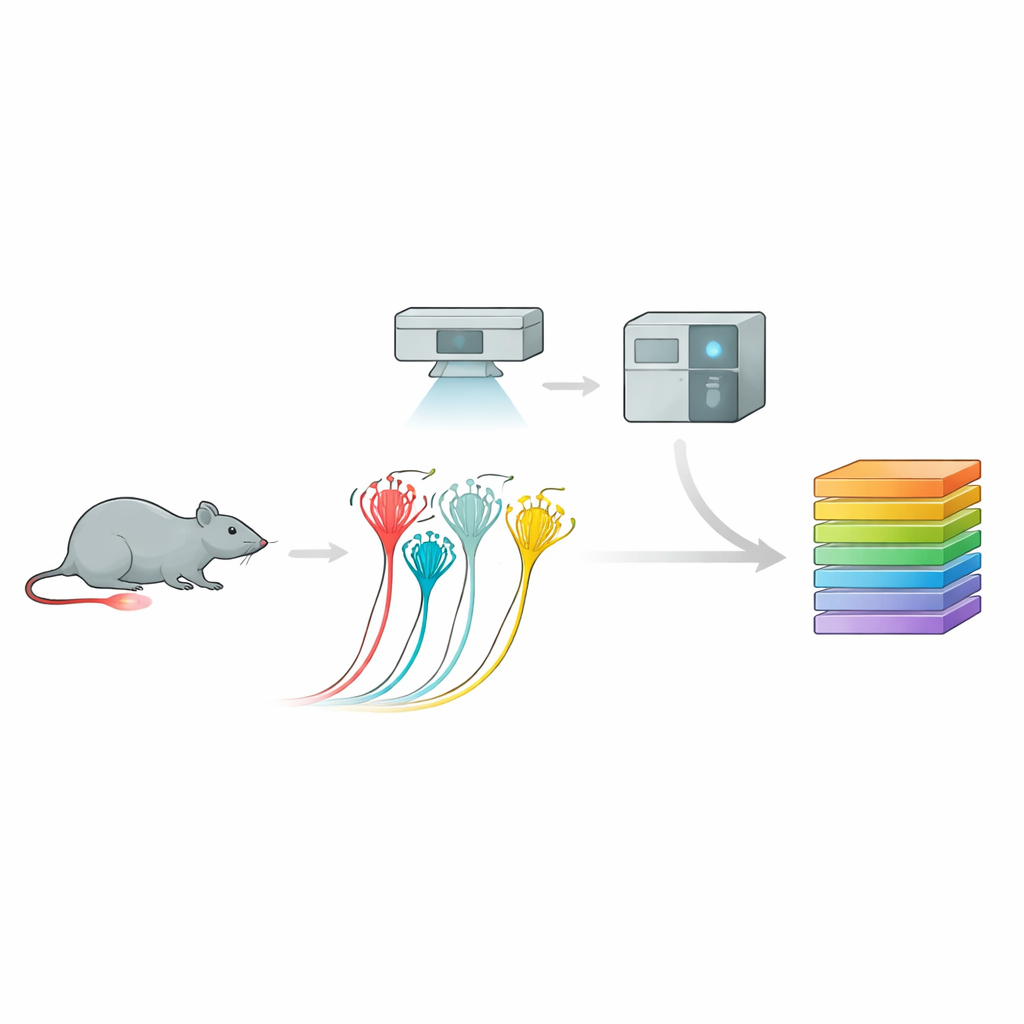
Per farlo, il team ha utilizzato una pipeline potente chiamata proteomica visiva profonda. Innanzitutto hanno coltivato neuroni sensoriali murini in coltura e registrato le loro risposte elettriche alla pressione, distinguendo nocicettori peptidergici, nocicettori non peptidergici e neuroni più grandi sensibili al tatto in base al comportamento e ai marcatori di superficie. Poi, con analisi d’immagine guidata dall’intelligenza artificiale e microdissezione laser, hanno ritagliato con precisione solo le cellule d’interesse. Ogni minuscolo campione — fino a una frazione di singolo neurone — è stato analizzato con uno spettrometro di massa ultrasensibile che ha identificato e quantificato migliaia di proteine. Questo approccio ha prodotto profili proteici ricchi per ogni sottotipo neuronale, rivelando “impronte” molecolari distinte che corrispondevano in gran parte, ma estendevano anche, le mappe precedenti basate sull’espressione genica.
La diversità delle cellule del dolore scritta nelle proteine
I ricercatori hanno scoperto che ogni sottotipo di nocicettore porta con sé un set centrale stabile di proteine, oltre a una propria firma unica. Nocicettori peptidergici e non peptidergici — due classi di cellule del dolore riconosciute da tempo — hanno mostrato differenze chiare nei canali ionici, nelle molecole di segnalazione e nei percorsi metabolici. Molte proteine già note per il loro ruolo nel dolore sono emerse, ma anche candidati meno familiari che marcavano con forza un sottotipo rispetto a un altro. Importante, confrontando i neuroni in coltura con quelli ancora incorporati nel tessuto spinale, la maggior parte delle proteine si sovrapponeva. Ciò suggerisce che i neuroni in coltura, pilastro della ricerca sul dolore, conservano in gran parte la loro identità in vivo a livello proteico, rendendoli un modello affidabile per esplorare il funzionamento delle vie del dolore.
Come l’infiammazione “riattiva” le fibre del dolore
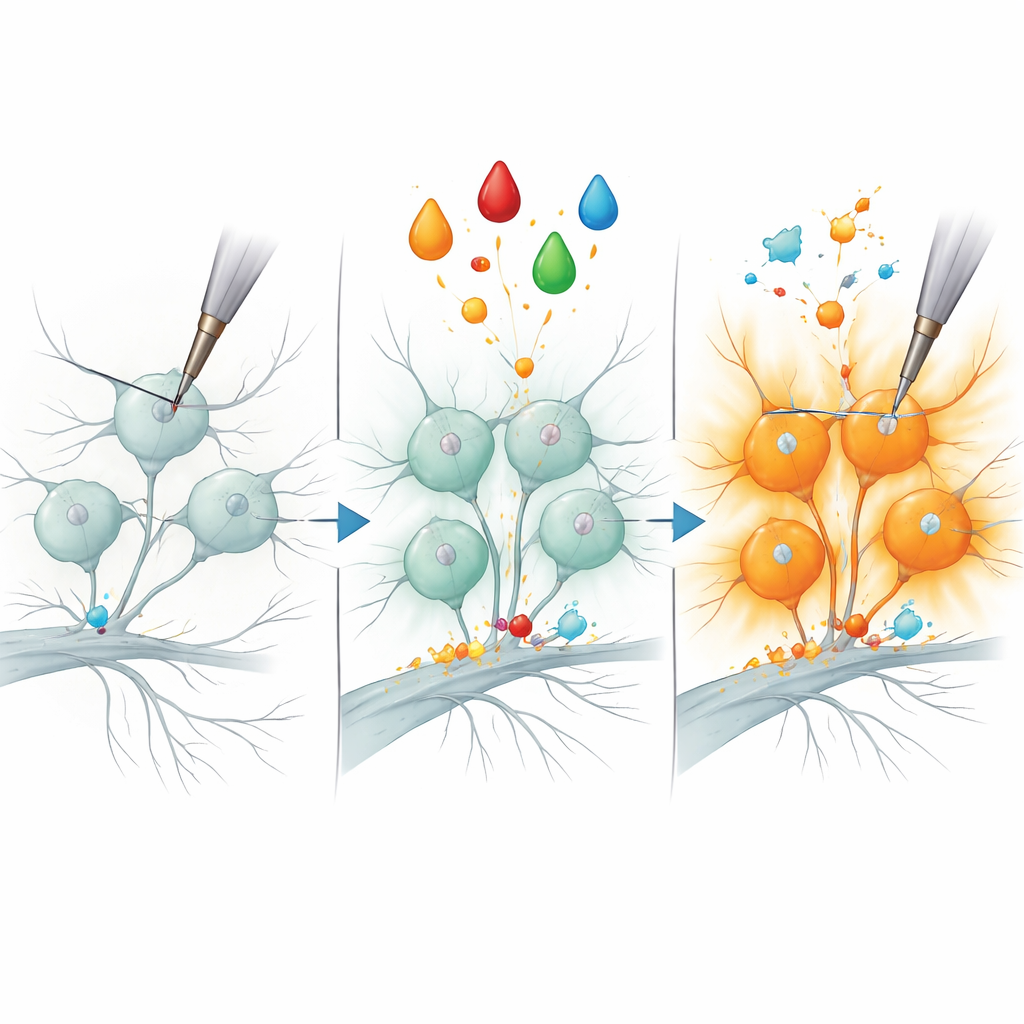
Lo studio si è poi concentrato su uno scenario classico del dolore: la sensibilizzazione infiammatoria. In animali e persone, un fattore di crescita chiamato NGF può rendere certi nocicettori molto più sensibili agli stimoli meccanici, un processo ritenuto contribuire alla tenerezza della pelle o delle articolazioni infiammate. Gli autori hanno mimato questo condizionando i neuroni in coltura con NGF più un attivatore delle chinasi proteiche, trasformando nocicettori peptidergici precedentemente silenti in rispondenti robusti all’indentazione meccanica. Confrontando i profili proteici delle cellule trattate e non trattate, hanno rilevato un piccolo set di proteine i cui livelli aumentavano specificamente nei nocicettori peptidergici sensibilizzati. Un enzima, B3GNT2, che aiuta ad aggiungere catene di zuccheri ad altre molecole, è emerso come un candidato particolarmente forte.
Una nuova leva molecolare sul dolore
Per verificare se B3GNT2 è più di un semplice spettatore, il team ha ridotto la sua produzione nei nocicettori usando RNA interferente e ha poi ripetuto il trattamento infiammatorio. In modo sorprendente, molte meno cellule sono diventate meccanicamente reattive, suggerendo che questo enzima è necessario per il “riattivarsi” di certe fibre del dolore. Sebbene altre caratteristiche della sensibilizzazione dipendano probabilmente da proteine addizionali, questo risultato collega un enzima specifico che modifica zuccheri all’insorgenza rapida dell’ipersensibilità meccanica. Poiché variazioni del gene umano B3GNT2 sono state associate a condizioni infiammatorie dolorose, il lavoro pone questa proteina — e le modifiche zuccherine che compie — come un nuovo e promettente angolo per comprendere e, in prospettiva, trattare il dolore cronico.
Citazione: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
Parole chiave: nocicettori, proteomica, dolore cronico, neuroni sensoriali, fattore di crescita nervoso