Clear Sky Science · tr
Derin görsel proteomik, nosiseptör çeşitliliğini ve ağrı hedeflerini ortaya çıkarıyor
Neden küçük ağrı algılayıcı hücreler önemli?
Ağrı, vücudun en önemli uyarı sistemlerinden biridir; ancak tüm ağrı algılayan sinir hücreleri aynı şekilde davranmaz. Bazıları ısıya, bazıları sıkışma veya basınca yanıt verir; bazıları ise yaralanma veya iltihaplandıklarında “uyanana” kadar sessiz kalır. Bu çalışma, fare ağrı algılayıcı nöronlarının içindeki gerçek proteinleri tek tek inceleyerek bunları birbirinden ayıran özellikleri anlamayı—ve kronik ağrıyı hafifletmek için hedeflenebilecek yeni moleküler anahtarları belirlemeyi—amaçlıyor.
Vücudun ağrı haber taşıyıcılarına daha yakından bakış
Dorsal kök ganglionları adı verilen omurilikteki duyu nöron demetleri, dokunma, sıcaklık ve yaralanma ile ilgili bilgileri beyne iletir. Bu demetlerin içinde zararlı uyaranları algılamaya uzmanlaşmış nosiseptörler de dahil olmak üzere birçok nöron alt türü bulunur. Önceki araştırmalar bu çeşitliliği haritalamak için hücrenin talimat kitabı olan RNA’yı kullanmıştı. Ancak RNA yalnızca hikâyenin bir kısmını anlatır: hangi proteinlerin olabileceğine işaret eder, hangilerinin gerçekten mevcut ve aktif olduğunu göstermez. Nihayetinde bir nöronun ateşlenme biçimini ve ağrıyı nasıl hissettiğimizi proteinler, genler değil, şekillendirir. Yazarlar farklı duyu nöron tiplerinin ayrıntılı bir protein düzeyi haritasını çıkarmayı; iki ana ağrı algılayıcı alt grubunu ve dokunmaya duyarlı mekanoreseptörleri içerecek şekilde hedeflediler.
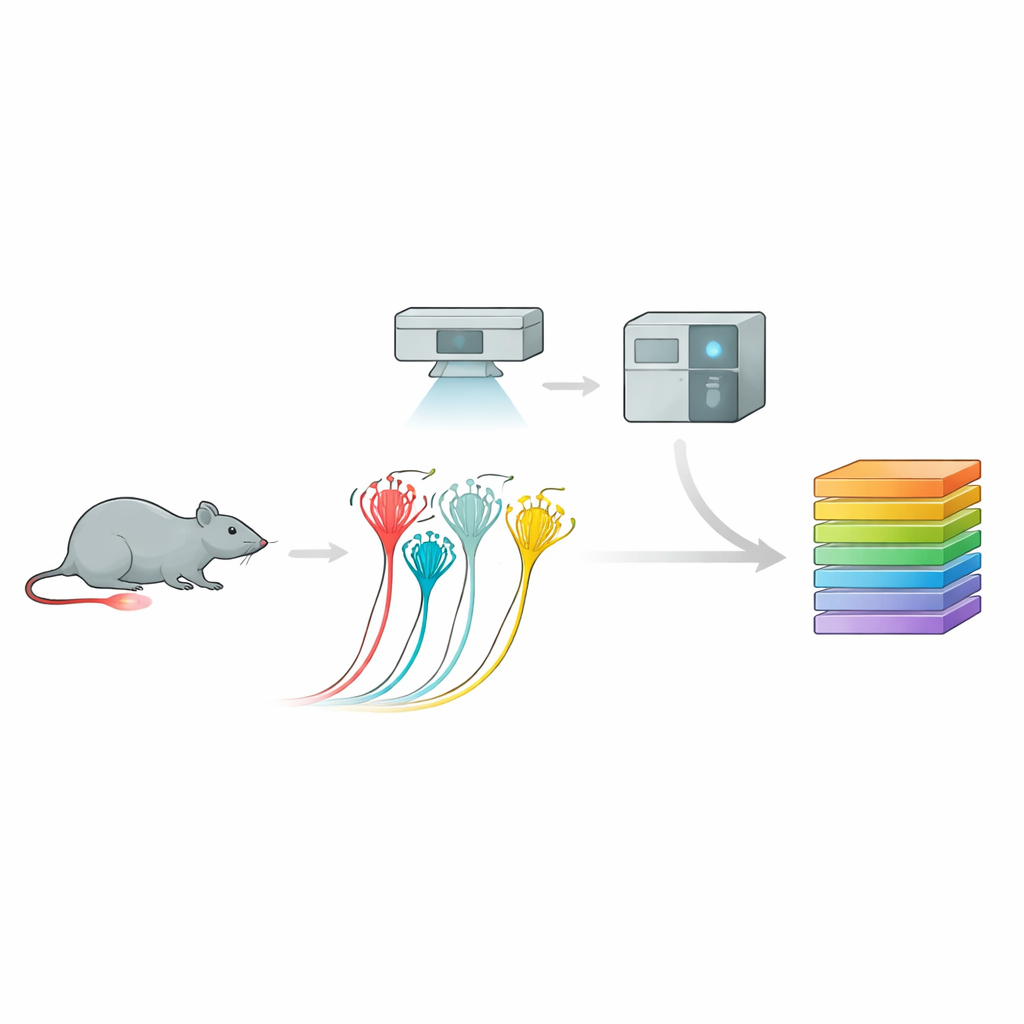
Görüntüleri protein kataloglarına çevirme
Bunu yapmak için ekip, derin görsel proteomik adı verilen güçlü bir boru hattı kullandı. Önce fare duyu nöronlarını kültürde yetiştirdiler ve basınca karşı elektriksel yanıtlarını kaydederek davranışları ve yüzey belirteçlerine göre peptiderjik nosiseptörleri, peptiderjik olmayan nosiseptörleri ve daha büyük dokunmaya duyarlı nöronları ayırt ettiler. Ardından yapay zekâ destekli görüntü analizi ve lazer mikrodiseksiyon kullanarak yalnızca ilgilenilen hücreleri hassas biçimde kestiler. Tek bir nöronun bir kesrinin bile altındaki her küçük örnek, binlerce proteini tanımlayan ve nicelendirip raporlayan ultrasensitif bir kütle spektrometresine verildi. Bu yaklaşım, her nöron alt türü için zengin protein profilleri üreterek, önceki gen ifadesi haritalarıyla iyi örtüşen ancak onları aynı zamanda genişleten belirgin moleküler “parmak izleri” ortaya çıkardı.
Proteinlerde yazılmış ağrı hücresi çeşitliliği
Araştırmacılar, her nosiseptör alt türünün sabit bir çekirdek protein setine sahip olduğunu ve buna ek olarak kendi benzersiz imzasını taşıdığını buldu. Uzun süredir tanınan iki ağrı hücresi sınıfı olan peptiderjik ve peptiderjik olmayan nosiseptörler, iyon kanalları, sinyal molekülleri ve metabolik yollar açısından belirgin farklılıklar gösterdi. Birçok bilinen ağrıyla ilişkili protein ortaya çıkarken, bir alt türü diğerinden güçlü biçimde ayıran daha az tanıdık adaylar da belirdi. Önemli olarak, ekip kültürdeki nöronları omurilik dokusunda hâlâ gömülü haldeki nöronlarla karşılaştırdığında çoğu proteinin örtüştüğünü gördü. Bu, ağrı araştırmalarında sıkça kullanılan kültürdeki nöronların protein düzeyinde büyük ölçüde beden içindeki kimliklerini koruduğunu ve ağrı yolaklarının nasıl çalıştığını araştırmak için güvenilir bir model sunduğunu öne sürüyor.
İltihaplanma nasıl ağrı liflerini “sessizlikten çıkarır”?
Çalışma daha sonra klasik bir ağrı senaryosuna odaklandı: inflamatuar duyarlılık artışı. Hem hayvanlarda hem de insanlarda NGF adı verilen bir büyüme faktörü, belirli nosiseptörleri mekanik uyaranlara karşı dramatik biçimde daha hassas hale getirebilir; bunun iltihaplı deri veya eklem hassasiyetine katkıda bulunduğu düşünülür. Yazarlar bunu, kültürdeki nöronları NGF ile artı bir protein kinaz aktivatörüyle muamele ederek taklit ettiler; daha önce sessiz olan peptiderjik nosiseptörler mekanik indente karşı güçlü yanıt veren hücrelere dönüştü. Muamele görmüş ve görmemiş hücrelerin protein profillerini karşılaştırdıklarında, özellikle duyarlı hale gelmiş peptiderjik nöronlarda düzeyi artan küçük bir protein seti tespit ettiler. Diğer moleküllere şeker zincirleri eklemeye yardımcı olan B3GNT2 adlı bir enzim, özellikle güçlü bir aday olarak öne çıktı.
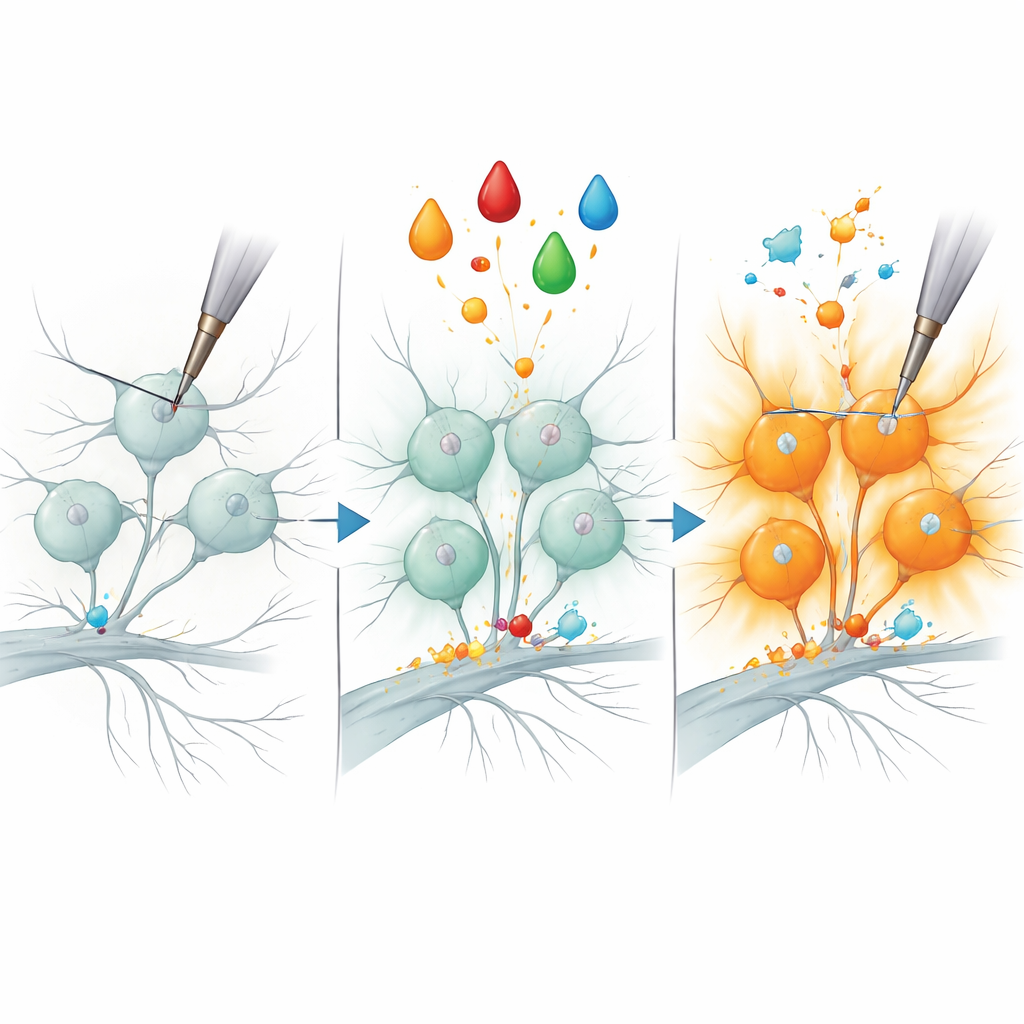
Ağrı üzerinde yeni bir moleküler tutamaç
B3GNT2’nin sadece bir yoldaş olup olmadığını sınamak için ekip, küçük interferans RNA kullanarak nosiseptörlerde bu enzimin üretimini azalttı ve ardından inflamatuar muameleyi tekrarladı. Çarpıcı biçimde, mekanik olarak yanıt veren nöron sayısı çok daha az oldu; bu da bu enzimin belirli ağrı liflerinin “sessizlikten çıkarılması” için gerekli olduğunu düşündürmektedir. Duyarlılığın diğer özelliklerinin muhtemelen ek proteinlere bağlı olması beklenirken, bu sonuç hızla ortaya çıkan mekanik aşırı duyarlılıkla spesifik bir şeker-modifiye edici enzimi ilişkilendiriyor. İnsan B3GNT2 genindeki varyasyonların ağrılı inflamatuar durumlarla ilişkilendirilmiş olması nedeniyle, bu çalışma bu proteini—ve onun gerçekleştirdiği şeker modifikasyonlarını—kronik ağrıyı anlamak ve nihayetinde tedavi etmek için umut verici yeni bir açı olarak konumlandırıyor.
Atıf: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
Anahtar kelimeler: nosiseptörler, proteomik, kronik ağrı, duyu nöronları, sinir büyüme faktörü