Clear Sky Science · he
פרוטאומיקה חזותית עמוקה חושפת שונות בנוציספטורים ומטרות לכאב
מדוע תאים זעירים החשים בכאב חשובים
הכאב הוא אחד ממערכות האזהרה החשובות של הגוף, ובכל זאת לא כל תאי העצב החשים בכאב פועלים באותו אופן. חלקם מגיבים לחום, אחרים לנקישה או ללחץ, וחלק נשארים שקטים עד שפציעה או דלקת "מעיר" אותם. המחקר הזה חופר לעומק את החלבונים שבתוך נוירוני העכבר החשים בכאב ברמת תא יחיד, כדי להבין מה מפריד ביניהם — ולזהות מתגים מולקולריים חדשים שעשויים לשמש מטרה להקלה על כאב כרוני.
מבט צמוד על שליחי הכאב של הגוף
בולטים של תאי עצב סנסוריים בעמוד השדרה, הקרויים גנגליונים של שורש גבי, מעבירים מידע על מגע, טמפרטורה ופציעה אל המוח. בתוך הבולטים האלו יש תת־סוגים רבים של נוירונים, כולל נוציספטורים שמתמחים בזיהוי גירויים מזיקים. מחקרים קודמים השתמשו ב־RNA, מדריך ההוראות של התא, כדי למפות את המגוון הזה. אבל RNA מספר רק חלק מהסיפור: הוא מרמז אילו חלבונים עשויים להיות קיימים, לא אילו מהם נמצאים בפועל ומופעלים. החלבונים, לא הגנים, הם אלה שמעצבים בסופו של דבר כיצד הנוירון יורה וכיצד אנו חשים בכאב. המחברים שאפו לבנות מפת חלבונים מפורטת של סוגי נוירונים סנסוריים שונים, כולל שתי תת־קבוצות עיקריות החושבות בכאב ונוירונים מכאנורצפטיביים רגישי מגע.
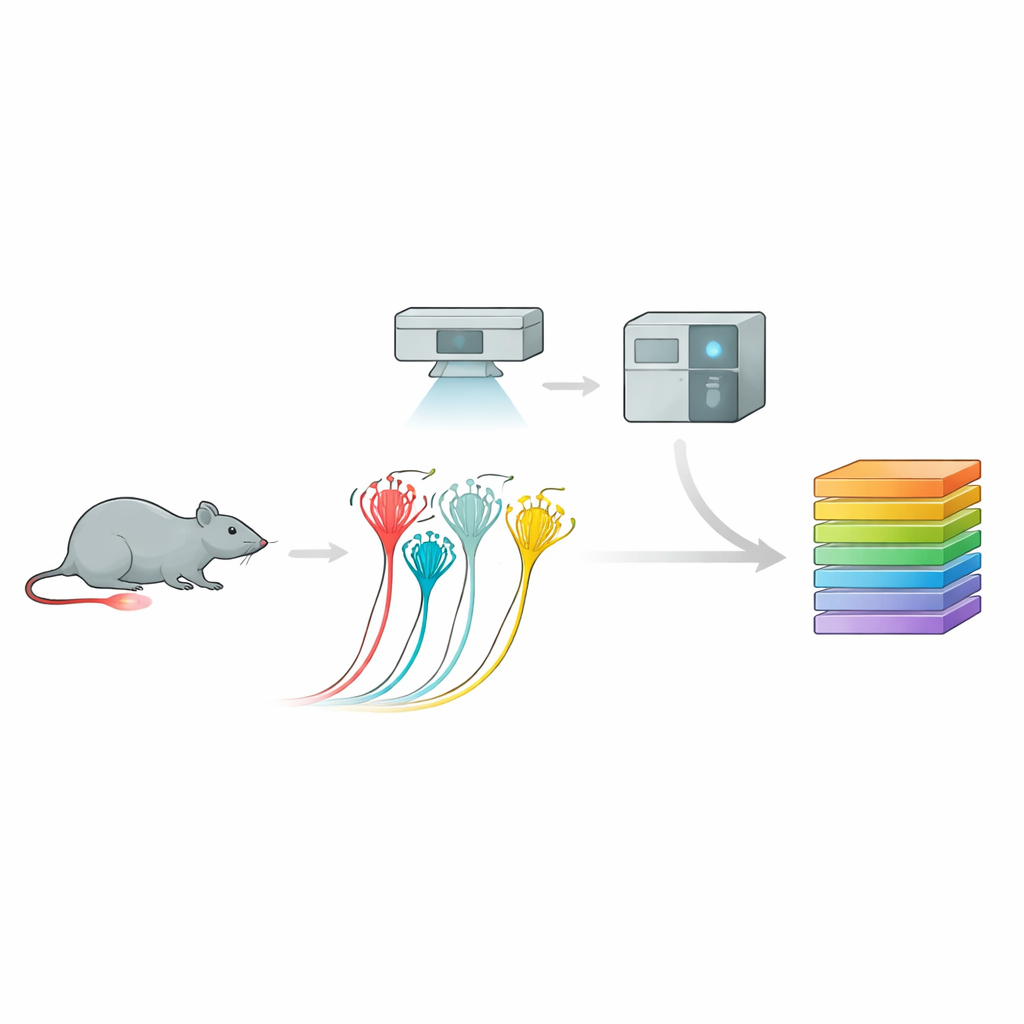
הפיכת תמונות לרשימות חלבוניים
לעשות זאת, הצוות השתמש בצינור עבודה עוצמתי שנקרא פרוטאומיקה חזותית עמוקה. ראשית, הם גידלו נוירונים סנסוריים של עכבר בתרביות והקלטו את התגובות החשמליות שלהם ללחץ, תוך הבחנה בין נוציספטורים פפטידרגיים, נוציספטורים לא־פפטידרגיים ונוירונים גדולים רגישי מגע בהתבסס על התנהגות וסמנים سطحיים. לאחר מכן, באמצעות ניתוח תמונה מונחה בינה מלאכותית וחתוך מיקרו־לייזר, הם גזרו בדיוק רק את התאים הרלוונטיים. כל דגימה זעירה — עד חלק מתא בודד — הוזנה למספר מסה רגיש ביותר שזיהה וכימות אלפי חלבונים. גישה זו ייצרה פרופילים חלבוניים עשירים לכל תת־סוג נוירון, וחשפה "טביעות אצבע" מולקולריות מובחנות שתאמו במידה רבה אך גם הרחיבו את מפת ביטוי הגנים הקודמת.
שונות תאי הכאב כתובה בחלבונים
החוקרים מצאו שלכל תת־סוג נוציספטור יש סט ליבה יציב של חלבונים, בנוסף לחתימה ייחודית משלו. נוציספטורים פפטידרגיים ולא־פפטידרגיים — שתי כיתות של תאי כאב המוכרות זמן רב — הראו הבדלים ברורים בתעלות יון, במולקולות איתות ובנתיבי מטבוליזם. רבים מהחלבונים הידועים כקשורים לכאב הופיעו, אך הופיעו גם מועמדים פחות מוכרים שסימנו בעוצמה תת־סוג אחד על פני אחר. באופן חשוב, כאשר הצוות השווה בין נוירונים בתרבית לנוירונים שעדיין מוטמעים ברקמת עמוד השדרה, רוב החלבונים חופפו. ממצא זה מרמז כי נוירונים בתרבית, המשמשים רבות במחקר הכאב, שומרים במידה רבה על זהותם בגוף ברמת החלבון, מה שהופך אותם למודל אמין לחקירת אופן פעולת מסלולי הכאב.
כיצד דלקת "מבטלת השתקה" של סיבי הכאב
המחקר התרכז לאחר מכן בתרחיש כאב קלאסי: רגישות דלקתית. ביצורים ובאנשים, גורם גדילה הנקרא NGF יכול להפוך נוציספטורים מסוימים לרגישים באופן דרמטי לגירויים מכאניים — תהליך הנחשב לתרום לרגישות בעור או במפרקים מדוללים. המחברים חיקו זאת על ידי אמבטיית נוירונים בתרבית ב־NGF בתוספת פעיל של קינאז חלבון, וכך הפכו נוציספטורים פפטידרגיים שקטים קודם לכן למגיבים עזים להטבעה מכאנית. בהשוואת הפרופילים החלבוניים של תאים מטופלים ולא מטופלים, הם גילו סט קטן של חלבונים שרמותיהם עלו באופן ספציפי בנוציספטורים פפטידרגיים מרגישים. אנזים אחד, B3GNT2, המסייע בהוספת שרשראות סוכר למולקולות אחרות, התגלה כמועמד בולט במיוחד.
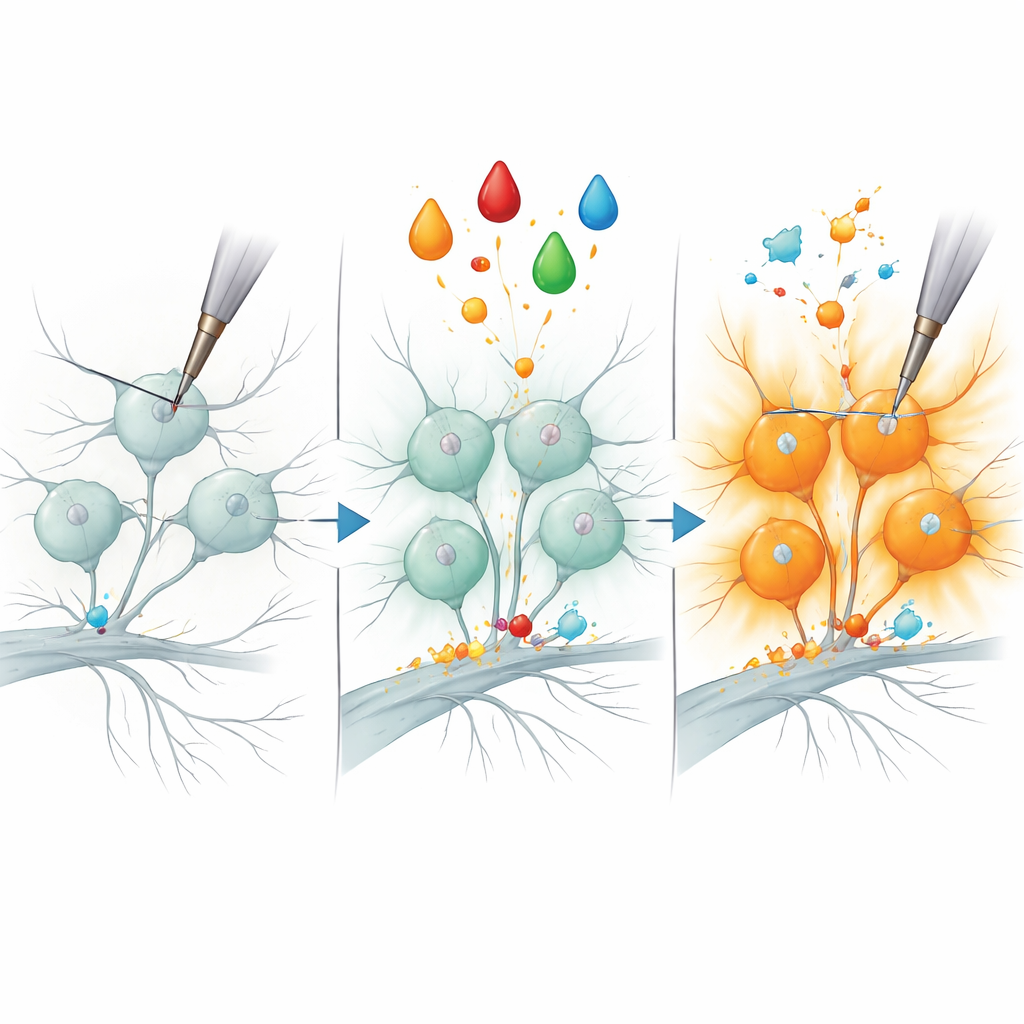
יד מולקולרית חדשה על הכאב
כדי לבדוק האם B3GNT2 הוא יותר מסתם צופה מהצד, הצוות הפחית את ייצורו בנוציספטורים באמצעות RNA מתערב קטן ואז חזר על הטיפול הדלקתי. באופן מרשים, הרבה פחות נוירונים הפכו לרגישים מכאנית, מה שמרמז כי אנזים זה נדרש ל"ביטול ההשתקה" של סיבי כאב מסוימים. בעוד שתכונות נוספות של הרגישות כנראה תלויות בחלבונים נוספים, תוצאה זו מקשרת אנזים ספציפי המשנה סוכרים להופעה המהירה של רגישות מכאנית מוגברת. מכיוון ששינויים בגֵן האנושי B3GNT2 הובחנו כקשורים למצבים דלקתיים כואבים, הממצא מציב את החלבון הזה — ואת התיקונים הסוכריים שהוא מבצע — כזווית מבט מבטיחה להבנה ובהמשך לטיפול בכאב כרוני.
ציטוט: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
מילות מפתח: נוֹציצפטורים, פרוטאומיקה, כאב כרוני, נוירונים סנסוריים, גורם גדילה עצבי