Clear Sky Science · nl
Diepe visuele proteomica onthult diversiteit van nociceptoren en pijn‑doelen
Waarom kleine pijn‑gevoelige cellen ertoe doen
Pijn is een van de belangrijkste waarschuwingssystemen van het lichaam, maar niet alle pijn‑gevoelige zenuwcellen gedragen zich hetzelfde. Sommige reageren op warmte, andere op knijpen of druk, en sommige blijven stil totdat een verwonding of ontsteking ze “waakt”. Deze studie onderzoekt diepgaand de feitelijke eiwitten in individuele muizencellen die pijn waarnemen om te begrijpen wat hen van elkaar onderscheidt — en om nieuwe moleculaire schakelaars te identificeren die mogelijk kunnen worden gericht om chronische pijn te verlichten.
Een nadere blik op de boodschappers van pijn
Bundels sensorische zenuwcellen in de wervelkolom, dorsale ganglia genaamd, sturen informatie over aanraking, temperatuur en letsel naar de hersenen. Binnen deze bundels zijn veel neuronale subtypes, waaronder nociceptoren die gespecialiseerd zijn in het detecteren van schadelijke prikkels. Eerder onderzoek gebruikte RNA, het instructieboek van de cel, om deze diversiteit in kaart te brengen. Maar RNA vertelt slechts een deel van het verhaal: het geeft aan welke eiwitten mogelijk bestaan, niet welke daadwerkelijk aanwezig en actief zijn. Eiwitten, niet genen, bepalen uiteindelijk hoe een neuron vuurt en hoe we pijn ervaren. De auteurs wilden een gedetailleerde kaart op eiwitniveau maken van verschillende typen sensorische neuronen, waaronder twee belangrijke pijn‑waarnemende subgroepen en aanraking‑gevoelige mechanoreceptoren.
Beelden omzetten in eiwitcatalogi
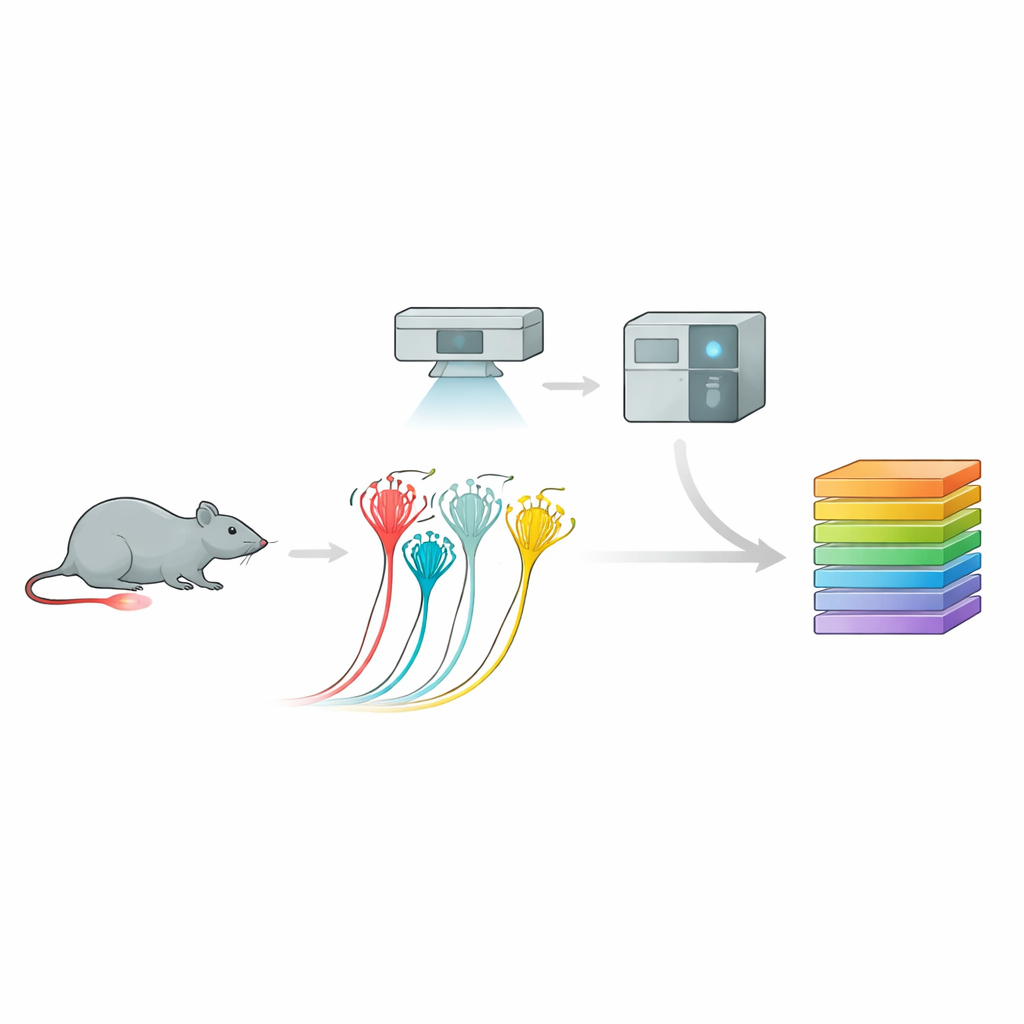
Daartoe gebruikte het team een krachtige pijplijn genaamd diepe visuele proteomica. Eerst kweekten ze muizensensorische neuronen in cultuur en registreerden hun elektrische reacties op druk, waarmee ze peptiderge nociceptoren, niet‑peptiderge nociceptoren en grotere aanraking‑gevoelige neuronen konden onderscheiden op basis van gedrag en oppervlaktekenmerken. Vervolgens sneden ze met behulp van AI‑gestuurde beeldanalyse en laser‑microdissectie precies de gewenste cellen uit. Elk minuscuul monster — tot een fractie van een enkele neuron — werd in een ultrasensitieve massaspectrometer gevoerd die duizenden eiwitten identificeerde en kwantificeerde. Deze aanpak leverde rijke eiwitprofielen op voor elk neuron‑subtype, die onderscheidende moleculaire “vingerafdrukken” onthulden die goed overeenkwamen met, maar ook verder gingen dan, eerdere gen‑expressiekaarten.
Pijndiversiteit geschreven in eiwitten
De onderzoekers vonden dat elk nociceptor‑subtype een stabiele kernset eiwitten draagt, plus een eigen unieke signatuur. Peptiderge en niet‑peptiderge nociceptoren — twee lang herkende pijncelklassen — toonden duidelijke verschillen in ionkanalen, signaalmoleculen en metabole paden. Veel bekende pijngerelateerde eiwitten kwamen naar voren, maar ook minder bekende kandidaten die sterk één subtype markeerden. Belangrijk is dat, wanneer het team gecultiveerde neuronen vergeleek met neuronen die nog ingebed waren in wervelweefsel, de meeste eiwitten overlappenden. Dit suggereert dat gecultiveerde neuronen, een hoeksteen van pijnonderzoek, grotendeels hun identiteit uit het lichaam behouden op eiwitniveau, waardoor ze een betrouwbaar model vormen om te onderzoeken hoe pijnpaden werken.
Hoe ontsteking pijnvezels “onsilenceert”
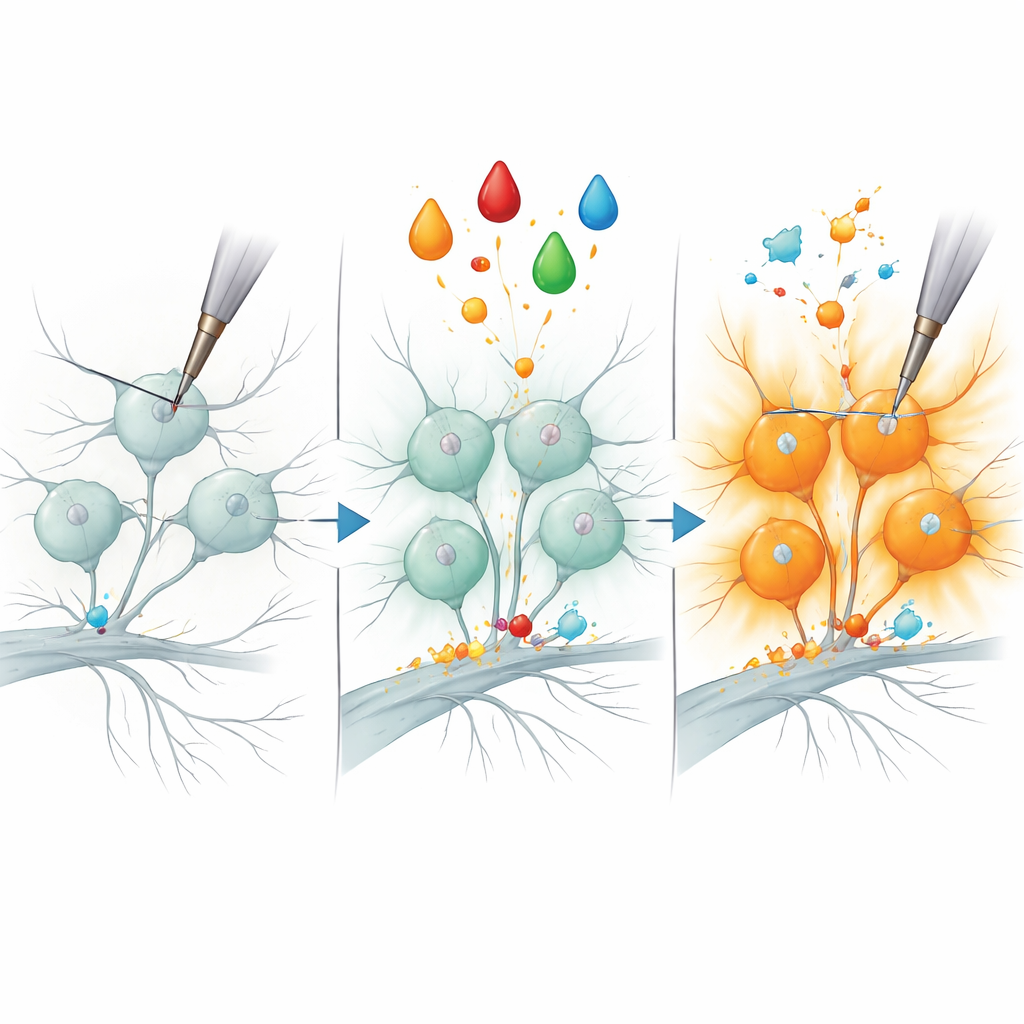
De studie zoomde vervolgens in op een klassiek pijnscenario: inflammatoire sensitivering. Bij dieren en mensen kan een groeifactor genaamd NGF bepaalde nociceptoren veel gevoeliger maken voor mechanische prikkels, een proces dat wordt verondersteld bij te dragen aan de gevoeligheid van ontstoken huid of gewrichten. De auteurs imiteerden dit door gecultiveerde neuronen te behandelen met NGF plus een eiwitkinaas‑activator, waardoor eerder stille peptiderge nociceptoren veranderden in sterke reageerders op mechanische indentering. Door de eiwitprofielen van behandelde en onbehandelde cellen te vergelijken, ontdekten ze een kleine set eiwitten waarvan de niveaus specifiek stegen in gesensitiseerde peptiderge neuronen. Eén enzym, B3GNT2, dat helpt bij het toevoegen van suikerketens aan andere moleculen, kwam naar voren als een bijzonder sterke kandidaat.
Een nieuw moleculair handvat voor pijn
Om te testen of B3GNT2 meer is dan een passant, verminderde het team de productie ervan in nociceptoren met behulp van kleine interfererende RNA’s en herhaalden vervolgens de inflammatoire behandeling. Opvallend werd een veel kleiner aantal neuronen mechanisch responsief, wat suggereert dat dit enzym nodig is voor het “onsilencen” van bepaalde pijnvezels. Hoewel andere kenmerken van sensitivering waarschijnlijk afhangen van aanvullende eiwitten, koppelt dit resultaat een specifiek suiker‑modificerend enzym aan het snelle ontstaan van mechanische hypersensitiviteit. Omdat variaties in het menselijke B3GNT2‑gen zijn geassocieerd met pijnlijke ontstekingsaandoeningen, positioneert dit werk dit eiwit — en de suikerwijzigingen die het uitvoert — als een veelbelovende nieuwe invalshoek voor het begrijpen en mogelijk behandelen van chronische pijn.
Bronvermelding: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
Trefwoorden: nociceptoren, proteomica, chronische pijn, sensorische neuronen, zenuwgroeifactor