Clear Sky Science · ar
البروتيوميات البصرية المتعمقة تكشف تنوّع مستقبلات الألم وأهداف الألم
لماذا تهمّ خلايا الحسّ بالألم الدقيقة
الألم هو واحد من أهم أنظمة التحذير في الجسم، ومع ذلك لا تتصرف كل الخلايا العصبية المستقبلة للألم بنفس الطريقة. فبعضها يستجيب للحرارة، وبعضها للقرص أو الضغط، وبعضها يبقى صامتًا حتى «يوقظه» الضرر أو الالتهاب. تتعمق هذه الدراسة في البروتينات الفعلية داخل خلايا ألم مفردة من الفئران لفهم ما يميّزها عن بعضها البعض—ولتحديد مفاتيح جزيئية جديدة يمكن استهدافها لتخفيف الألم المزمن.
نظرة أقرب على رسولّي الألم في الجسم
حزم من الخلايا العصبية الحسية في العمود الفقري، تُسمى العقد الجذرية الظهرية، تنقل معلومات حول اللمس والحرارة والضرر إلى الدماغ. داخل هذه الحزم توجد العديد من الأنواع الفرعية من الخلايا العصبية، بما في ذلك مستقبلات الألم المتخصّصة في اكتشاف المحفزات الضارة. استخدمت أبحاث سابقة الرنا، دليل التعليمات الخلوية، لرسم هذا التنوع. لكن الرنا يروي جزءًا فقط من القصة: فهو يشير إلى البروتينات التي قد تتواجد، لا إلى تلك الموجودة والفعّالة فعليًا. البروتينات، وليس الجينات، هي التي تشكّل في النهاية كيفية إطلاق الخلية العصبية للنبضات وكيف نشعر بالألم. هدف المؤلفين كان بناء خريطة مفصّلة على مستوى البروتين لأنواع الخلايا العصبية الحسية المختلفة، بما في ذلك مجموعتين رئيسيتين للشعور بالألم ومستقبلات ميكانيكية حسّاسة لللمس.
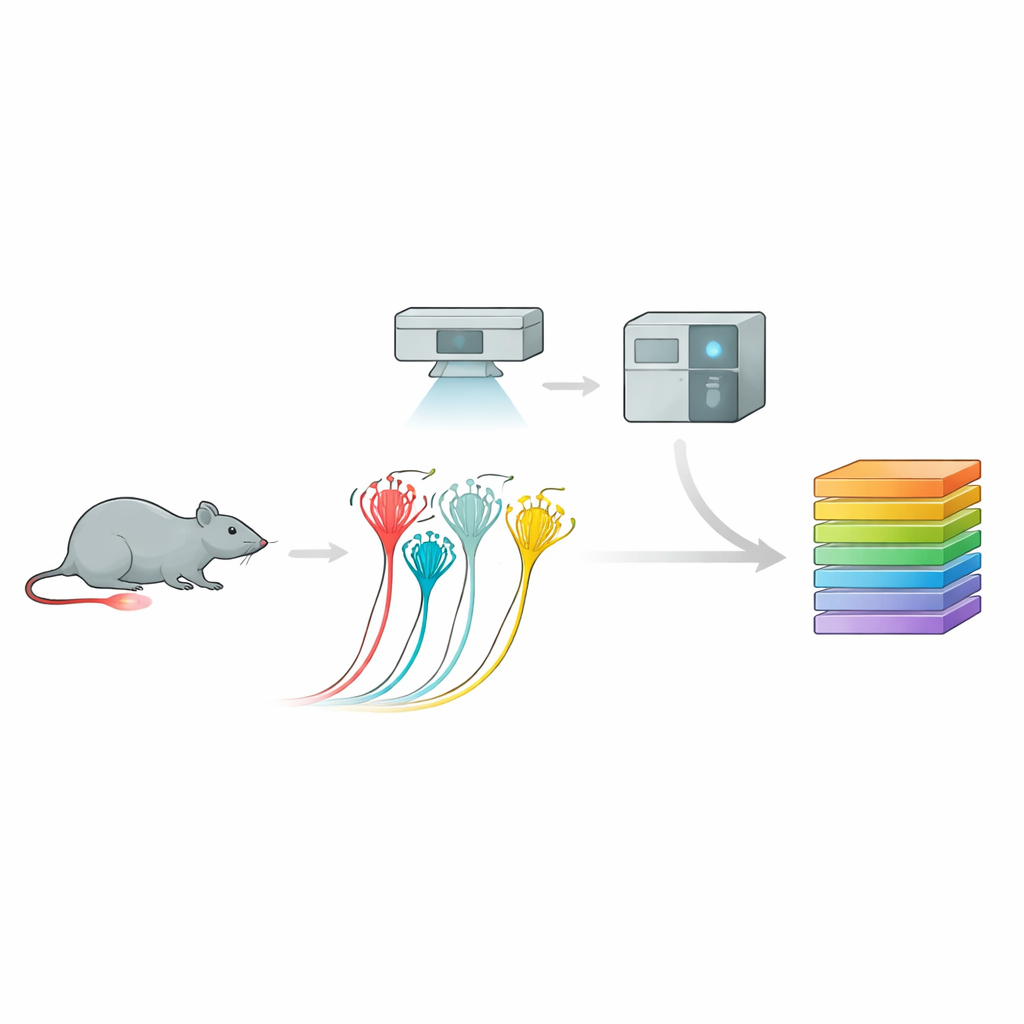
تحويل الصور إلى فهارس للبروتينات
للقيام بذلك، استخدمت المجموعة سلسلة أدوات قوية تُدعى البروتيوميات البصرية المتعمقة. أولًا، زرعوا خلايا عصبية حسية من الفئران في ثقافات وسجلوا استجابتها الكهربائية للضغط، مميزين مستقبلات الألم الببتيدية وغير الببتيدية، والخلايا الأكبر الحساسة للمس وفقًا لسلوكها وعلاماتها السطحية. ثم، باستخدام تحليل صور موجه بالذكاء الاصطناعي وتشريح ليزري دقيق، قطعوا بدقة فقط الخلايا المطلوبة. كل عيّنة صغيرة—حتى أجزاء من خلية عصبية واحدة—وُضعت في مطياف كتلي شديد الحساسية حدد وكمّى آلاف البروتينات. أنتج هذا النهج ملفات بروتينية غنية لكل نوع فرعي من الخلايا العصبية، كاشفًا عن «بصمات» جزيئية مميزة تتوافق جيدًا مع، لكن تتجاوز أيضًا، خرائط التعبير الجيني السابقة.
تنوع خلايا الألم مكتوب في البروتينات
وجد الباحثون أن كل نوع فرعي من مستقبلات الألم يحمل مجموعة أساسية مستقرة من البروتينات، بالإضافة إلى توقيعه الفريد الخاص. أظهرت المستقبلات الببتيدية وغير الببتيدية—وهي فئتان معروفتان منذ زمن—فروقات واضحة في قنوات الأيونات، وجزيئات الإشارة، والمسارات الأيضية. ظهرت العديد من البروتينات المعروفة المرتبطة بالألم، كما ظهرت مرشّحات أقل شهرة تميّز نوعًا فرعيًا عن آخر بقوة. والأهم من ذلك، عندما قارن الفريق الخلايا المزروعة بالخلايا المضمنة بعدم في نسيج العمود الفقري، تداخلت معظم البروتينات. وهذا يشير إلى أن الخلايا المزروعة، وهي مرجع في أبحاث الألم، تحافظ إلى حد كبير على هويتها داخل الجسم على مستوى البروتين، مما يجعلها نموذجًا موثوقًا لاستكشاف كيفية عمل مسارات الألم.
كيف «يفكّ الالتزام الصامت» للليفات الألمية الالتهاب
ثم ركزت الدراسة على سيناريو ألم كلاسيكي: التحسّس الالتهابي. لدى الحيوانات والبشر، يمكن لعامل نمو يُدعى NGF أن يجعل بعض مستقبلات الألم أكثر حساسية للمحفزات الميكانيكية بصورة كبيرة، وهي عملية يُعتقد أنها تساهم في حساسية الجلد أو المفاصل الملتهبة. قلّد المؤلفون ذلك عن طريق حمّام خلايا مزروعة بعامل NGF بالإضافة إلى مُنشّط كيناز بروتيني، محوّلين مستقبلات الألم الببتيدية الصامتة سابقًا إلى مستجيبات قوية للاقتباس الميكانيكي. من خلال مقارنة الملفات البروتينية للخلايا المعالجة وغير المعالجة، رصدوا مجموعة صغيرة من البروتينات ارتفعت مستوياتها خاصة في المستقبلات الببتيدية المستثارة. برز إنزيم واحد، B3GNT2، الذي يساعد على إضافة سلاسل سكرية إلى جزيئات أخرى، كمرشح قوي خصوصًا.
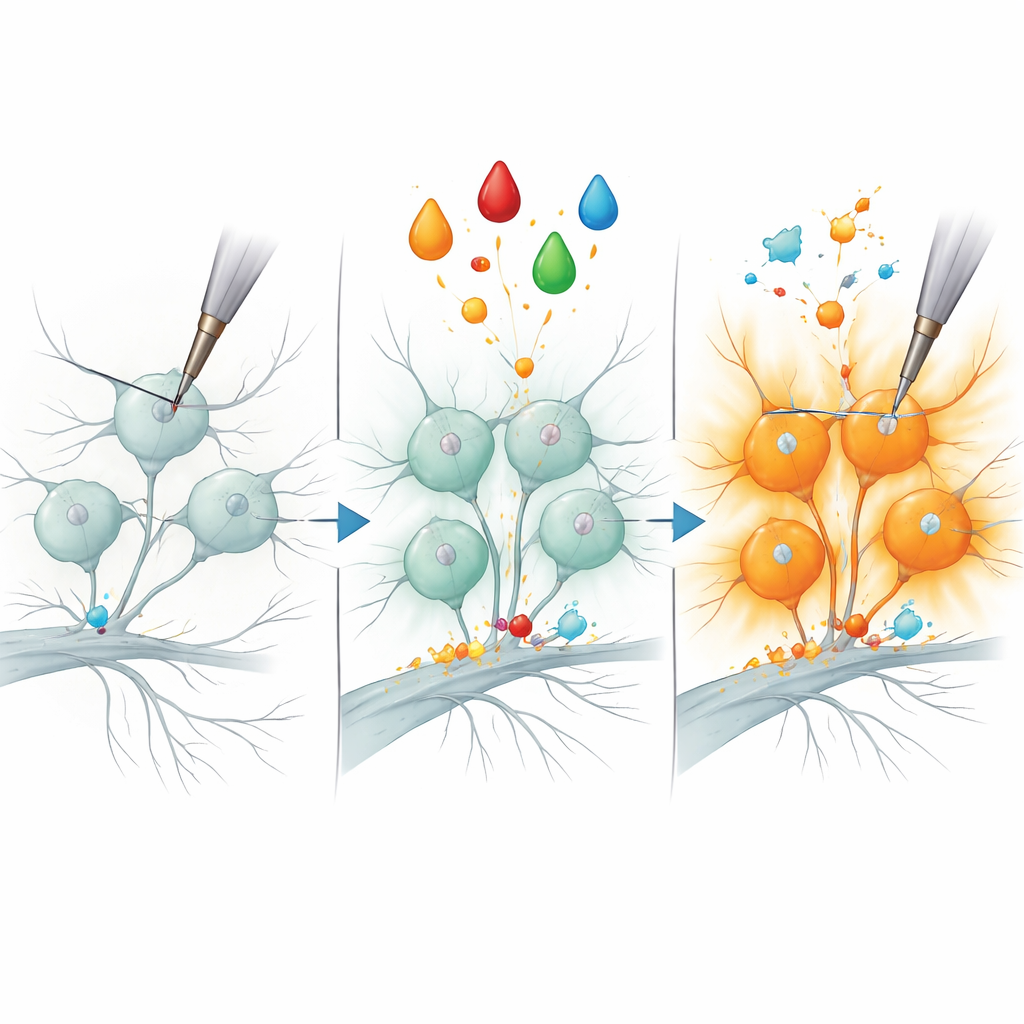
مقبض جزيئي جديد للألم
لاختبار ما إذا كان B3GNT2 أكثر من مجرد مرافق، قلّل الفريق من إنتاجه في مستقبلات الألم باستخدام رنا متداخل صغير ثم كرّر المعالجة الالتهابية. بشكل لافت، أصبح عدد أقل بكثير من الخلايا العصبية مستجيبًا ميكانيكيًا، ما يشير إلى أن هذا الإنزيم مطلوب لـ«إلغاء صمت» بعض الألياف المؤلمة. بينما تعتمد سمات أخرى من التحسّس على بروتينات إضافية على الأرجح، تربط هذه النتيجة إنزيمًا محددًا معدِّلًا للسكر ببدء فرط الحساسية الميكانيكية السريع. وبما أن تباينات في جين B3GNT2 البشري رُبطت بحالات التهابية مؤلمة، تضع هذه الدراسة هذا البروتين—والتعديلات السكرية التي يؤديها—كزاوية واعدة لفهم وعلاج الألم المزمن مستقبلاً.
الاستشهاد: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
الكلمات المفتاحية: مستقبلات الألم, البروتيوميات, الألم المزمن, الخلايا العصبية الحسية, عامل نمو الأعصاب