Clear Sky Science · pl
Głęboka wizualna proteomika ujawnia różnorodność nocyceptorów i cele bólowe
Dlaczego małe komórki czujące ból mają znaczenie
Ból jest jednym z najważniejszych systemów ostrzegawczych organizmu, jednak nie wszystkie komórki nerwowe wykrywające ból zachowują się tak samo. Niektóre reagują na ciepło, inne na szczypanie lub ucisk, a niektóre pozostają ciche, dopóki uraz lub zapalenie ich nie „obudzą”. To badanie zagląda głęboko w białka występujące w pojedynczych mysich neuronach czuciowych, aby zrozumieć, co je od siebie odróżnia — i wskazać nowe molekularne przełączniki, które mogłyby być celem terapii łagodzących ból przewlekły.
Uważniejsze spojrzenie na przekaźniki bólu w organizmie
Pęczki neuronów czuciowych w kręgosłupie, zwane zwojami rdzeniowymi grzbietowymi, przesyłają do mózgu informacje o dotyku, temperaturze i urazie. W tych pęczkach występuje wiele podtypów neuronów, w tym nocyceptory specjalizujące się w wykrywaniu bodźców szkodliwych. Wcześniejsze badania wykorzystywały RNA, instrukcję komórkową, do mapowania tej różnorodności. RNA daje jednak tylko część obrazu: sugeruje, jakie białka mogą istnieć, ale nie mówi, które z nich są faktycznie obecne i aktywne. To białka, a nie geny, ostatecznie kształtują sposób, w jaki neuron wyzwala impulsy i jak odczuwamy ból. Autorzy postanowili zbudować szczegółową mapę na poziomie białek różnych typów neuronów czuciowych, obejmującą dwie główne podgrupy nocyceptorów oraz mechanoreceptory wrażliwe na dotyk.
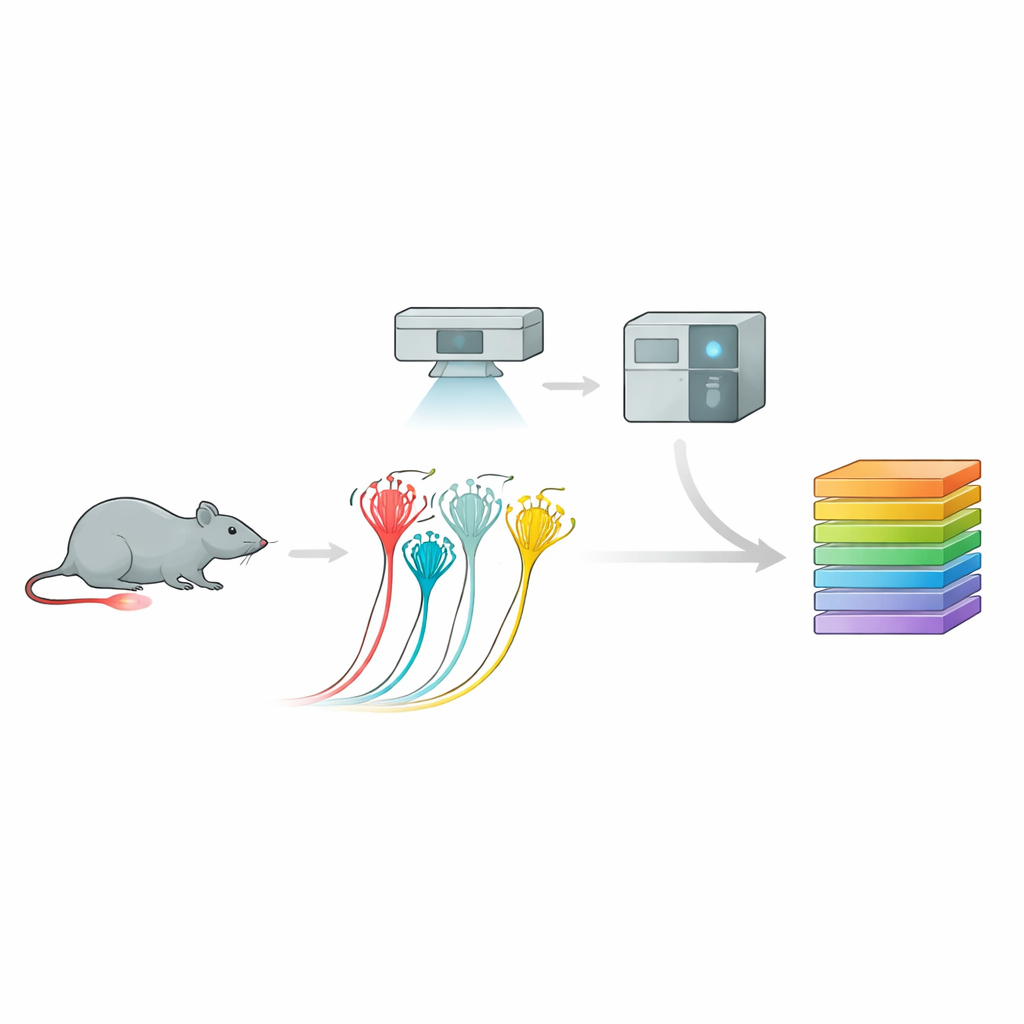
Przekształcanie obrazów w katalogi białek
Aby to osiągnąć, zespół zastosował potężny proces zwany głęboką wizualną proteomiką. Najpierw hodowali mysie neurony czuciowe w hodowli i rejestrowali ich odpowiedzi elektryczne na ucisk, rozróżniając nocyceptory peptydergiczne, nocyceptory niepeptydergiczne i większe neurony wrażliwe na dotyk na podstawie ich zachowania i markerów powierzchniowych. Następnie, przy użyciu analizy obrazów wspomaganej sztuczną inteligencją i mikrodysekcji laserowej, precyzyjnie wycinali tylko interesujące ich komórki. Każda maleńka próbka — sięgająca ułamka pojedynczego neuronu — była analizowana przez ultrasensytywny spektrometr mas, który identyfikował i kwantyfikował tysiące białek. To podejście dało bogate profile białkowe dla każdego podtypu neuronu, ujawniając odrębne molekularne „odciski palców”, które dobrze korelowały z wcześniejszymi mapami ekspresji genów, ale je także rozszerzały.
Różnorodność komórek bólowych zapisana w białkach
Naukowcy odkryli, że każdy podtyp nocyceptora ma stabilny zestaw jądrowych białek oraz własny unikatowy podpis. Nocyceptory peptydergiczne i niepeptydergiczne — dwa długo rozpoznawane klasy komórek bólowych — wykazywały wyraźne różnice w kanalach jonowych, cząsteczkach sygnałowych i szlakach metabolicznych. Pojawiło się wiele znanych białek związanych z bólem, ale także mniej znanych kandydatów, które wyraźnie wyróżniały jeden podtyp od drugiego. Co ważne, porównanie neuronów hodowanych w kulturze z neuronami nadal osadzonymi w tkance rdzeniowej wykazało dużą zbieżność białek. Sugeruje to, że neurony w hodowli, będące podstawowym modelem badań nad bólem, w dużym stopniu zachowują swoją tożsamość in vivo na poziomie białkowym, co czyni je wiarygodnym modelem do badania mechanizmów bólu.
Jak zapalenie „odcisza” włókna bólowe
Badanie skupiło się następnie na klasycznym scenariuszu bólowym: uwrażliwieniu zapalnym. Zarówno u zwierząt, jak i u ludzi, czynnik wzrostu nerwów (NGF) może znacząco zwiększać wrażliwość niektórych nocyceptorów na bodźce mechaniczne — proces uważany za przyczynę bolesności zapalonej skóry czy stawów. Autorzy odtworzyli to, kąpiąc neurony hodowane w NGF wraz z aktywatorem kinazy białkowej, co przemieniło wcześniej ciche nocyceptory peptydergiczne w silnie reagujące na mechaniczne wgłębienie. Porównując profile białkowe komórek traktowanych i nietraktowanych, wykryli niewielki zestaw białek, których poziomy podniosły się specyficznie w uwrażliwionych nocyceptorach peptydergicznych. Jednym z wyróżniających się kandydatów była enzym B3GNT2, który uczestniczy w dołączaniu łańcuchów cukrowych do innych cząsteczek.
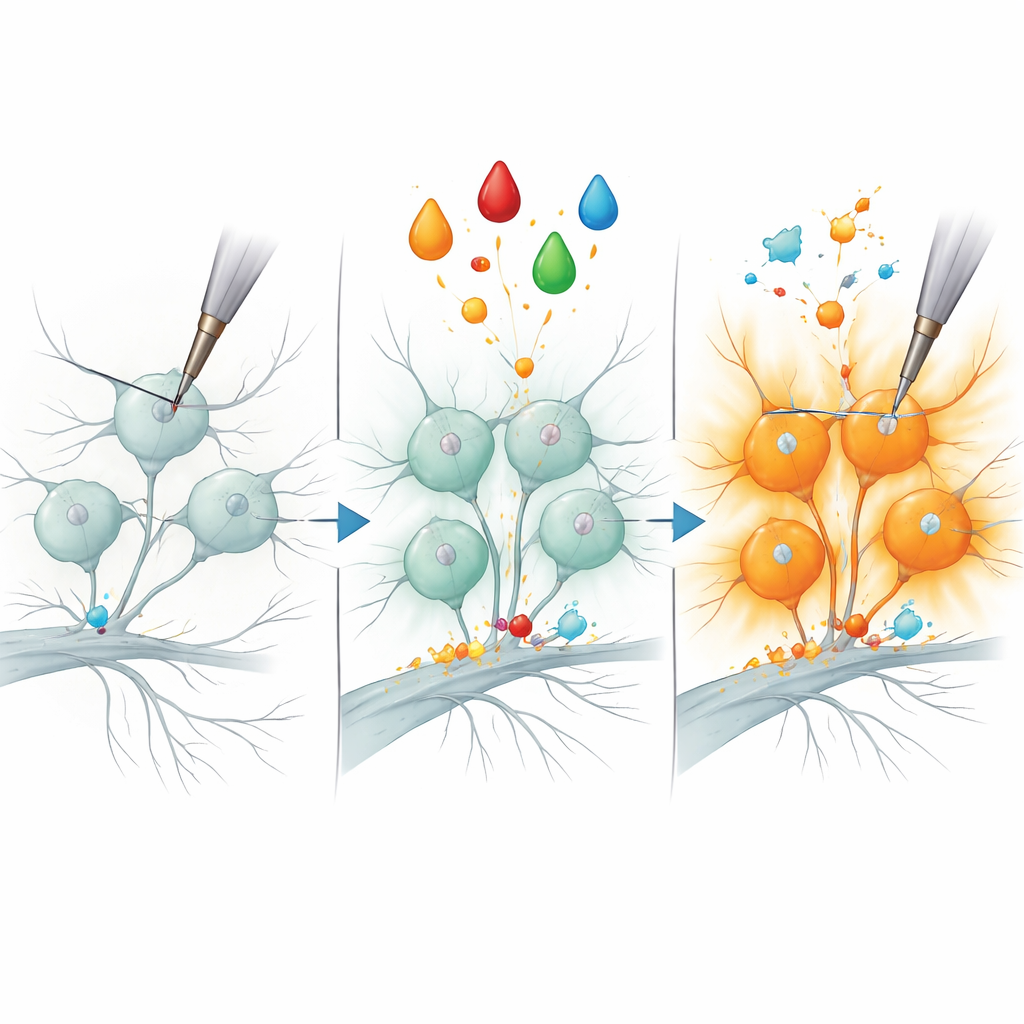
Nowy molekularny uchwyt na ból
Aby sprawdzić, czy B3GNT2 jest czymś więcej niż tylko towarzyszem procesu, zespół zmniejszył jego produkcję w nocyceptorach przy użyciu małych interferujących RNA, a następnie powtórzył leczenie zapalne. Co uderzające, znacznie mniej neuronów stało się mechanicznie reagujących, co sugeruje, że ten enzym jest wymagany do „odciszania” niektórych włókien bólowych. Chociaż inne elementy uwrażliwienia prawdopodobnie zależą od dodatkowych białek, wynik ten łączy konkretny enzym modyfikujący cukry z szybkim początkiem nadwrażliwości mechanicznej. Ponieważ warianty ludzkiego genu B3GNT2 zostały powiązane z bolesnymi stanami zapalnymi, praca ta stawia to białko — i przeprowadzane przez nie modyfikacje cukrowe — jako obiecujący nowy punkt widzenia w rozumieniu i potencjalnym leczeniu bólu przewlekłego.
Cytowanie: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
Słowa kluczowe: nocyceptory, proteomika, ból przewlekły, neurony czuciowe, czynnik wzrostu nerwów