Clear Sky Science · sv
Djup visuell proteomik avslöjar nociceptorernas mångfald och smärtmål
Varför små smärtsensoriska celler är viktiga
Smärta är ett av kroppens viktigaste varningssystem, men alla smärtsensoriska nervceller beter sig inte likadant. Vissa reagerar på värme, andra på nyp eller tryck, och några förblir tysta tills skada eller inflammation "väcker" dem. Denna studie går på djupet i de faktiska proteinerna inne i individuella mus-nociceptorer för att förstå vad som skiljer dem åt — och för att peka ut nya molekylära omkopplare som skulle kunna riktas för att lindra kronisk smärta.
Närmare titt på kroppens smärtbudbärare
Knippen av sensoriska nervceller i ryggraden, kallade dorsalrotsganglier, skickar information om beröring, temperatur och skada upp till hjärnan. Inom dessa knippen finns många neuron-subtyper, inklusive nociceptorer som specialiserar sig på att upptäcka skadliga stimuli. Tidigare forskning använde RNA, cellens instruktionsbok, för att kartlägga denna mångfald. Men RNA berättar bara en del av historien: det antyder vilka proteiner som kan finnas, inte vilka som faktiskt är närvarande och aktiva. Proteiner, inte gener, formar i slutändan hur en neuron fyrar och hur vi upplever smärta. Författarna ville bygga en detaljerad kartläggning på protein-nivå av olika sensoriska neuron-typer, inklusive två stora smärtsensoriska undergrupper och beröringskänsliga mekanoreceptorer.
Att omvandla bilder till proteinkataloger
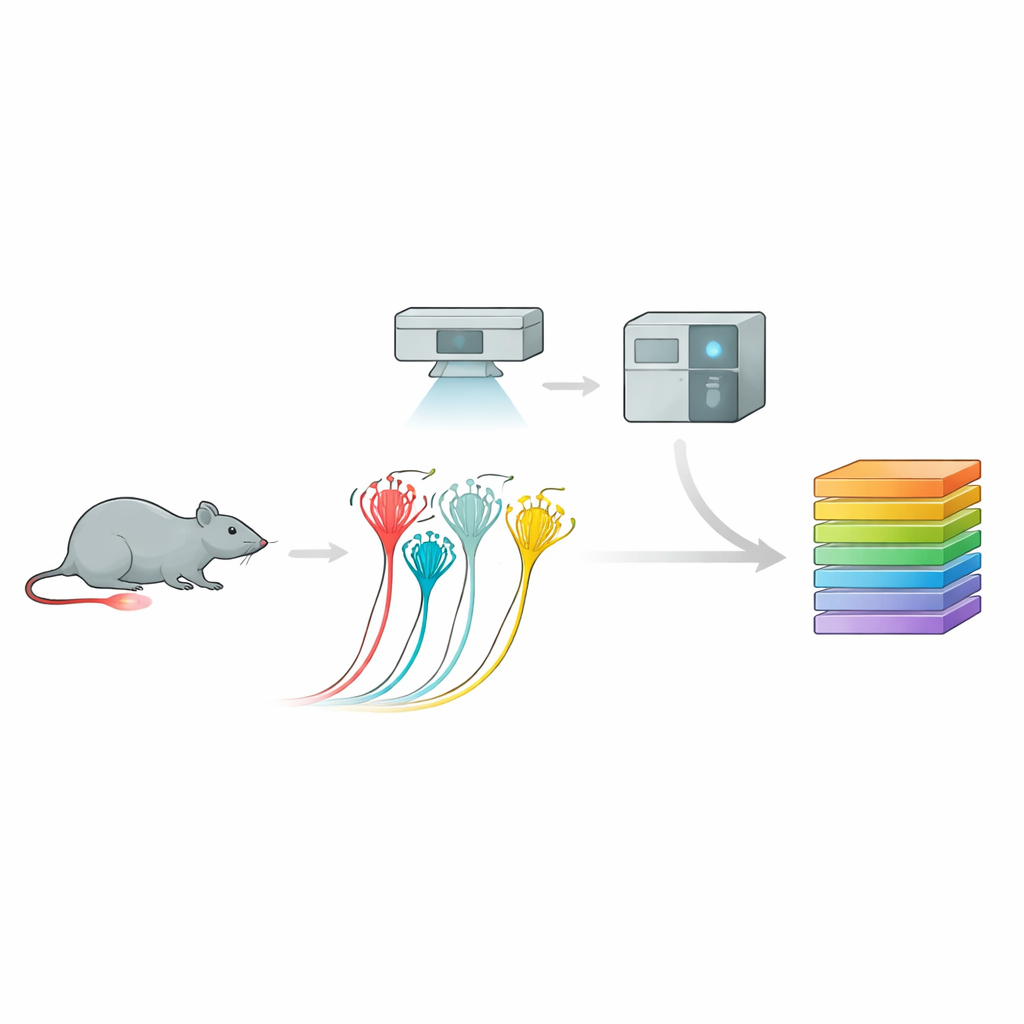
För att göra detta använde teamet en kraftfull pipeline kallad djup visuell proteomik. Först odlade de mus-sensoriska neuroner i kultur och registrerade deras elektriska svar på tryck, vilket gjorde det möjligt att skilja peptidergiska nociceptorer, icke-peptidergiska nociceptorer och större beröringskänsliga neuroner utifrån deras beteende och ytmärken. Sedan, med AI-styrd bildanalys och laser-mikrodissektion, skar de noggrant ut endast de celler som var av intresse. Varje litet prov — ner till en bråkdel av en enskild neuron — matades in i ett ultrasensitivt massespektrometer som identifierade och kvantifierade tusentals proteiner. Denna metod gav rika proteinprofiler för varje neuron-subtyp och avslöjade distinkta molekylära ”fingeravtryck” som stämde väl överens med, men också utökade, tidigare genuttryckskartor.
Smärtcellernas mångfald skriven i proteiner
Forskarnas resultat visade att varje nociceptor-subtyp bär på en stabil kärna av proteiner, plus en egen unik signatur. Peptidergiska och icke-peptidergiska nociceptorer — två länge erkända smärtcellsklasser — uppvisade tydliga skillnader i jonkanaler, signalmolekyler och metaboliska vägar. Många kända smärtrelaterade proteiner dök upp, men också mindre välkända kandidater som tydligt markerade den ena subtypen över den andra. Viktigt är att när teamet jämförde odlade neuroner med neuroner som fortfarande var inbäddade i ryggmärgsvävnad, överlappade de flesta proteiner. Det tyder på att odlade neuroner, ett huvudverktyg inom smärtforskning, till stor del bevarar sin identitet i kroppen på protein-nivå, vilket gör dem till en pålitlig modell för att utforska hur smärtbanor fungerar.
Hur inflammation "avtystar" smärtfibrer
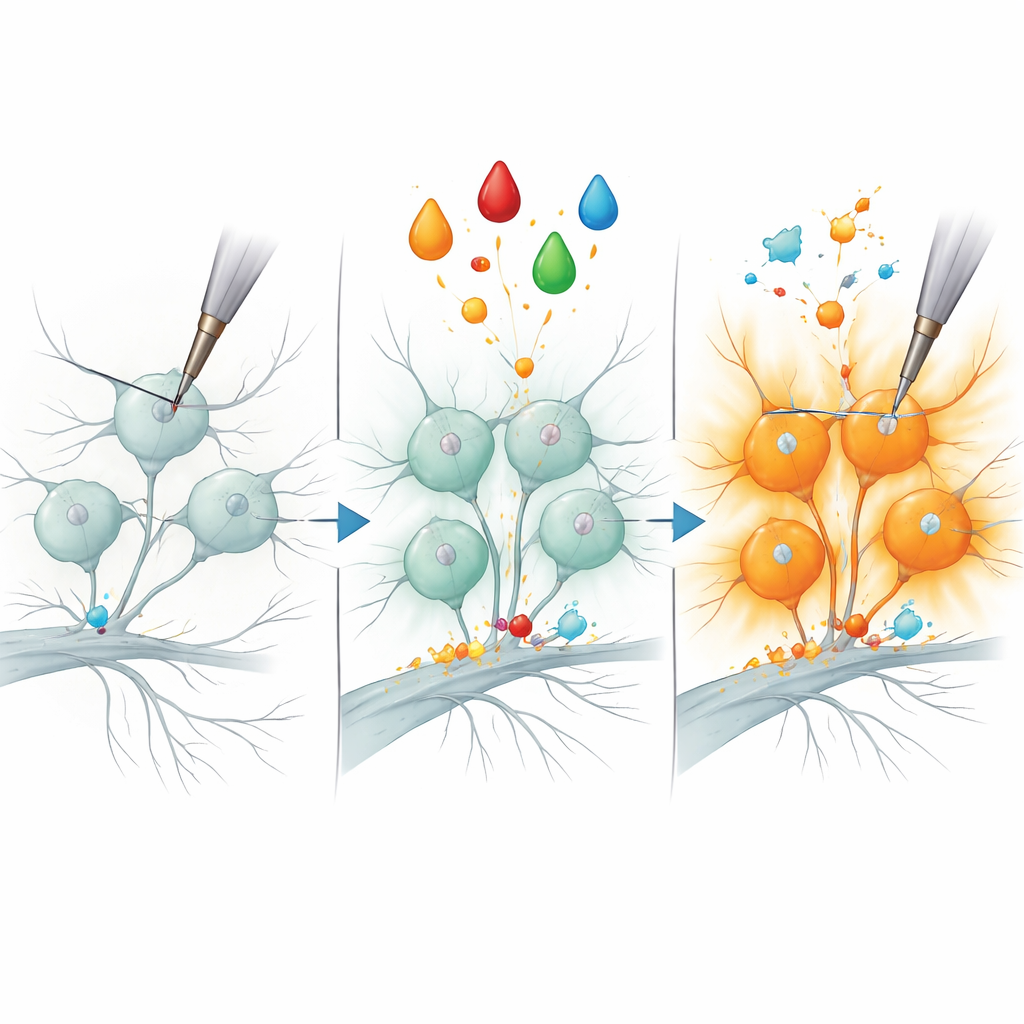
Studien zoomade sedan in på ett klassiskt smärtscenario: inflammatorisk sensibilisering. Hos både djur och människor kan en tillväxtfaktor kallad NGF göra vissa nociceptorer dramatiskt mer känsliga för mekaniska stimuli, en process som tros bidra till ömheten i inflammerad hud eller leder. Författarna efterliknade detta genom att bada odlade neuroner i NGF plus en protein-kinas-aktivator, vilket förvandlade tidigare tysta peptidergiska nociceptorer till starka reagerande på mekanisk indentation. Genom att jämföra proteinprofilerna hos behandlade och obehandlade celler upptäckte de en liten uppsättning proteiner vars nivåer steg specifikt i sensibiliserade peptidergiska neuroner. Ett enzym, B3GNT2, som hjälper till att fästa sockerkedjor på andra molekyler, framträdde som en särskilt stark kandidat.
En ny molekylär grepp om smärta
För att testa om B3GNT2 är mer än en bihandling minskade teamet dess produktion i nociceptorer med hjälp av små interfererande RNA och upprepade sedan den inflammatoriska behandlingen. Slående nog blev långt färre neuroner mekaniskt responsiva, vilket tyder på att detta enzym krävs för "avtystningen" av vissa smärtfibrer. Medan andra aspekter av sensibilisering sannolikt beror på ytterligare proteiner, kopplar detta resultat ett specifikt socker-modifierande enzym till den snabba uppkomsten av mekanisk överkänslighet. Eftersom variationer i det mänskliga B3GNT2-genet har associerats med smärtsamma inflammatoriska tillstånd placerar arbetet detta protein — och de sockermodifieringar det utför — som en lovande ny ingång för att förstå och så småningom behandla kronisk smärta.
Citering: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
Nyckelord: nociceptorer, proteomik, kronisk smärta, sensoriska neuroner, nervtillväxtfaktor