Clear Sky Science · de
Tiefgehende visuelle Proteomik enthüllt Nociceptor-Vielfalt und Schmerz-Ziele
Warum winzige schmerzempfindliche Zellen wichtig sind
Schmerz ist eines der wichtigsten Warnsysteme des Körpers, aber nicht alle schmerzempfindlichen Nervenzellen verhalten sich gleich. Manche reagieren auf Wärme, andere auf Kneifen oder Druck, und einige bleiben stumm, bis Verletzung oder Entzündung sie „aufwecken“. Diese Studie untersucht die tatsächlichen Proteine in einzelnen schmerzempfindlichen Mausneuronen, um zu verstehen, was sie voneinander unterscheidet — und um neue molekulare Schalter zu identifizieren, die zur Linderung chronischer Schmerzen angezielt werden könnten.
Ein genauerer Blick auf die Boten des Schmerzes
Bündel von sensorischen Nervenzellen im Rückenmark, sogenannte Hinterwurzelganglien, senden Informationen über Berührung, Temperatur und Verletzung an das Gehirn. Innerhalb dieser Bündel gibt es viele Neuronen-Subtypen, darunter Nocizeptoren, die auf schädliche Reize spezialisiert sind. Frühere Arbeiten nutzten RNA, das Instruktionshandbuch der Zelle, um diese Vielfalt zu kartieren. RNA erzählt aber nur einen Teil der Geschichte: Sie deutet an, welche Proteine existieren könnten, nicht welche tatsächlich vorhanden und aktiv sind. Proteine — nicht Gene — bestimmen letztlich, wie ein Neuron feuert und wie wir Schmerz empfinden. Die Autorinnen und Autoren wollten eine detaillierte Karte auf Protein-Ebene verschiedener sensorischer Neuronentypen erstellen, darunter zwei große schmerzempfindliche Untergruppen und berührungsempfindliche Mechanorezeptoren.
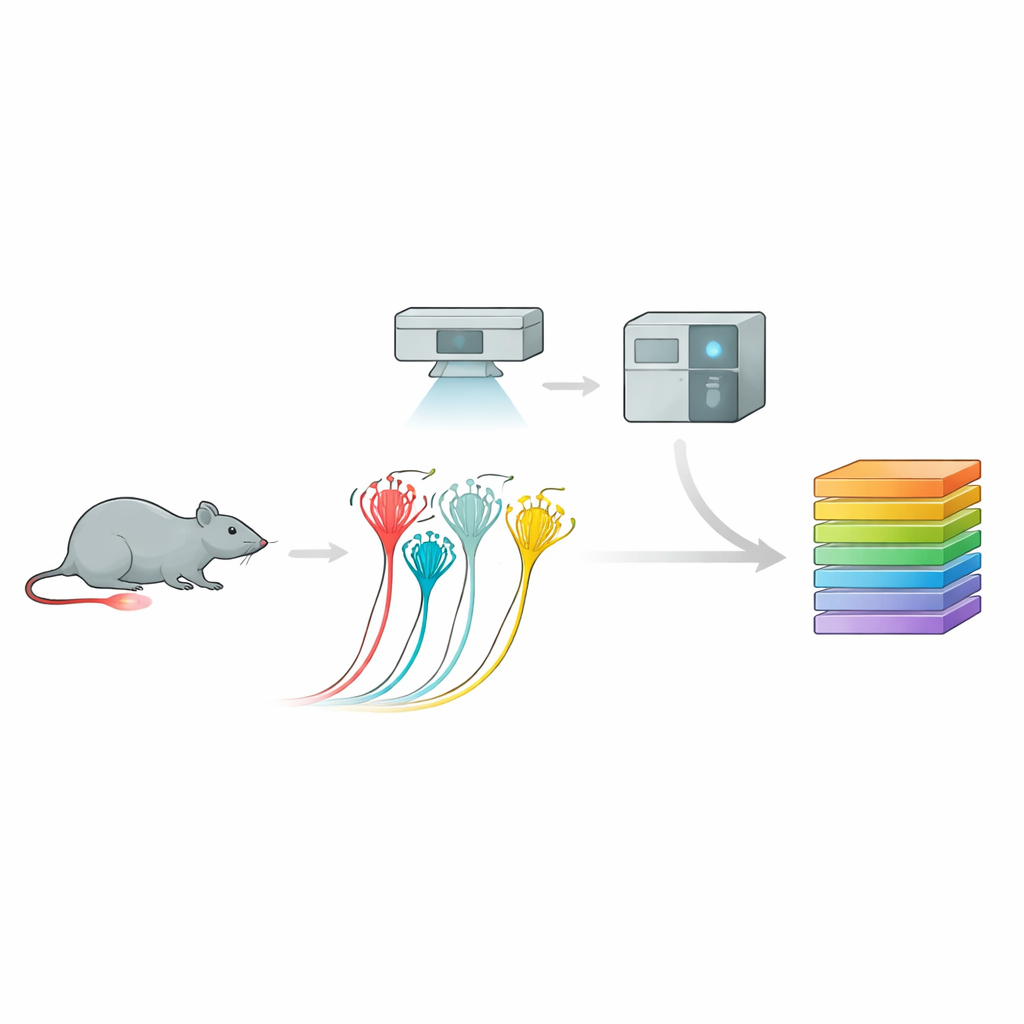
Bilder in Proteinkataloge verwandeln
Hierfür nutzte das Team eine leistungsfähige Pipeline namens Deep Visual Proteomics. Zuerst züchteten sie Maus-Sensorneuronen in Kultur und zeichneten deren elektrische Reaktionen auf Druck auf, sodass peptiderge Nocizeptoren, nicht-peptiderge Nocizeptoren und größere, berührungsempfindliche Neuronen anhand ihres Verhaltens und ihrer Oberflächenmarker unterschieden werden konnten. Mithilfe KI-gestützter Bildanalyse und Laser-Mikrodissektion schnitten sie dann gezielt nur die Zellen von Interesse aus. Jede winzige Probe — bis hin zu einem Bruchteil eines einzelnen Neurons — wurde in ein ultrasensitives Massenspektrometer gegeben, das Tausende von Proteinen identifizierte und quantifizierte. Dieser Ansatz erzeugte reichhaltige Proteinprofile für jeden Neuronentyp und offenbarte eindeutige molekulare „Fingerabdrücke“, die gut mit, aber auch über frühere Genexpressionskarten hinausgingen.
Schmerz-Zellvielfalt in Proteinen geschrieben
Die Forschenden stellten fest, dass jeder Nocizeptor-Subtyp einen stabilen Kernsatz von Proteinen trägt sowie ein eigenes, einzigartiges Signatur-Muster. Peptiderge und nicht-peptiderge Nocizeptoren — zwei lange bekannte Schmerz-Zellklassen — zeigten klare Unterschiede bei Ionenkanälen, Signalmolekülen und Stoffwechselwegen. Viele bekannte, mit Schmerz assoziierte Proteine traten auf, ebenso weniger vertraute Kandidaten, die einen Subtyp deutlich gegenüber anderen markierten. Wichtig war außerdem: Beim Vergleich von kultivierten Neuronen mit in spinalem Gewebe eingebetteten Neuronen überlappten die meisten Proteine. Das legt nahe, dass kultivierte Neuronen, ein zentraler Bestandteil der Schmerzforschung, ihre Identität auf Protein-Ebene größtenteils bewahren und somit ein verlässliches Modell sind, um Schmerzwege zu untersuchen.
Wie Entzündung Schmerzfasern „entschweigt“
Die Studie richtete dann den Fokus auf ein klassisches Schmerz-Szenario: die entzündliche Sensibilisierung. Bei Tieren und Menschen kann ein Wachstumsfaktor namens NGF bestimmte Nocizeptoren deutlich empfindlicher gegenüber mechanischen Reizen machen, ein Prozess, der zur Druckempfindlichkeit entzündeter Haut oder Gelenke beitragen soll. Die Autorinnen und Autoren ahmten dies nach, indem sie kultivierte Neuronen in NGF plus einen Protein-Kinase-Aktivator tauchten und zuvor stille peptiderge Nocizeptoren in robuste Reagierer auf mechanische Einbuchtung verwandelten. Im Vergleich der Proteinprofile behandelte und unbehandelter Zellen entdeckten sie eine kleine Anzahl von Proteinen, deren Spiegel speziell in sensibilisierten peptidergen Neuronen anstiegen. Ein Enzym, B3GNT2, das beim Anfügen von Zuckerketten an andere Moleküle hilft, stach als besonders starker Kandidat hervor.
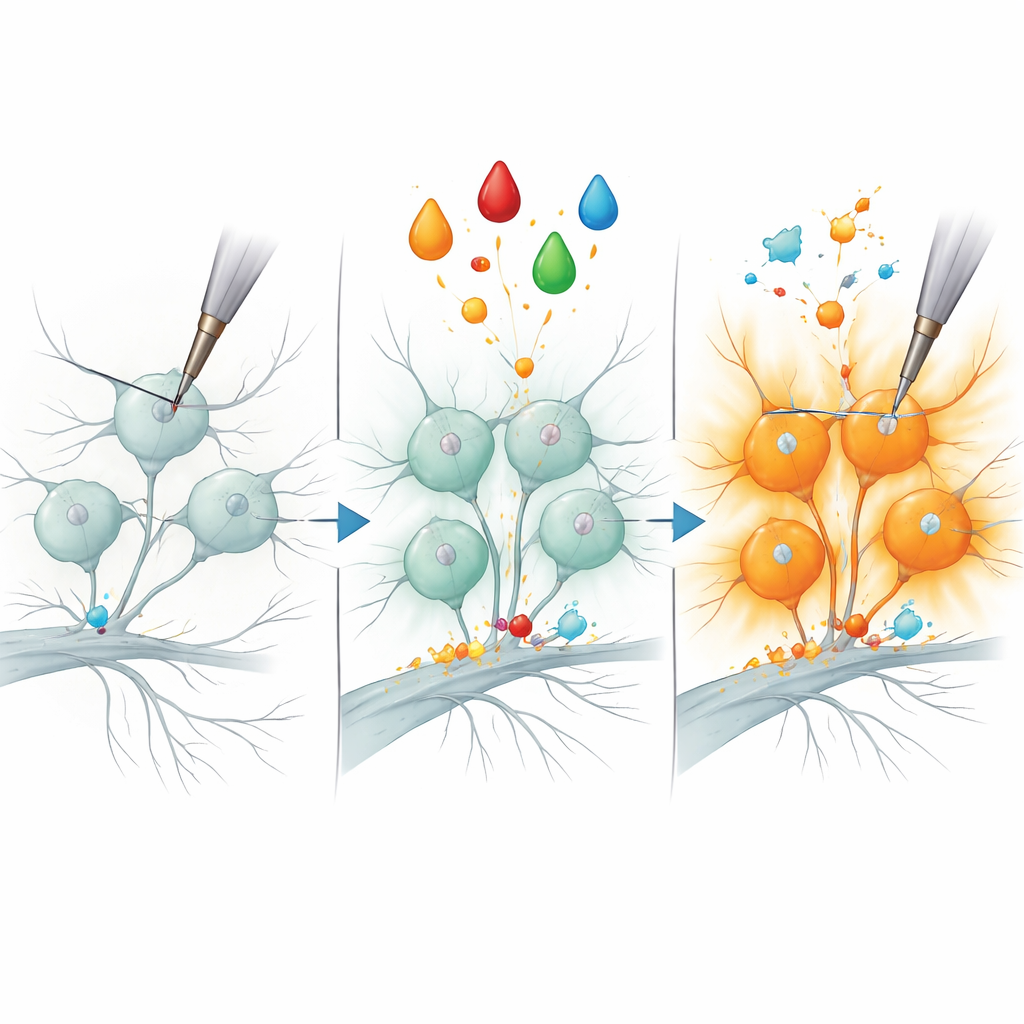
Ein neuer molekularer Ansatzpunkt für Schmerz
Um zu prüfen, ob B3GNT2 mehr als ein bloßer Begleiter ist, reduzierten die Forschenden seine Produktion in Nocizeptoren mithilfe kleiner interferierender RNA und wiederholten dann die entzündliche Behandlung. Bemerkenswerterweise wurden deutlich weniger Neurone mechanisch reaktiv, was darauf hindeutet, dass dieses Enzym für das „Entschweigen“ bestimmter Schmerzfasern erforderlich ist. Auch wenn andere Aspekte der Sensibilisierung wahrscheinlich von zusätzlichen Proteinen abhängen, verknüpft dieses Ergebnis ein spezifisches zucker-modifizierendes Enzym mit dem raschen Einsetzen mechanischer Überempfindlichkeit. Da Variationen im menschlichen B3GNT2-Gen mit schmerzhaften Entzündungszuständen in Verbindung gebracht wurden, positioniert die Arbeit dieses Protein — und die von ihm vorgenommenen Zucker-Modifikationen — als vielversprechenden neuen Ansatzpunkt zum Verständnis und letztlich zur Behandlung chronischer Schmerzen.
Zitation: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
Schlüsselwörter: Nocizeptoren, Proteomik, chronische Schmerzen, Sensorische Neuronen, Nerv-Wachstumsfaktor