Clear Sky Science · es
La proteómica visual profunda revela la diversidad de los nociceptores y dianas del dolor
Por qué importan las pequeñas células que detectan el dolor
El dolor es uno de los sistemas de alarma más importantes del cuerpo, pero no todas las células nerviosas que detectan el dolor actúan igual. Unas responden al calor, otras al pellizco o a la presión, y algunas permanecen silenciosas hasta que una lesión o inflamación las “despiertan”. Este estudio examina en profundidad las proteínas reales dentro de neuronas sensibles al dolor individuales de ratón para entender qué las distingue entre sí y para identificar interruptores moleculares nuevos que podrían dirigirse para aliviar el dolor crónico.
Una mirada más cercana a los mensajeros del dolor del cuerpo
Racimos de células nerviosas sensoriales en la médula espinal, llamados ganglios de la raíz dorsal, envían información sobre el tacto, la temperatura y la lesión al cerebro. Dentro de esos racimos hay muchos subtipos de neuronas, incluidos nociceptores especializados en detectar estímulos nocivos. Investigaciones previas utilizaron ARN, el manual de instrucciones celular, para cartografiar esta diversidad. Pero el ARN solo cuenta una parte de la historia: insinúa qué proteínas podrían existir, no cuáles están realmente presentes y activas. Son las proteínas, no los genes, las que en última instancia determinan cómo dispara una neurona y cómo percibimos el dolor. Los autores se propusieron construir un mapa detallado a nivel de proteínas de diferentes tipos de neuronas sensoriales, incluidos dos subgrupos principales detectores del dolor y mecanorreceptores sensibles al tacto.
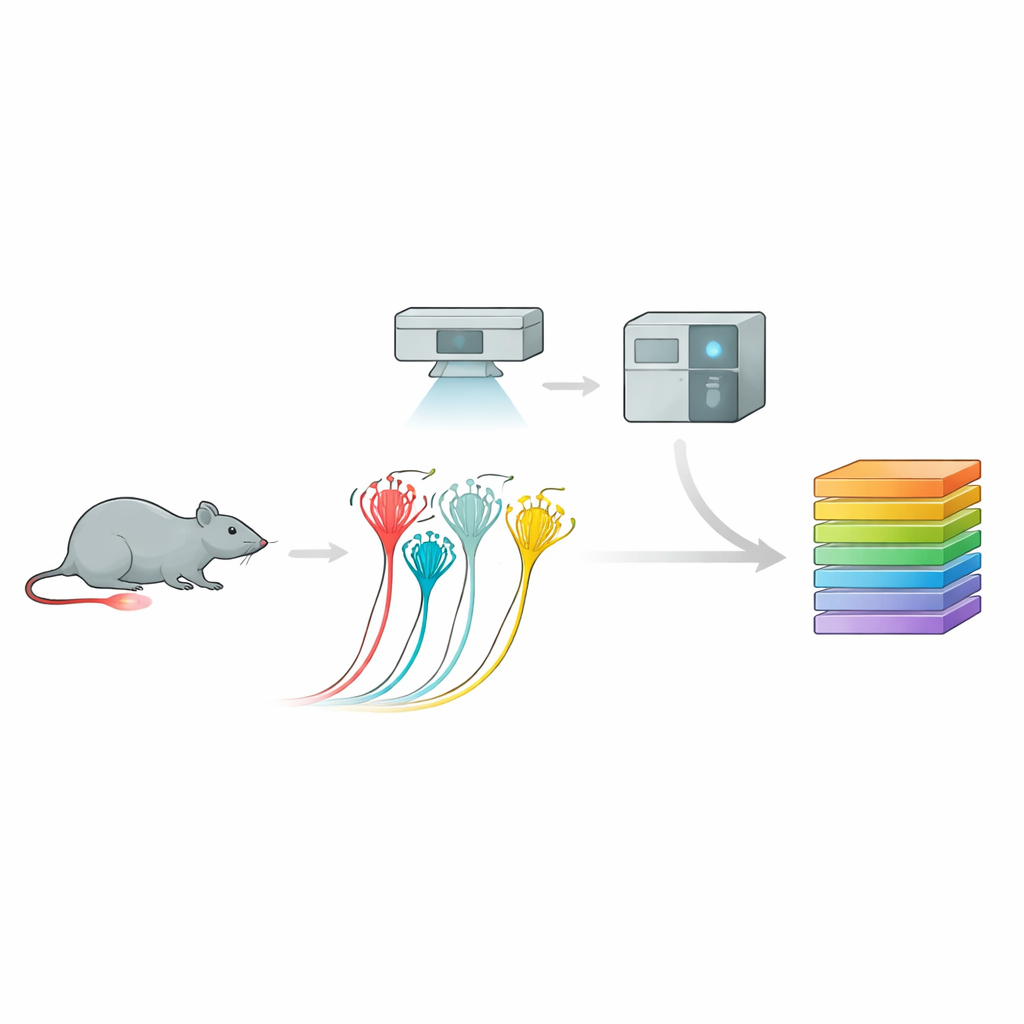
Convertir imágenes en catálogos de proteínas
Para ello, el equipo empleó una potente metodología llamada proteómica visual profunda. Primero, cultivaron neuronas sensoriales de ratón y registraron sus respuestas eléctricas a la presión, distinguiendo nociceptores peptidérgicos, nociceptores no peptidérgicos y neuronas más grandes sensibles al tacto en función de su comportamiento y marcadores de superficie. Luego, mediante análisis de imagen guiado por IA y microdisección láser, cortaron con precisión solo las células de interés. Cada diminuta muestra —hasta una fracción de una sola neurona— se introdujo en un espectrómetro de masas ultrasensible que identificó y cuantificó miles de proteínas. Este enfoque produjo perfiles proteicos ricos para cada subtipo neuronal, revelando “huellas” moleculares distintas que concordaban con, pero también ampliaban, los mapas de expresión génica previos.
La diversidad de las células del dolor escrita en proteínas
Los investigadores hallaron que cada subtipo de nociceptor posee un conjunto central estable de proteínas, además de su propia firma única. Los nociceptores peptidérgicos y no peptidérgicos —dos clases de células del dolor reconocidas desde hace tiempo— mostraron diferencias claras en canales iónicos, moléculas de señalización y vías metabólicas. Aparecieron muchas proteínas relacionadas con el dolor ya conocidas, pero también candidatos menos familiares que marcaban de forma contundente a un subtipo frente a otro. De modo importante, al comparar neuronas en cultivo con neuronas todavía embebidas en tejido espinal, la mayoría de las proteínas coincidieron. Esto sugiere que las neuronas en cultivo, una herramienta habitual en la investigación del dolor, conservan en gran medida su identidad intracorporal a nivel proteico, lo que las convierte en un modelo fiable para explorar cómo funcionan las vías del dolor.
Cómo la inflamación “dessilencia” las fibras del dolor
El estudio se centró luego en un escenario clásico del dolor: la sensibilización inflamatoria. Tanto en animales como en personas, un factor de crecimiento llamado NGF puede volver ciertos nociceptores notablemente más sensibles a estímulos mecánicos, un proceso que se cree contribuye a la hipersensibilidad de la piel o las articulaciones inflamadas. Los autores recrearon esto bañando las neuronas en cultivo con NGF más un activador de quinasas de proteínas, convirtiendo nociceptores peptidérgicos previamente silenciosos en respondedores robustos a la indentación mecánica. Al comparar los perfiles proteicos de células tratadas y no tratadas, detectaron un pequeño conjunto de proteínas cuyos niveles aumentaron específicamente en los nociceptores peptidérgicos sensibilizados. Una enzima, B3GNT2, que ayuda a añadir cadenas de azúcar a otras moléculas, emergió como una candidata particularmente sólida.
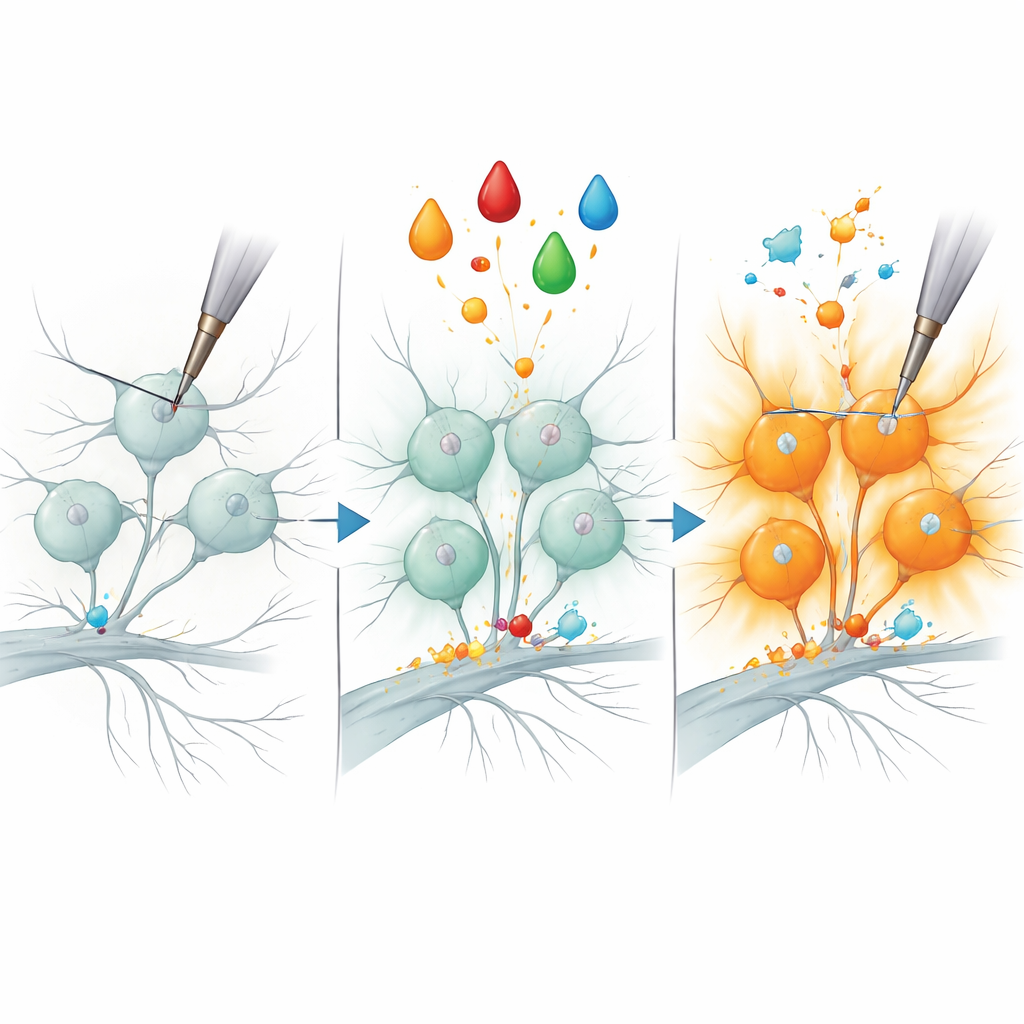
Un nuevo punto de apoyo molecular sobre el dolor
Para comprobar si B3GNT2 es más que un mero acompañante, el equipo redujo su producción en nociceptores usando ARN interferente y luego repitió el tratamiento inflamatorio. Sorprendentemente, muchas menos neuronas se volvieron sensibles mecánicamente, lo que sugiere que esta enzima es necesaria para el “desilenciamiento” de ciertas fibras del dolor. Si bien otras características de la sensibilización probablemente dependen de proteínas adicionales, este resultado vincula una enzima específica modificadora de azúcares con el inicio rápido de la hipersensibilidad mecánica. Dado que variaciones en el gen humano B3GNT2 se han asociado con condiciones inflamatorias dolorosas, el trabajo posiciona a esta proteína —y las modificaciones de azúcar que realiza— como un enfoque prometedor para comprender y, eventualmente, tratar el dolor crónico.
Cita: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
Palabras clave: nociceptores, proteómica, dolor crónico, neuronas sensoriales, factor de crecimiento nervioso