Clear Sky Science · fr
La protéomique visuelle approfondie révèle la diversité des nocicepteurs et des cibles de la douleur
Pourquoi ces minuscules cellules sensorielles de la douleur comptent
La douleur est l’un des systèmes d’alerte les plus importants du corps, pourtant toutes les cellules nerveuses sensibles à la douleur ne se comportent pas de la même manière. Certaines réagissent à la chaleur, d’autres à la pincée ou à la pression, et certaines restent silencieuses jusqu’à ce qu’une blessure ou une inflammation « les réveille ». Cette étude explore en profondeur les protéines réelles présentes à l’intérieur de neurones nociceptifs individuels de souris pour comprendre ce qui les distingue les uns des autres — et pour repérer de nouveaux interrupteurs moléculaires susceptibles d’être ciblés pour soulager la douleur chronique.
Un regard plus précis sur les messagers de la douleur
Des paquets de cellules nerveuses sensorielles dans la moelle épinière, appelés ganglions rachidiens dorsaux, transmettent au cerveau des informations sur le toucher, la température et les lésions. Dans ces amas coexistent de nombreux sous-types de neurones, y compris des nocicepteurs spécialisés dans la détection d’un stimulus nocif. Des recherches antérieures ont utilisé l’ARN, le mode d’emploi de la cellule, pour cartographier cette diversité. Mais l’ARN ne raconte qu’une partie de l’histoire : il indique quels protéines pourraient exister, pas lesquelles sont réellement présentes et actives. Ce sont les protéines, non les gènes, qui déterminent en fin de compte comment un neurone s’active et comment nous ressentons la douleur. Les auteurs se sont donné pour objectif de construire une carte détaillée au niveau protéique des différents types de neurones sensoriels, incluant deux grands sous-groupes de détecteurs de douleur et des mécanorécepteurs sensibles au toucher.
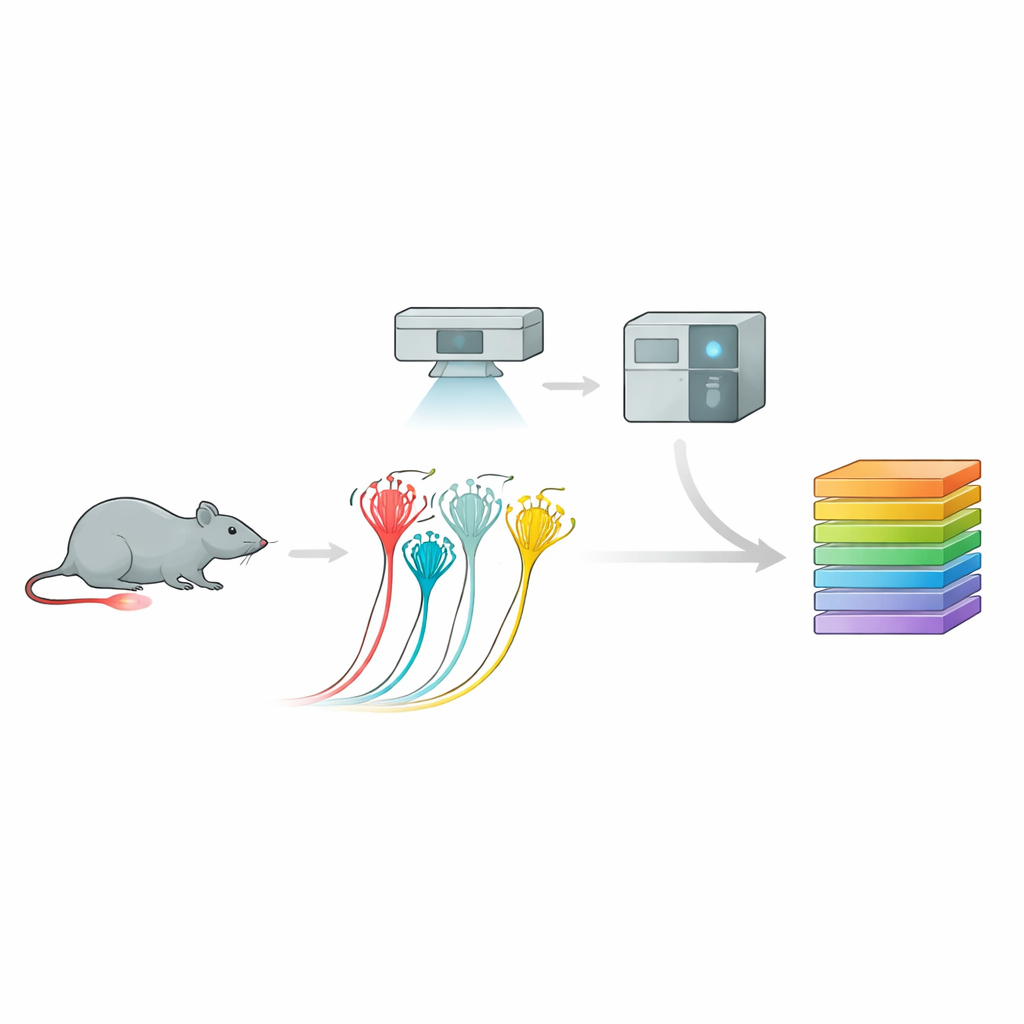
Transformer des images en catalogues protéiques
Pour ce faire, l’équipe a utilisé une chaîne d’analyse puissante appelée protéomique visuelle approfondie. D’abord, ils ont cultivé des neurones sensoriels de souris et enregistré leurs réponses électriques à la pression, distinguant les nocicepteurs peptidergiques, non peptidergiques et les neurones plus volumineux sensibles au toucher en se basant sur leur comportement et des marqueurs de surface. Ensuite, grâce à une analyse d’images guidée par IA et à la microdissection au laser, ils ont découpé avec précision uniquement les cellules d’intérêt. Chaque minuscule échantillon — jusqu’à une fraction d’un seul neurone — a été injecté dans un spectromètre de masse ultrasensible qui a identifié et quantifié des milliers de protéines. Cette approche a produit des profils protéiques riches pour chaque sous-type de neurone, révélant des « empreintes » moléculaires distinctes qui concordent avec, mais vont aussi au-delà des, cartes d’expression génique précédentes.
La diversité des cellules de la douleur écrite en protéines
Les chercheurs ont constaté que chaque sous-type de nocicepteur possède un ensemble central stable de protéines, auquel s’ajoute sa propre signature unique. Les nocicepteurs peptidergiques et non peptidergiques — deux classes de cellules de la douleur reconnues depuis longtemps — présentaient des différences nettes dans les canaux ioniques, les molécules de signalisation et les voies métaboliques. De nombreuses protéines déjà liées à la douleur ont été retrouvées, mais aussi des candidats moins familiers marquant fortement un sous-type plutôt qu’un autre. Fait important, lorsque l’équipe a comparé des neurones en culture à des neurones encore intégrés dans le tissu spinal, la majorité des protéines se chevauchaient. Cela suggère que les neurones en culture, couramment utilisés en recherche sur la douleur, conservent largement leur identité in vivo au niveau protéique, faisant d’eux un modèle fiable pour explorer le fonctionnement des voies de la douleur.
Comment l’inflammation « désilence » les fibres douloureuses
L’étude s’est ensuite focalisée sur un scénario classique de la douleur : la sensibilisation inflammatoire. Chez les animaux comme chez l’humain, un facteur de croissance appelé NGF peut rendre certains nocicepteurs beaucoup plus sensibles aux stimulations mécaniques, un processus supposé contribuer à la sensibilité des peaux ou articulations enflammées. Les auteurs ont reproduit cela en exposant des neurones en culture au NGF associé à un activateur de protéine kinase, transformant des nocicepteurs peptidergiques auparavant silencieux en répondeurs robustes à l’indentation mécanique. En comparant les profils protéiques des cellules traitées et non traitées, ils ont détecté un petit ensemble de protéines dont les niveaux augmentaient spécifiquement dans les nocicepteurs peptidergiques sensibilisés. Une enzyme, B3GNT2, qui participe à l’ajout de chaînes glycosidiques à d’autres molécules, est apparue comme un candidat particulièrement solide.
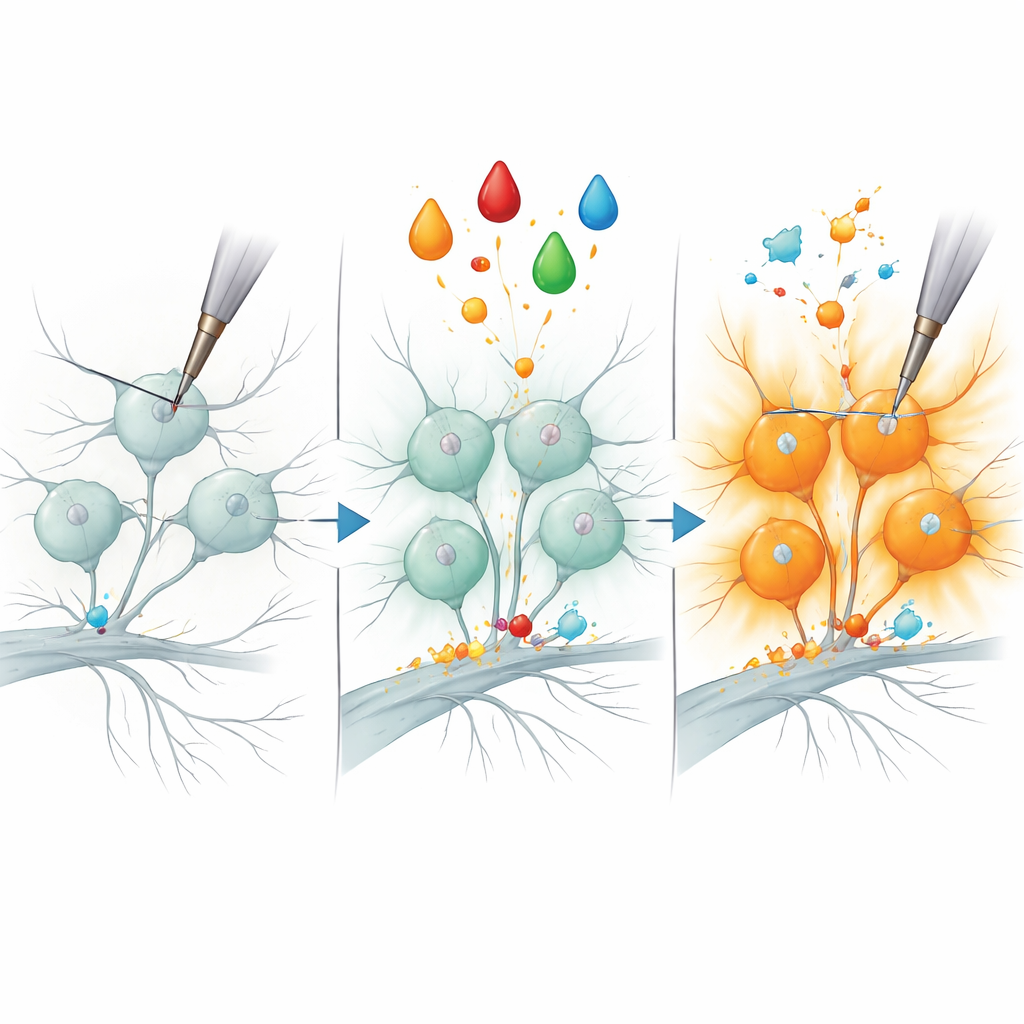
Une nouvelle poignée moléculaire sur la douleur
Pour vérifier si B3GNT2 est plus qu’un simple marqueur, l’équipe a réduit sa production dans les nocicepteurs en utilisant des ARN interférents, puis a répété le traitement inflammatoire. De manière saisissante, bien moins de neurones sont devenus mécaniquement réactifs, suggérant que cette enzyme est nécessaire au « désilencement » de certaines fibres de la douleur. Alors que d’autres aspects de la sensibilisation dépendent probablement de protéines additionnelles, ce résultat relie une enzyme spécifique de modification sucrée à l’apparition rapide de l’hypersensibilité mécanique. Parce que des variations du gène humain B3GNT2 ont été associées à des affections inflammatoires douloureuses, ce travail positionne cette protéine — et les modifications sucrées qu’elle réalise — comme un nouvel angle prometteur pour comprendre et, éventuellement, traiter la douleur chronique.
Citation: Chakrabarti, S., Makhmut, A., Mohammadi, A. et al. Deep visual proteomics uncovers nociceptor diversity and pain targets. Nat Commun 17, 3437 (2026). https://doi.org/10.1038/s41467-026-71418-8
Mots-clés: nocicepteurs, protéomique, douleur chronique, neurones sensoriels, facteur de croissance nerveuse