Clear Sky Science · zh
基于FRET的c-di-GMP生物传感器工具箱及其用于全基因组映射c-di-GMP调控的FRET-To-Sort应用
细菌如何决定“停靠”还是“游动”
细菌不断在自由游动与在称为生物膜的黏性群体中定居之间做出选择,这一切换影响感染、环境循环乃至工业结垢。本文介绍了新的工具,允许科学家在单个细胞中实时观察一种关键的内部信号,并利用这些工具揭示了一个令人意外的联系:细菌微小推进器(鞭毛)旋转的强弱与其形成生物膜的决策之间的关系。
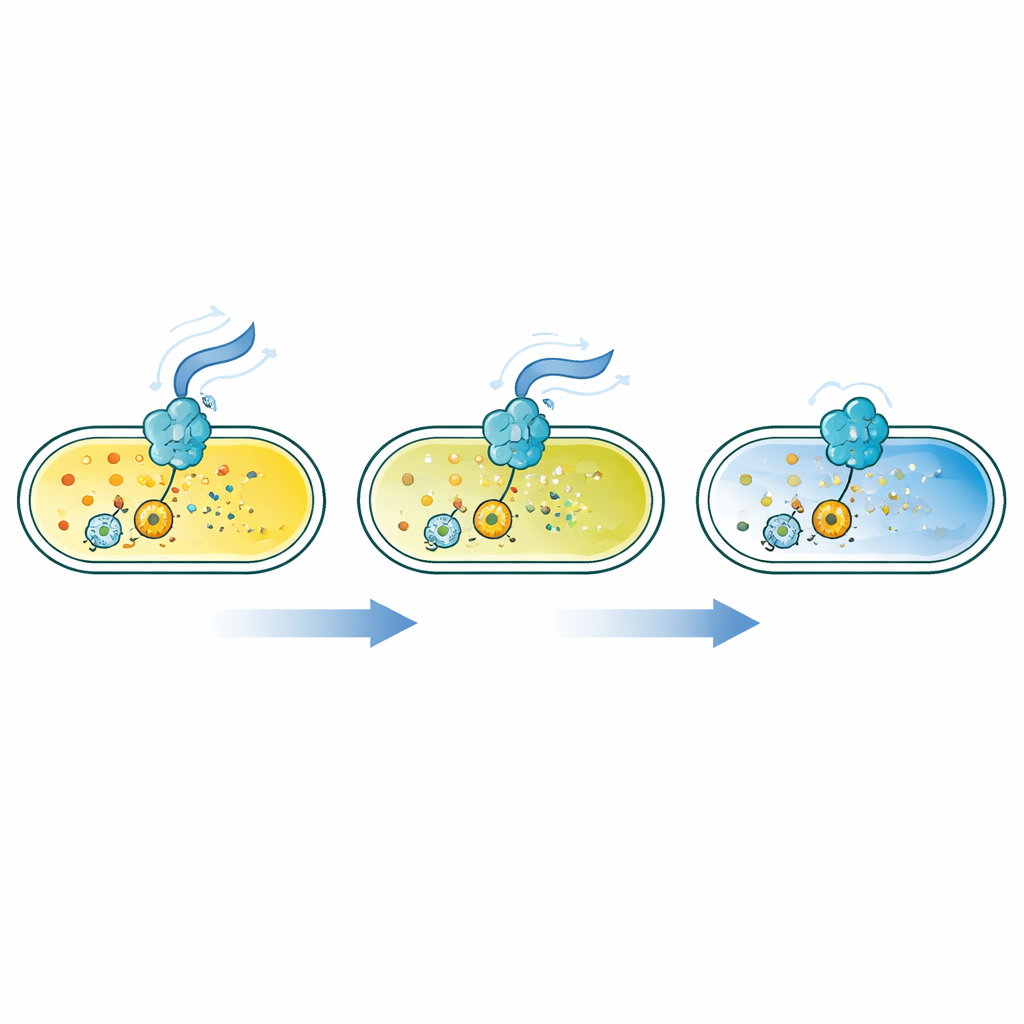
改变细菌生活方式的微小分子
许多细菌依赖一种环状小分子c-di-GMP作为内部开关。低含量有利于快速游动,而较高含量促使细胞定居、附着在表面并形成生物膜。该信号由一族响应营养、氧气、应激等因素的酶合成和降解。然而直到现在,研究人员还缺乏一套灵敏、快速且可广泛调节的传感器来观测活细胞内c-di-GMP的整个浓度范围,尤其是在该分子极低浓度时。
构建多用途的颜色变化传感器工具箱
作者基于FRET设计了一系列蛋白质传感器。FRET是一种当两个荧光蛋白靠得很近时,一个可以将能量传递给另一个的过程。他们将一对明亮的荧光蛋白融合到一组细菌“读者”蛋白上,这些读者在结合c-di-GMP时会改变构象。根据设计不同,这种构象变化要么使荧光对更靠近,要么将它们推远,从而改变FRET信号。通过在大肠杆菌(Escherichia coli)中筛选90种不同的读者蛋白,他们鉴定出16种对宽广c-di-GMP浓度范围有强响应的传感器,覆盖大约十亿分之十到百万分之一的浓度——既能检测自由游动细菌中常见的低水平,也能覆盖生物膜中的较高水平。
在单细胞层面更仔细地观察
利用这套工具箱,团队改进了一种流式细胞术方法,能够每秒精确测量成千上万细胞的FRET,并校正光学伪影以便跨实验和传感器比较结果。他们通过两种方式确认了所测得的结合强度:将透化的细胞浸泡在已知c-di-GMP溶液中,以及在试管中测试纯化的传感器。随后他们在微流控通道中追踪单个细菌,发现c-di-GMP水平在细胞之间以及随时间都有强烈波动,即便在遗传上相同的群体中亦是如此。高亲和力的传感器揭示了这些低浓度范围内的细微差异,而旧的、灵敏度较低的传感器在很大程度上错过了这些差异。
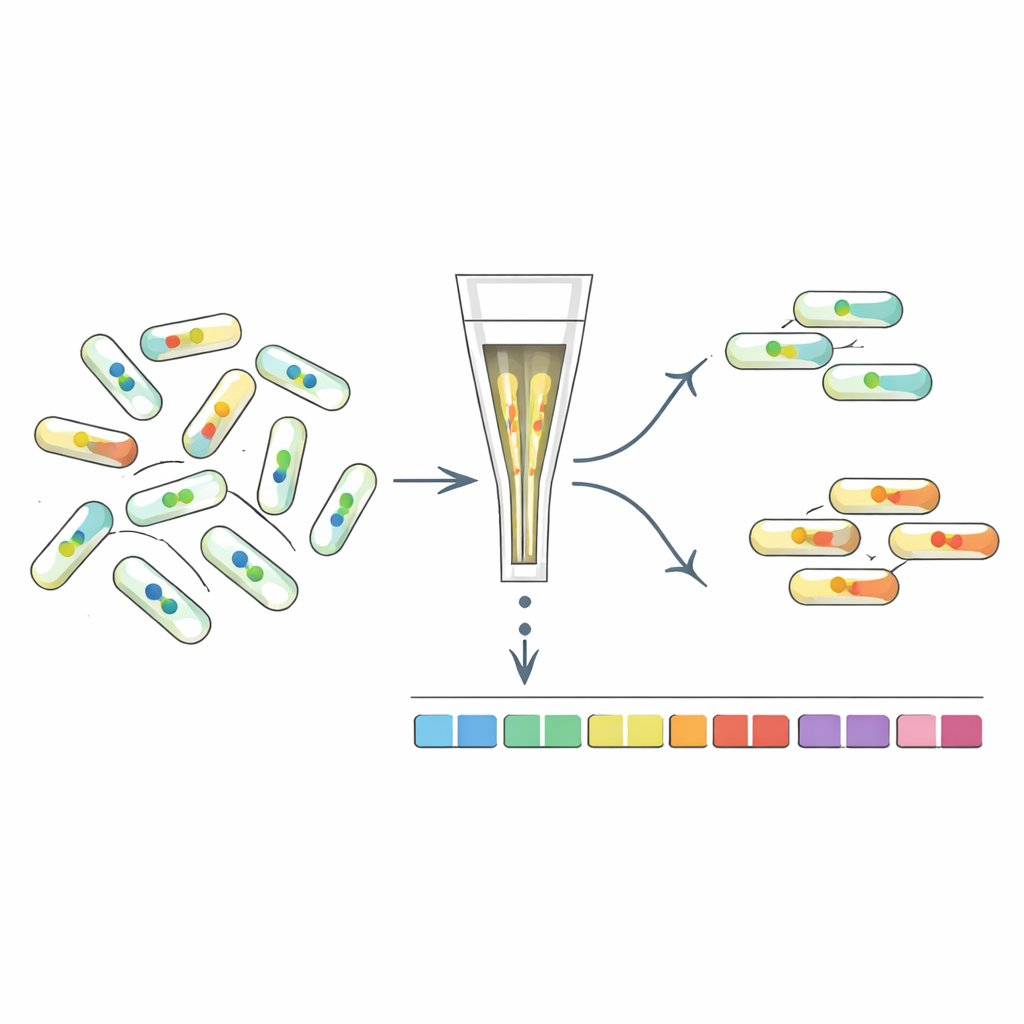
按内部信号对突变体进行分选
为了解哪些基因影响c-di-GMP水平,研究者们开发了“FRET-To-Sort”,将其传感器与高通量突变体筛选结合。他们将挑选出的传感器引入一个带条形码的数万株大肠杆菌突变体文库,然后使用细胞分选器收集那些FRET信号异常高或低的细胞,这些信号反映了c-di-GMP的改变。对条形码的测序揭示了这些异常细胞中被破坏的基因。正如预期的那样,已知c-di-GMP酶的突变体被富集。但筛选还突出了许多其他基因,包括参与细胞包膜、菌毛(表面毛状纤维)、应激反应以及令人注目的推动游动的旋转鞭毛系统的基因。
鞭毛马达作为隐形的信号旋钮
分析揭示了鞭毛系统的双面作用。阻断构建鞭毛基座早期步骤的突变会提高c-di-GMP,因为它们间接降低了一种关键降解酶的产生。相反,破坏马达旋转部件或去除外部丝状体的突变则产生相反效果:降低c-di-GMP。进一步实验表明,当鞭毛无法旋转时,细胞膜电位——即跨外膜的电压——升高,而这种高电位抑制了一种主要c-di-GMP合成酶的活性。化学塌陷膜电位则产生相反作用,提升c-di-GMP。即便用特异性抗体机械卡住鞭毛也会降低c-di-GMP,这表明细菌能感知其马达的负载情况,并将这种机械信息转化为生活方式的决策信号。
这对理解和控制细菌意味着什么
总体而言,这些结果提供了一套标准化的活细胞c-di-GMP传感器以及一种强大的策略来绘制输入这一中心开关的遗传网络。对非专业读者而言,关键结论是细菌不仅对化学物质做出反应;它们还“感知”推进器转动的难易程度并相应调整内部信号。通过将机械应变和细胞膜的电学状态与决定黏附与游动的分子联系起来,这项工作为探查并可能破坏医学与环境上重要微生物的生物膜形成开辟了新途径。
引用: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
关键词: 细菌第二信使, 生物膜调控, FRET生物传感器, 鞭毛运动性, 全基因组突变体筛选