Clear Sky Science · sv
Verktygslåda med FRET-baserade c-di-GMP-biosensorer och dess FRET-To-Sort-applikation för genomomfattande kartläggning av c-di-GMP-reglering
Hur bakterier bestämmer sig för att fästa eller simma
Bakterier växlar ständigt mellan att röra sig fritt och att slå sig ner i slemmiga samhällen som kallas biofilmer — ett val som påverkar infektioner, miljöcykler och även industriell påväxt. Denna artikel presenterar nya verktyg som låter forskare följa en viktig intern signal i enskilda bakterieceller i realtid, och använder dem för att avslöja en överraskande koppling mellan hur snabbt en bakteries små propellrar snurrar och dess beslut att bygga biofilm.
En liten molekyl som ändrar bakteriers livsstil
Många bakterier använder en liten ringformad molekyl, c-di-GMP, som en intern strömbrytare. Låga nivåer gynnar snabb simning, medan högre nivåer driver cellerna mot att slå sig ner, fästa vid ytor och bilda biofilmer. Signalen syntetiseras och bryts ner av familjer av enzymer som svarar på näring, syre, stress och mer. Fram till nu har forskare saknat en enhetlig uppsättning känsliga, snabba och allmänt justerbara sensorer för att se hela spannet av c-di-GMP-nivåer inne i levande celler, särskilt när molekylen finns i mycket låga koncentrationer.
Bygga en mångsidig verktygslåda för färgförändrande sensorer
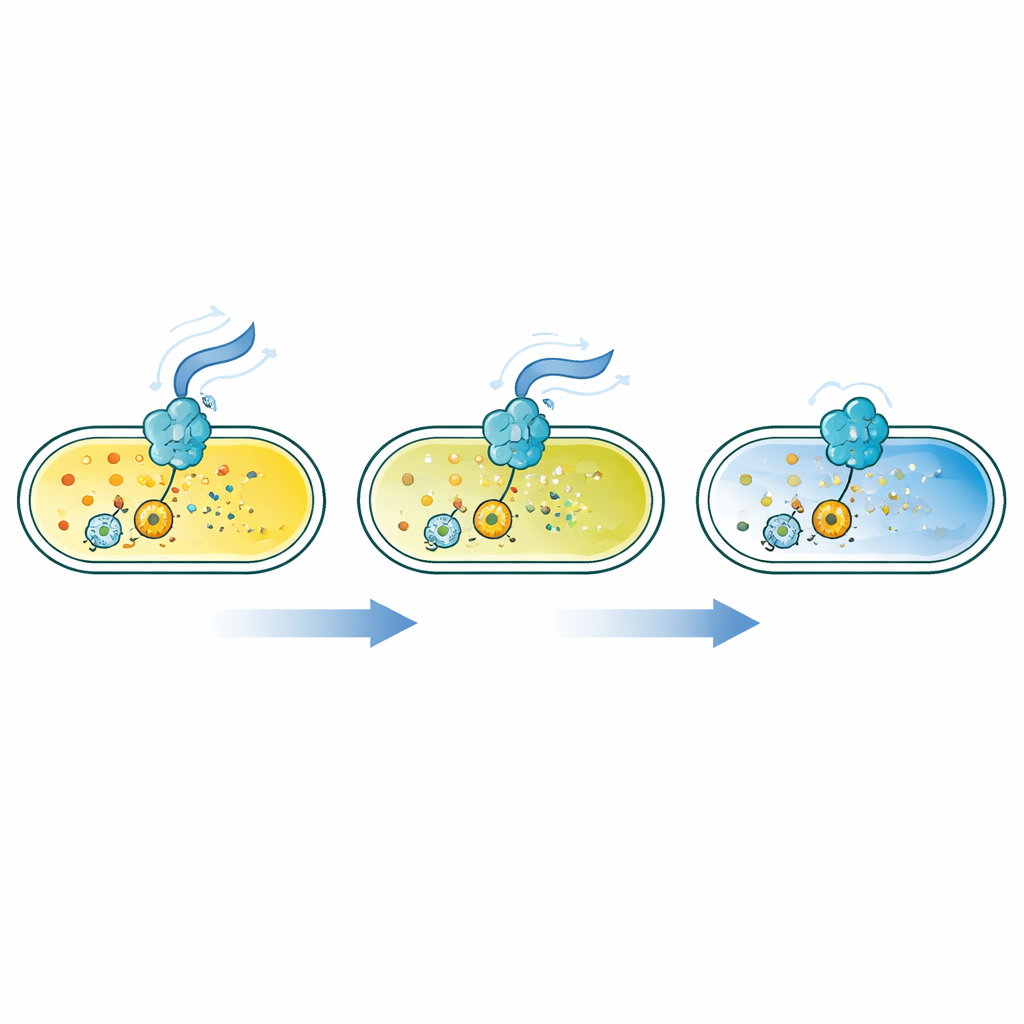
Forskarna konstruerade en familj proteinsensorer baserade på FRET, en process där ett fluorescerande protein kan överföra energi till ett annat när de sitter mycket nära varandra. De fäste par av starkt lysande fluorescerande proteiner vid en uppsättning bakteriella ”läsar”-proteiner som ändrar form när de binder c-di-GMP. Beroende på konstruktionen för detta formskifte antingen de fluorescerande paren närmare varandra eller pressas isär, vilket ändrar FRET-signalen. Genom att skärma av 90 olika läsarproteiner i Escherichia coli identifierade de 16 sensorer som reagerar starkt över ett brett spann av c-di-GMP-koncentrationer, från ungefär tio miljarder delar av en mol till en miljondel — vilket täcker de låga nivåer som ofta finns i fritt simmande bakterier såväl som högre nivåer i biofilmer.
En närmare titt på enskilda celler
Med denna verktygslåda förbättrade teamet en flödescytometri-metod som mäter FRET precist i tusentals celler per sekund, och korrigerade för optiska artefakter så att resultat kan jämföras mellan experiment och sensorer. De bekräftade de uppmätta bindningsstyrkorna på två sätt: genom att blöta genomsläppliggjorda celler i kända c-di-GMP-lösningar och genom att testa renade sensorer i provrör. De följde sedan enskilda bakterier i mikrofluidiska kanaler och fann att c-di-GMP-nivåerna varierar kraftigt mellan celler och över tid, även i genetiskt identiska populationer. Högaffinitetsensorer avslöjade subtila skillnader i dessa låga koncentrationsområden som äldre, svagare sensorer till stora delar missade.
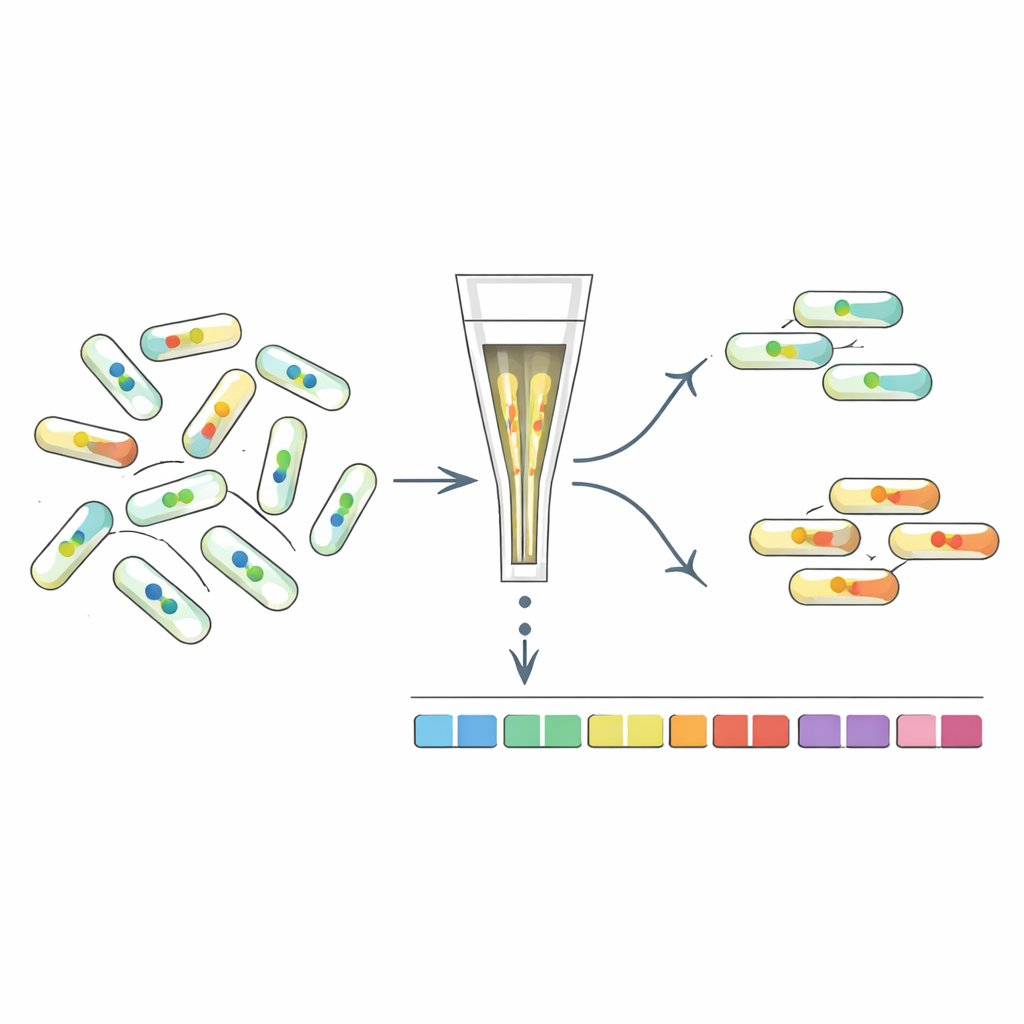
Sortera mutanter efter deras interna signal
För att förstå vilka gener som formar c-di-GMP-nivåerna utvecklade forskarna ”FRET-To-Sort”, som kopplar deras sensorer till höggenomströmmande mutantscreening. De införde utvalda sensorer i ett streckkods-bibliotek av tiotusentals E. coli-mutanter och använde sedan en cellsorter för att samla celler med ovanligt hög eller låg FRET-signal, vilket indikerar förändrade c-di-GMP-nivåer. Sekvensering av streckkoderna avslöjade vilka gener som var störda i dessa avvikare. Som väntat var mutanter i kända c-di-GMP-enzymer berikade. Men screeningen framhöll också många andra gener, inklusive de som är inblandade i cellmembranet, fimbrier (hårslocklika ytfibrer), stressresponser och, slående nog, de roterande flagellerna som driver simning.
Flagellmotorer som dolda signalrattar
Analysen avslöjade en tvåsidig roll för flagellsystemet. Mutationer som blockerar tidiga steg i uppbyggnaden av flagellens bas höjde c-di-GMP, eftersom de indirekt sänkte produktionen av ett nyckelenzym som bryter ner molekylen. Däremot hade mutationer som inaktiverade motorernas snurrande delar eller avlägsnade den externa filamenten motsatt effekt: de sänkte c-di-GMP. Ytterligare experiment visade att när flageller inte kan rotera, ökar cellens membranpotential — spänningen över dess yttre gräns — och denna höga spänning dämpar aktiviteten hos ett huvudenzym som producerar c-di-GMP. Kemisk kollaps av membranpotentialen gav omvänd effekt och ökade c-di-GMP. Även fysisk fastkörning av flagellerna med specifika antikroppar reducerade c-di-GMP, vilket tyder på att bakterier känner av hur belastade deras motorer är och omvandlar denna mekaniska information till livsstilsbeslut.
Vad detta betyder för att förstå och kontrollera bakterier
Tillsammans ger dessa resultat ett standardiserat set av sensorer för c-di-GMP i levande celler och en kraftfull strategi för att kartlägga de genetiska nätverk som matar in i denna centrala strömbrytare. För icke-specialister är huvudpoängen att bakterier inte bara reagerar på kemikalier; de ”känner” också hur lätt deras små propellrar snurrar och justerar sina interna signaler därefter. Genom att koppla mekanisk belastning och elektriskt tillstånd vid cellmembranet till molekylen som styr fästande kontra simmande öppnar detta arbete nya sätt att undersöka och kanske störa biofilmsbildning i medicinskt och miljömässigt viktiga mikrober.
Citering: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
Nyckelord: bakteriella andra budbärare, biofilmreglering, FRET-biosensorer, flagellär rörlighet, genomomfattande mutantscreening