Clear Sky Science · es
Caja de herramientas de biosensores FRET para c-di-GMP y su aplicación FRET-To-Sort para el mapeo genómico de la regulación de c-di-GMP
Cómo deciden las bacterias si quedarse o nadar
Las bacterias eligen constantemente entre deambular libremente y asentarse en comunidades pegajosas llamadas biopelículas, un cambio que influye en las infecciones, los ciclos ambientales e incluso las incrustaciones industriales. Este artículo presenta nuevas herramientas que permiten a los científicos observar una señal interna clave en células bacterianas individuales en tiempo real, y las utiliza para descubrir un vínculo sorprendente entre la velocidad de giro de los diminutos propulsores de una bacteria y su decisión de formar biopelículas.
Una molécula diminuta que cambia el estilo de vida bacteriano
Muchas bacterias dependen de una pequeña molécula en forma de anillo, el c-di-GMP, como un interruptor interno. Cantidades bajas favorecen la natación rápida, mientras que niveles más altos empujan a las células hacia el asentamiento, la adhesión a superficies y la formación de biopelículas. Esta señal se sintetiza y degrada mediante familias de enzimas que responden a nutrientes, oxígeno, estrés y otros estímulos. Hasta ahora, sin embargo, los investigadores carecían de un conjunto único de sensores sensibles, rápidos y ampliamente ajustables para ver el rango completo de niveles de c-di-GMP dentro de células vivas, especialmente cuando la molécula está presente en concentraciones muy bajas.
Construyendo una caja de herramientas de sensores de cambio de color versátiles
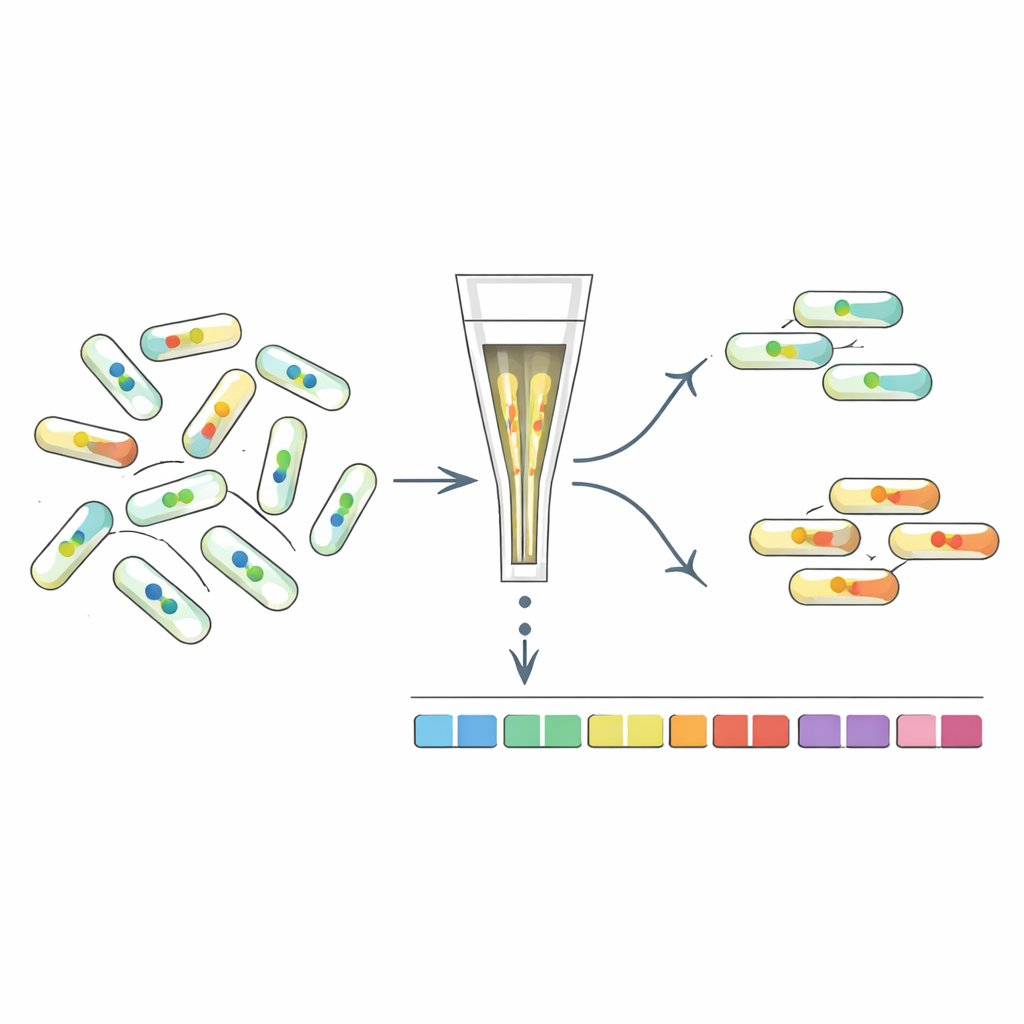
Los autores diseñaron una familia de sensores proteicos basados en FRET, un proceso en el que una proteína fluorescente puede transferir energía a otra cuando están muy próximas. Fusionaron pares de proteínas fluorescentes brillantes a un conjunto de proteínas “lectoras” bacterianas que cambian de forma al unirse a c-di-GMP. Según el diseño, este cambio de forma acerca el par fluorescente o los separa, alterando la señal FRET. Mediante el cribado de 90 proteínas lectoras distintas en Escherichia coli, identificaron 16 sensores que responden con fuerza a lo largo de un amplio rango de concentraciones de c-di-GMP, desde aproximadamente diez milmillonésimas de mol hasta una millonésima—cubriendo los niveles bajos que se encuentran a menudo en bacterias nadadoras y los niveles más altos en biopelículas.
Observando más de cerca células individuales
Con esta caja de herramientas, el equipo mejoró un método de citometría de flujo que mide FRET con precisión en miles de células por segundo, corrigiendo artefactos ópticos para que los resultados puedan compararse entre experimentos y sensores. Confirmaron las afinidades medidas de dos maneras: permeabilizando células y exponiéndolas a soluciones de c-di-GMP de concentración conocida y probando sensores purificados en tubos de ensayo. Luego siguieron bacterias individuales en canales microfluídicos, encontrando que los niveles de c-di-GMP fluctúan fuertemente entre células y a lo largo del tiempo, incluso en poblaciones genéticamente idénticas. Los sensores de alta afinidad revelaron diferencias sutiles en estos rangos de baja concentración que los sensores antiguos y menos sensibles apenas detectaban.
Separando mutantes según su señal interna
Para entender qué genes moldean los niveles de c-di-GMP, los investigadores desarrollaron “FRET-To-Sort”, que acopla sus sensores a un cribado de mutantes de alto rendimiento. Introdujeron sensores seleccionados en una biblioteca codificada por códigos de barras de decenas de miles de mutantes de E. coli, y luego usaron un separador celular para recoger células con señales FRET inusualmente altas o bajas, indicativas de c-di-GMP alterado. La secuenciación de los códigos de barras reveló qué genes estaban interrumpidos en estos valores atípicos. Como era de esperar, los mutantes en enzimas conocidas de c-di-GMP se enriquecieron. Pero el cribado también destacó muchos otros genes, incluidos los implicados en la envoltura celular, las fimbrias (fibras superficiales) , las respuestas al estrés y, de forma llamativa, los flagelos rotatorios que impulsan la natación.
Los motores flagelares como mandos ocultos de la señal
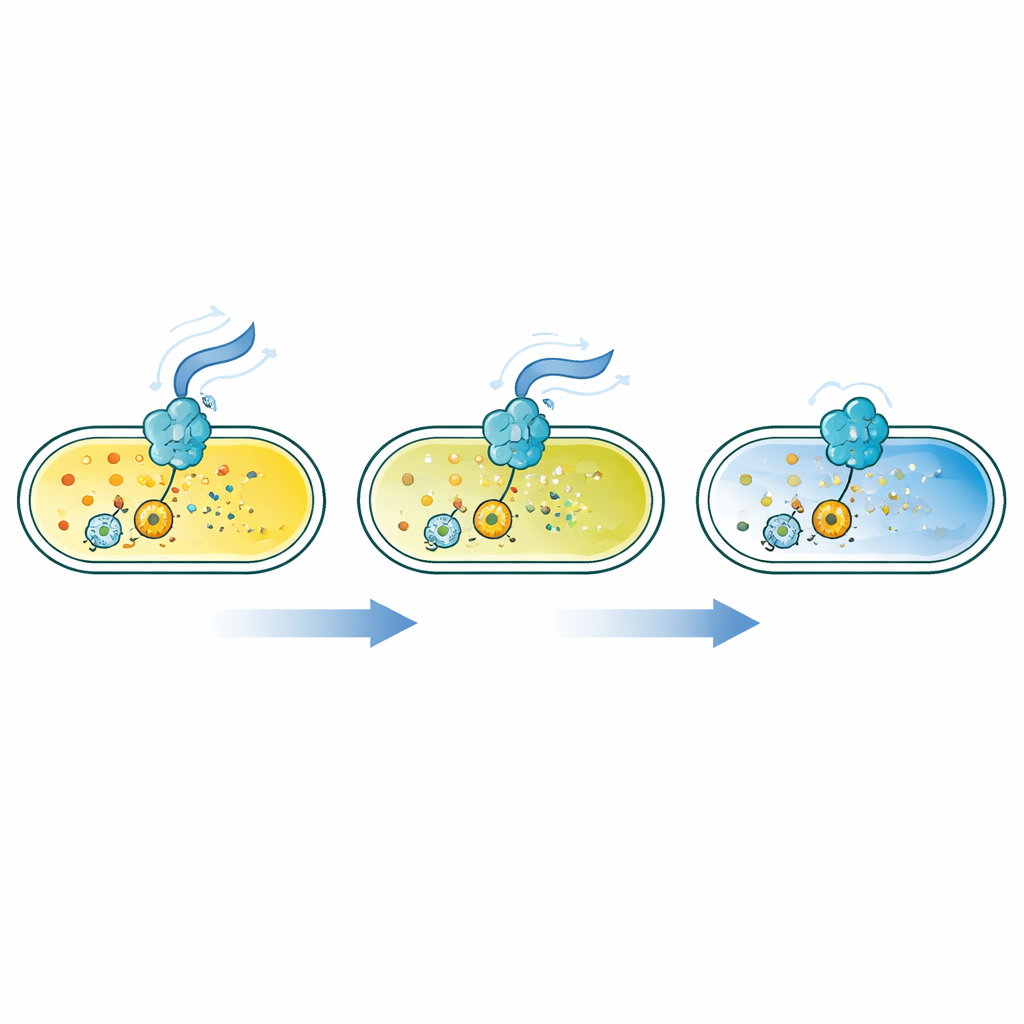
El análisis reveló un papel doble del sistema flagelar. Mutaciones que bloquean pasos tempranos en la construcción de la base flagelar aumentaron el c-di-GMP, porque indirectamente disminuían la producción de una enzima clave que degrada la molécula. En contraste, mutaciones que incapacitan las partes giratorias del motor o eliminan el filamento externo tuvieron el efecto opuesto: redujeron el c-di-GMP. Experimentos adicionales mostraron que cuando los flagelos no pueden rotar, el potencial de membrana de la célula—el voltaje a través de su límite externo—aumenta, y este alto voltaje atenúa la actividad de una enzima principal productora de c-di-GMP. Colapsar químicamente el potencial de membrana tuvo el efecto inverso, elevando el c-di-GMP. Incluso atascando físicamente los flagelos con anticuerpos específicos redujo el c-di-GMP, lo que sugiere que las bacterias detectan la carga en sus motores y traducen esta información mecánica en decisiones sobre su estilo de vida.
Qué implica esto para comprender y controlar las bacterias
En conjunto, estos resultados proporcionan un conjunto estandarizado de sensores de c-di-GMP en células vivas y una estrategia poderosa para mapear las redes genéticas que alimentan este interruptor central. Para el público general, la conclusión clave es que las bacterias no solo responden a señales químicas; también “sienten” lo fácil que giran sus diminutos propulsores y ajustan sus señales internas en consecuencia. Al vincular la tensión mecánica y el estado eléctrico de la membrana celular con la molécula que gobierna quedarse frente a nadar, este trabajo abre nuevas vías para sondear y quizá interrumpir la formación de biopelículas en microbios de importancia médica y ambiental.
Cita: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
Palabras clave: mensajeros secundarios bacterianos, regulación de biopelículas, biosensores FRET, motilidad flagelar, cribado de mutantes a escala genómica