Clear Sky Science · ru
Набор FRET-биосенсоров для c-di-GMP и их применение FRET-To-Sort для картирования регуляции c-di-GMP по всему геному
Как бактерии решают — держаться или плыть
Бактерии постоянно делают выбор между свободным перемещением и оседанием в скользких сообществах, называемых биопленками; этот переключатель влияет на инфекции, экологические циклы и даже промышленные отложения. В статье представлены новые инструменты, позволяющие наблюдать ключевой внутриклеточный сигнал в отдельных бактериальных клетках в реальном времени, а также с их помощью обнаружена неожиданная связь между скоростью вращения крошечных пропеллеров бактерии и её решением формировать биопленки.
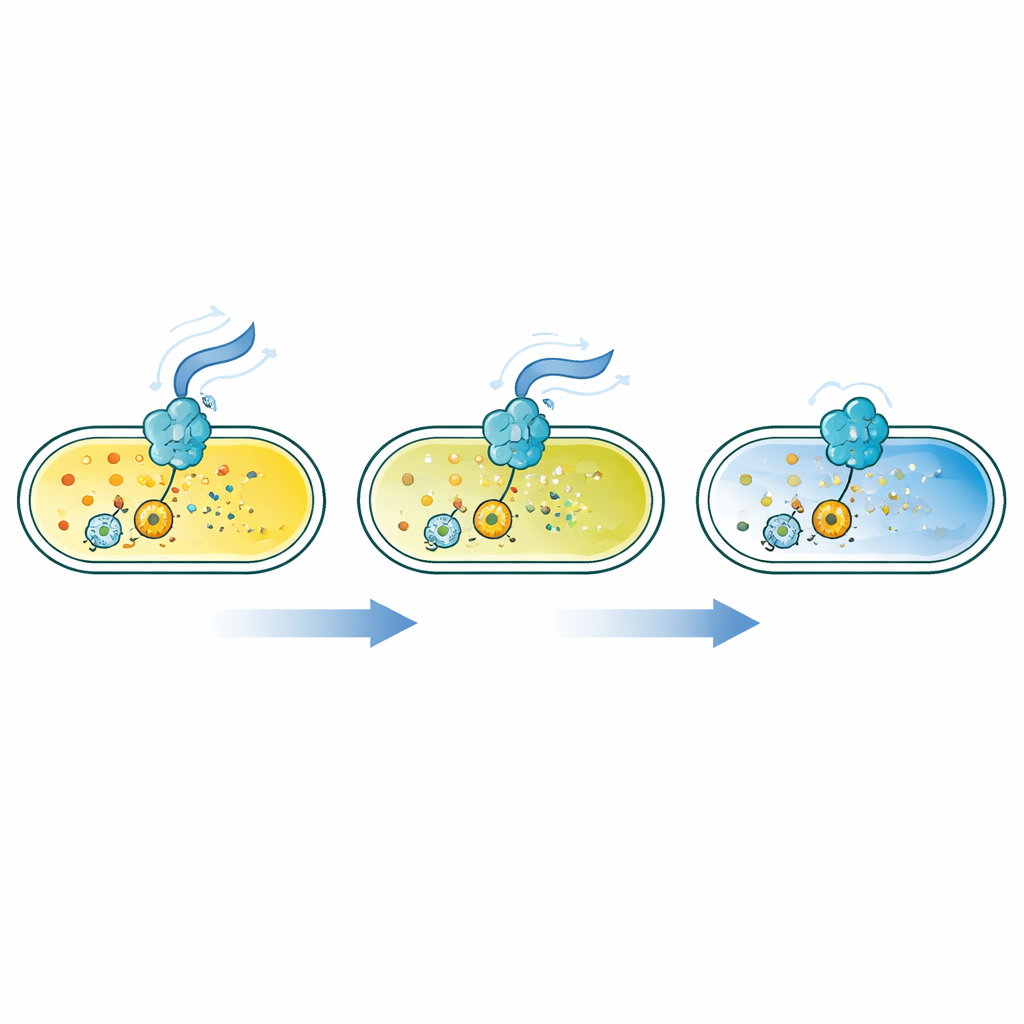
Крошечная молекула, меняющая образ жизни бактерий
Многие бактерии полагаются на маленькую кольцевую молекулу c-di-GMP как внутренний переключатель. Низкие концентрации способствуют быстрому плаванию, тогда как более высокие сдвигают клетки в сторону оседания, прикрепления к поверхностям и формирования биопленок. Этот сигнал синтезируется и разрушается семействами ферментов, которые реагируют на питательные вещества, кислород, стресс и другие факторы. До сих пор у исследователей не было единого набора чувствительных, быстрых и гибко настраиваемых датчиков, позволяющих увидеть полный диапазон уровней c-di-GMP в живых клетках, особенно при очень низких концентрациях.
Создание универсального набора цветоизменяющихся сенсоров
Авторы сконструировали семейство белковых сенсоров на основе FRET — процесса, при котором один флуоресцентный белок может передавать энергию другому при очень близком расположении. Они слили пары ярких флуоресцентных белков с набором бактериальных «ридерных» белков, которые меняют свою форму при связывании c-di-GMP. В зависимости от конструкции это изменение формы либо сближает флуорофоры, либо раздвигает их, меняя FRET-сигнал. Просcreenив 90 разных ридеров в Escherichia coli, они выявили 16 сенсоров, сильно реагирующих в широком диапазоне концентраций c-di-GMP — от примерно десяти миллиардных моля до миллионных — охватывая низкие уровни, характерные для свободноплавающих бактерий, и более высокие уровни в биопленках.
Внимательнее к отдельным клеткам
Имея этот набор, команда усовершенствовала методику проточной цитометрии, позволяющую точно измерять FRET у тысяч клеток в секунду, корректируя оптические артефакты так, чтобы результаты можно было сравнивать между экспериментами и сенсорами. Они подтвердили измеренные константы связывания двумя способами: пропитывая проницаемые клетки растворами с известной концентрацией c-di-GMP и тестируя очищенные сенсоры в пробирках. Затем они проследили отдельные бактерии в микрофлюидных каналах и обнаружили, что уровни c-di-GMP сильно флуктуируют между клетками и во времени, даже в генетически идентичных популяциях. Сенсоры с высокой аффинностью выявили тонкие различия в низком диапазоне концентраций, которые старые, менее чувствительные датчики в значительной степени пропускали.
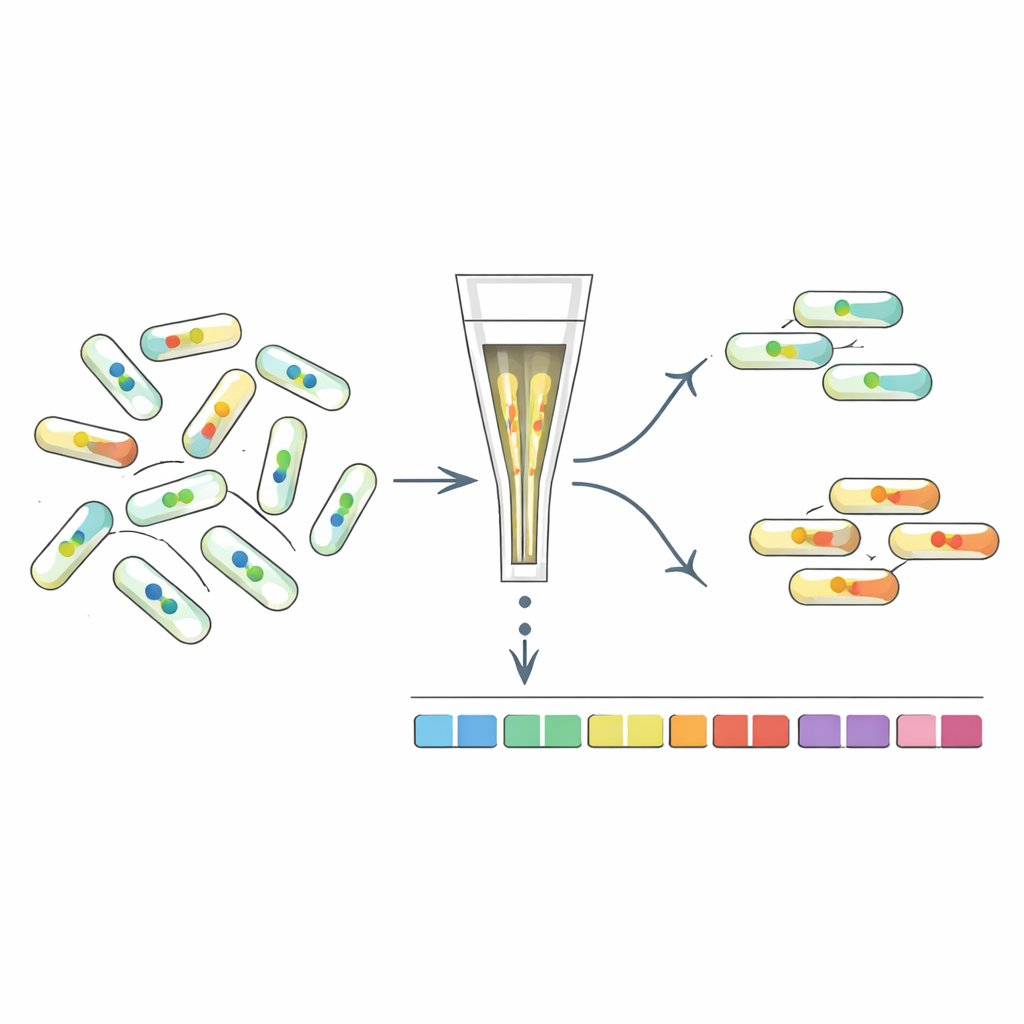
Сортировка мутантов по их внутриклеточному сигналу
Чтобы понять, какие гены формируют уровни c-di-GMP, исследователи разработали «FRET-To-Sort», стратегию, сочетающую их сенсоры с высокопроизводительным скринингом мутантов. Они ввели выбранные сенсоры в библиотеку штрихкодированных десятков тысяч мутантов E. coli, затем использовали клеточный сортировщик для отбора клеток с необычно высоким или низким FRET-сигналом, указывающим на изменённый уровень c-di-GMP. Секвенирование штрихкодов показало, какие гены были нарушены у этих аутлаеров. Как и ожидалось, мутанты в известных ферментах, связанных с c-di-GMP, оказались обогащены. Но скрининг также выделил множество других генов, включая те, что участвуют в строении оболочки клетки, фимбриях (волосковидных поверхностных структурах), стресс-ответах и, что особенно примечательно, роторных жгутиках, приводящих в движение плавание.
Жгутиковые моторы как скрытые регуляторы сигнала
Анализ выявил двоякую роль жгутиковой системы. Мутации, блокирующие ранние этапы сборки основания жгутика, повышали уровень c-di-GMP, поскольку они косвенно снижали продукцию ключевого фермента, разрушающего эту молекулу. Напротив, мутации, которые выключали вращающиеся части мотора или удаляли внешний филамент, имели противоположный эффект: они понижали c-di-GMP. Дальнейшие эксперименты показали, что когда жгутики не могут вращаться, мембранный потенциал клетки — напряжение через её внешнюю границу — повышается, и это высокое напряжение подавляет активность основного фермента, синтезирующего c-di-GMP. Химическое снижение мембранного потенциала давало обратный эффект, повышая c-di-GMP. Даже механическая блокировка жгутиков специфическими антителами снижала c-di-GMP, что указывает на то, что бактерии ощущают нагрузку на свои моторы и переводят эту механическую информацию в решения об образе жизни.
Что это значит для понимания и контроля бактерий
Вместе эти результаты дают стандартизованный набор сенсоров c-di-GMP для живых клеток и мощную стратегию для картирования генетических сетей, влияющих на этот центральный переключатель. Для неспециалистов главный вывод в том, что бактерии реагируют не только на химические сигналы; они также «чувствуют», насколько легко вращаются их крошечные пропеллеры, и соответствующим образом настраивают свои внутренние сигналы. Связав механическое напряжение и электрическое состояние мембраны с молекулой, которая управляет выбором между прикреплением и плаванием, эта работа открывает новые пути для исследования и, возможно, вмешательства в формирование биопленок у медицински и экологически значимых микроорганизмов.
Цитирование: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
Ключевые слова: бактериальные вторичные мессенджеры, регуляция биопленок, FRET-биосенсоры, жгутиковая подвижность, геномный скрининг мутантов