Clear Sky Science · nl
Gereedschapsset van FRET-gebaseerde c-di-GMP-biosensoren en de FRET-To-Sort-toepassing voor genoombrede in kaart brengen van c-di-GMP-regulatie
Hoe bacteriën beslissen of ze blijven plakken of gaan zwemmen
Bacteriën kiezen continu tussen vrij rondzwerven en zich vestigen in slijmachtige gemeenschappen die biofilms worden genoemd, een omschakeling die infecties, milieuprocessen en zelfs industriële vervuiling beïnvloedt. Dit artikel presenteert nieuwe instrumenten waarmee onderzoekers een belangrijke interne signaalstof in individuele bacteriële cellen in realtime kunnen volgen, en gebruikt deze om een verrassende verbinding bloot te leggen tussen hoe hard de kleine propellers van een bacterie draaien en de beslissing om biofilms te bouwen.
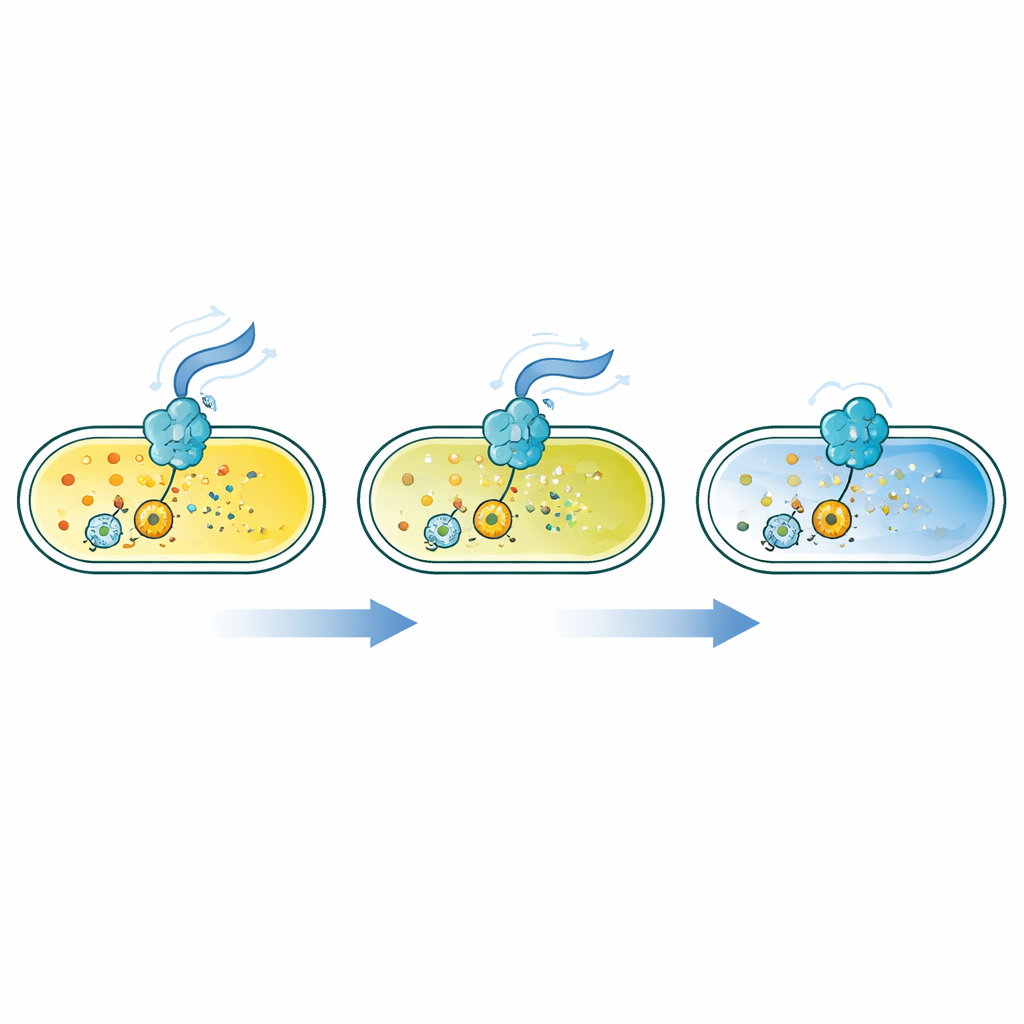
Een piepkleine molecule die bacteriële levensstijlen verandert
Veel bacteriën vertrouwen op een klein ringvormig molecuul, c-di-GMP, als interne schakelaar. Lage hoeveelheden bevorderen snel zwemmen, terwijl hogere niveaus cellen naar vestiging, hechten aan oppervlakken en biofilmvorming duwen. Dit signaal wordt gemaakt en afgebroken door families van enzymen die reageren op voedingsstoffen, zuurstof, stress en meer. Tot nu toe misten onderzoekers echter één set gevoelige, snelle en breed instelbare sensoren om het volledige bereik van c-di-GMP-niveaus in levende cellen te zien, vooral wanneer het molecuul in zeer lage concentraties aanwezig is.
Een veelzijdige gereedschapsset van kleurveranderende sensoren bouwen
De auteurs ontwierpen een familie eiwitsensoren op basis van FRET, een proces waarbij een fluorescerend eiwit energie kan overdragen aan een ander wanneer ze heel dicht bij elkaar zitten. Ze fuseerden paren van heldere fluorescerende eiwitten aan een reeks bacteriële “lezers” — eiwitten die van vorm veranderen wanneer ze c-di-GMP binden. Afhankelijk van het ontwerp brengt deze vormverandering het fluorescentiepaar dichter bij elkaar of duwt het uit elkaar, waardoor het FRET-signaal verandert. Door 90 verschillende lezer-eiwitten in Escherichia coli te screenen, identificeerden ze 16 sensoren die sterk reageren over een breed spectrum van c-di-GMP-concentraties, van ongeveer tien miljardsten van een mol tot een miljoenste — en daarmee de lage niveaus die vaak in vrijzwemmende bacteriën voorkomen evenals de hogere niveaus in biofilms beslaan.
Een nadere blik op individuele cellen
Met deze gereedschapsset verbeterde het team een flow-cytometrie-methode die FRET nauwkeurig meet in duizenden cellen per seconde, en corrigeerde voor optische artefacten zodat resultaten tussen experimenten en sensoren vergeleken kunnen worden. Ze bevestigden de gemeten bindingssterktes op twee manieren: door permeabiliseerde cellen in oplossingen met bekende c-di-GMP-concentraties te weken en door gezuiverde sensoren in reageerbuizen te testen. Vervolgens volgden ze individuele bacteriën in microfluïdische kanalen en ontdekten dat c-di-GMP-niveaus sterk fluctueren tussen cellen en in de tijd, zelfs in genetisch identieke populaties. Hoog-affiniteitsensoren onthulden subtiele verschillen in deze lage concentratiegebieden die oudere, zwakkere sensoren grotendeels misten.
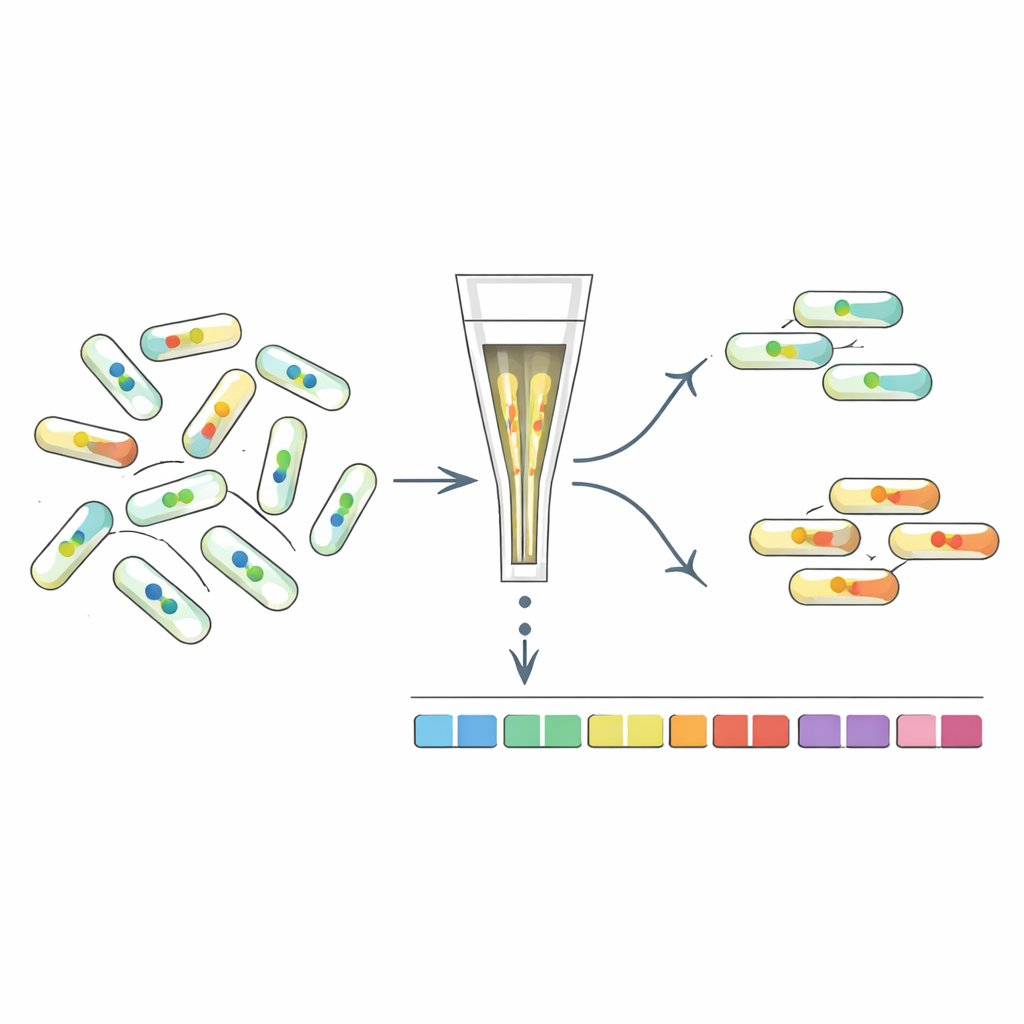
Mutanten sorteren op hun interne signaal
Om te begrijpen welke genen c-di-GMP-niveaus bepalen, ontwikkelden de onderzoekers “FRET-To-Sort”, dat hun sensoren koppelt aan hoogdoorvoer-mutantenscreening. Ze introduceerden geselecteerde sensoren in een gebarcodde bibliotheek van tienduizenden E. coli-mutanten en gebruikten vervolgens een cel-sorteerder om cellen te verzamelen met ongewoon hoge of lage FRET-signalen, wat wijst op veranderde c-di-GMP. Sequencing van de barcodes onthulde welke genen in deze uitschieters verstoord waren. Zoals verwacht waren mutanten in bekende c-di-GMP-enzymen verrijkt. Maar het screen benadrukte ook veel andere genen, waaronder die betrokken bij de celmembraan, fimbriae (haarachtige oppervlaktevezels), stressreacties en, opvallend, de roterende flagellen die het zwemmen aandrijven.
Flagellaire motoren als verborgen signaalknoppen
De analyse bracht een tweezijdige rol van het flagellaire systeem aan het licht. Mutaties die vroege stappen in de bouw van de flagelbasis blokkeren verhoogden c-di-GMP, omdat ze indirect de productie van een sleutelenzym dat het molecuul afbreekt verlaagden. Daarentegen hadden mutaties die de draaiende onderdelen van de motor uitschakelden of het externe filament verwijderden het tegenovergestelde effect: ze verlaagden c-di-GMP. Verdere experimenten toonden aan dat wanneer flagellen niet kunnen roteren, het membraanpotentiaal van de cel — de spanning over de buitenste grens — stijgt, en deze hoge spanning dempt de activiteit van een belangrijk c-di-GMP-producerend enzym. Chemisch inzakken van het membraanpotentiaal had het omgekeerde effect en verhoogde c-di-GMP. Zelfs het fysiek blokkeren van de flagellen met specifieke antilichamen verminderde c-di-GMP, wat erop wijst dat bacteriën voelen hoe zwaar hun motoren belast zijn en deze mechanische informatie vertalen naar levensstijlbeslissingen.
Wat dit betekent voor begrip en beheersing van bacteriën
Gezamenlijk leveren deze resultaten een gestandaardiseerde set levende-cel c-di-GMP-sensoren en een krachtige strategie om de genetische netwerken in kaart te brengen die in deze centrale schakelaar voeden. Voor niet-specialisten is de belangrijkste conclusie dat bacteriën niet alleen op chemische signalen reageren; ze “voelen” ook hoe gemakkelijk hun kleine propellers draaien en passen hun interne signalen daarop aan. Door mechanische spanning en de elektrische toestand van het celmembraan te koppelen aan het molecuul dat hechten versus zwemmen reguleert, opent dit werk nieuwe wegen om biofilmvorming te onderzoeken en mogelijk te verstoren in medisch en ecologisch belangrijke microben.
Bronvermelding: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
Trefwoorden: bacteriële tweede boodschappers, biofilmregulatie, FRET-biosensoren, flagellaire mobiliteit, genoomwijde mutantenscreening