Clear Sky Science · ar
مجموعة أدوات لمستشعرات c-di-GMP المعتمدة على FRET وتطبيق FRET-To-Sort لرسم خرائط تنظيم c-di-GMP عبر الجينوم
كيف تقرر البكتيريا متى تلتصق ومتى تسبح
تختار البكتيريا باستمرار بين التجول بحرية والاستقرار داخل مجتمعات مخاطية تُسمى الأغشية الحيوية؛ وهو تبديل يشكل مسارات العدوى والدورات البيئية وحتى التلوث الصناعي. تكشف هذه الورقة عن أدوات جديدة تتيح للعلماء مراقبة إشارة داخلية رئيسية في خلايا بكتيرية مفردة في الزمن الحقيقي، وتستخدم هذه الأدوات لكشف رابط مفاجئ بين سرعة دوران مراوح البكتيريا الدقيقة وقرارها بناء الأغشية الحيوية.
جزيء صغير يغير أنماط حياة البكتيريا
تعتمد كثير من البكتيريا على جزيء حلقي صغير، c-di-GMP، كمفتاح داخلي. التركيزات المنخفضة تفضل السباحة السريعة، بينما تدفع التركيزات الأعلى الخلايا نحو الاستقرار والالتصاق بالأسطح وتكوين الأغشية الحيوية. يُنتَج هذا الإشارة ويتحلل بواسطة عائلات من الإنزيمات التي تستجيب للمغذيات والأكسجين والإجهاد وعوامل أخرى. حتى الآن، لم يمتلك الباحثون مجموعة موحدة من المستشعرات الحساسة، السريعة والقابلة للضبط على نطاق واسع لرؤية الطيف الكامل لمستويات c-di-GMP داخل الخلايا الحية، لا سيما عندما يوجد الجزيء بتركيزات منخفضة جدًا.
بناء صندوق أدوات مستشعرات متغير الألوان متعدد الاستخدامات
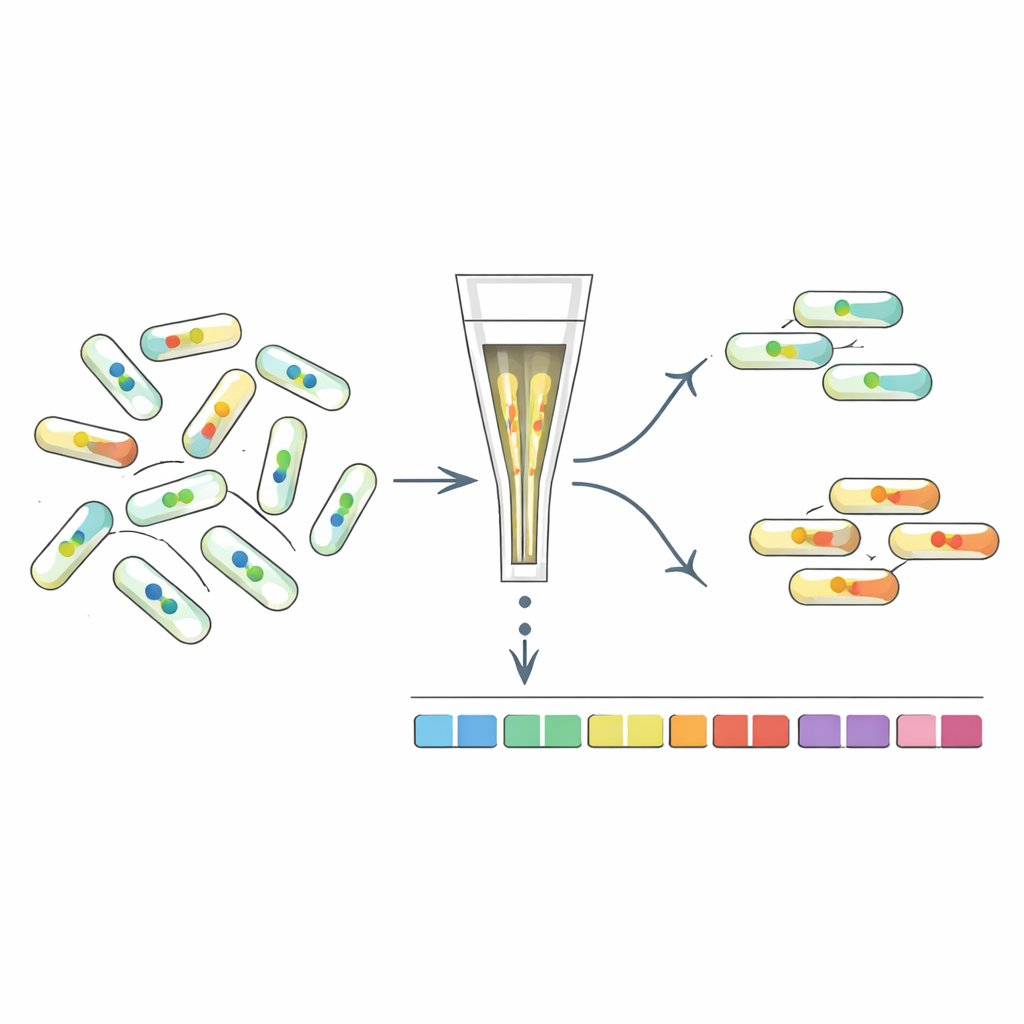
صمَّم المؤلفون مجموعة من مستشعرات البروتين القائمة على FRET، وهي عملية يمكن فيها لبروتين فلوري واحد أن ينقل الطاقة إلى بروتين فلوري آخر عندما يكونان متقاربين للغاية. ربطوا أزواجًا من البروتينات الفلورية الساطعة بمجموعة من بروتينات «القارئ» البكتيرية التي تغير شكلها عند ارتباطها بـ c-di-GMP. اعتمادًا على التصميم، يؤدي هذا التغير في الشكل إما إلى تقريب الزوج الفلوري أو تباعدهما، مما يغيّر إشارة FRET. عبر فحص 90 بروتين قارئ مختلف في Escherichia coli، حدَّدوا 16 مستشعرًا تستجيب بقوة عبر نطاق واسع من تراكيز c-di-GMP، من نحو عشرة مليارات من الجزئ حتى جزء من المليون — ما يغطي المستويات المنخفضة الموجودة عادةً في البكتيريا السابحة والحالات الأعلى في الأغشية الحيوية.
إلقاء نظرة أقرب على الخلايا المفردة
بامتلاك هذا الصندوق، حسَّن الفريق طريقة قياس FRET بالقياس الخلوي التدفقِي (flow cytometry) بحيث تقيس الإشارة بدقة في آلاف الخلايا بالثانية، مصحِّحًا للأخطاء البصرية بحيث يمكن مقارنة النتائج عبر التجارب والمستشعرات. أكدوا قوة الارتباط المقاسة بطريقتين: بنقع خلايا منفذة الغشاء في محاليل c-di-GMP معروفة وباختبار المستشعرات المنقاة في أنابيب اختبار. ثم تابعوا بكتيريا مفردة في قنوات ميكروفلويدية، فوجدوا أن مستويات c-di-GMP تتقلب بقوة من خلية لأخرى ومع الزمن، حتى داخل تجمعات متطابقة جينيًا. أكشفت المستشعرات عالية التقارب فروقًا دقيقة في نطاقات التركيز المنخفضة التي غفلت عنها المستشعرات الأقدم والأضعف إلى حد كبير.
فرز الطفرات حسب إشارتها الداخلية
لفهم الجينات التي تشكّل مستويات c-di-GMP، طوّر الباحثون «FRET-To-Sort»، الذي يربط مستشعراتهم بفحص طفرات عالي الإنتاجية. أدخلوا مستشعرات مختارة إلى مكتبة معنونة بالشيفرات الشريطية تضم عشرات الآلاف من طفرات E. coli، ثم استخدموا جهاز فرز الخلايا لجمع الخلايا ذات إشارات FRET العالية أو المنخفضة بشكل غير اعتيادي، دلالة على تغير في c-di-GMP. كشف تسلسل الشيفرات أي الجينات تعطلت في هذه الحالات الشاذة. كما هو متوقع، تراكمت الطفرات في إنزيمات معروفة مرتبطة بـ c-di-GMP. لكن الفحص أظهر أيضًا العديد من الجينات الأخرى، بما في ذلك تلك المشاركة في غلاف الخلية، الأهداب السطحية، استجابات الإجهاد، وبشكل لافت، المحركات الدوارة التي تدفع السباحة.
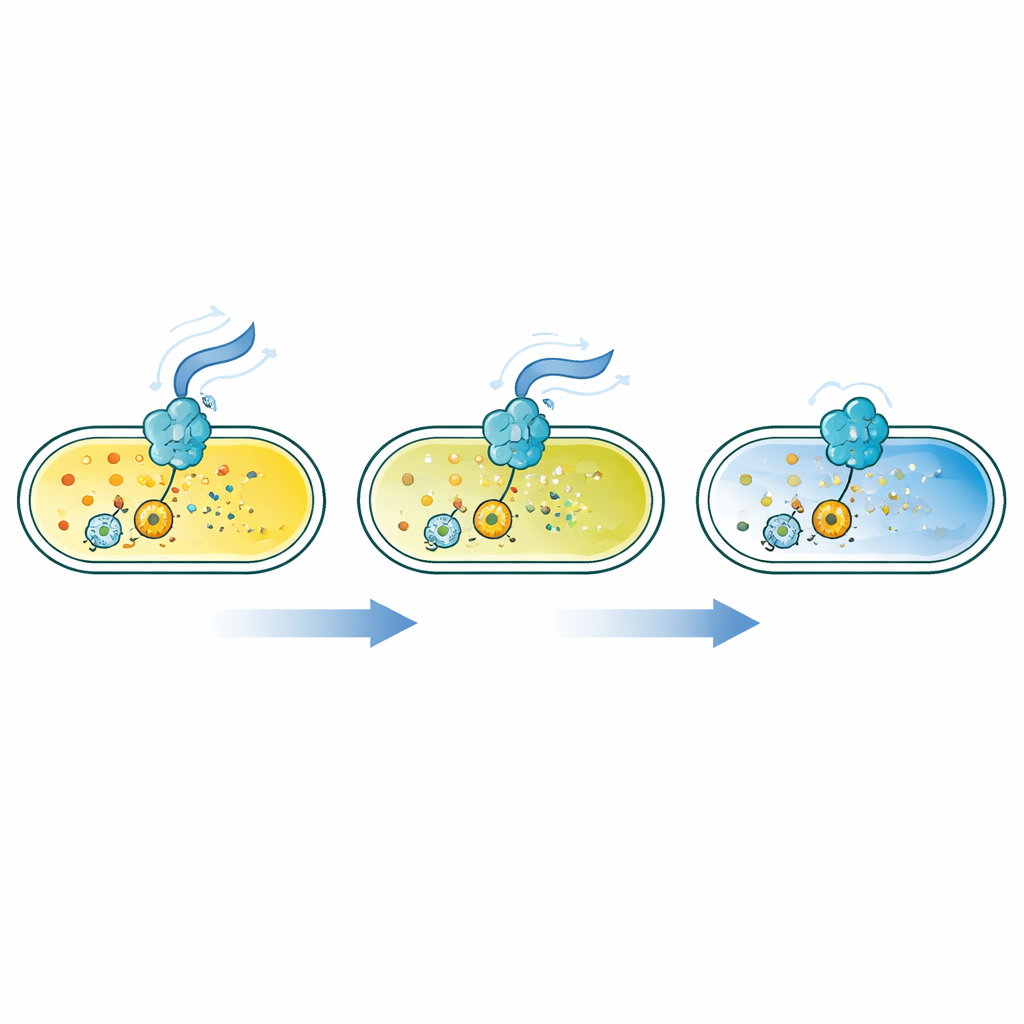
محركات الأهداب كقواعد ضبط إشارة خفية
كشفت التحليلات دورًا مزدوج الوجه لمنظومة الأهداب. الطفرات التي تعوق الخطوات المبكرة في بناء قاعدة الأهداب رفعت مستوى c-di-GMP، لأنها قللت بشكل غير مباشر إنتاج إنزيم رئيسي يحلّل هذا الجزيء. بالمقابل، الطفرات التي عطّلت أجزاء الدوران في المحرك أو أزالت الخيط الخارجي أثّرت بالعكس: خفّضت c-di-GMP. أظهرت تجارب لاحقة أنه عندما لا تستطيع الأهداب الدوران، يرتفع الجهد الغشائي للخلايا — أي الفرق في الجهد عبر الغشاء الخارجي — وهذا الجهد العالي يقمع نشاط إنزيم رئيسي منتج لـ c-di-GMP. انهيار الجهد الغشائي كيميائيًا أعطى التأثير المعاكس، فزاد c-di-GMP. حتى أن تعطل الأهداب ميكانيكيًا بواسطة أجسام مضادة محددة خفّض c-di-GMP، مما يوحي بأن البكتيريا تشعر بحِمل محركاتها وتترجم هذه المعلومة الميكانيكية إلى قرارات تتعلق بنمط حياتها.
ماذا يعني هذا لفهم البكتيريا والتحكم بها
توفر هذه النتائج معًا مجموعة موحدة من مستشعرات c-di-GMP للخلايا الحية واستراتيجية قوية لرسم شبكات الجينات التي تغذي هذا المفتاح المركزي. للمختصين غير المتخصصين، الخلاصة أن البكتيريا لا تستجيب للمواد الكيميائية فحسب؛ بل «تشعر» أيضًا بسهولة دوران مراوحها الدقيقة وتضبط إشاراتها الداخلية وفقًا لذلك. بوصْل الإجهاد الميكانيكي والحالة الكهربائية للغشاء الخلوي بالجزيء الذي يحدد الالتصاق مقابل السباحة، يفتح هذا العمل طرقًا جديدة لفحص وربما تعطيل تكوين الأغشية الحيوية في ميكروبات ذات أهمية طبية وبيئية.
الاستشهاد: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
الكلمات المفتاحية: الرسائل الثانية البكتيرية, تنظيم الأغشية الحيوية, مستشعرات FRET, حركة الأساطيل, فحص الطفرات عبر الجينوم