Clear Sky Science · de
Werkzeugkasten FRET-basierter c-di-GMP-Biosensoren und deren FRET-To-Sort-Anwendung zur genomweiten Kartierung der c-di-GMP-Regulation
Wie Bakterien entscheiden, ob sie kleben oder schwimmen
Bakterien wechseln ständig zwischen freier Fortbewegung und dem Verbleiben in schleimigen Gemeinschaften, den sogenannten Biofilmen — ein Umschalten, das Infektionen, ökologische Kreisläufe und sogar industrielle Beläge prägt. Diese Arbeit stellt neue Werkzeuge vor, mit denen Forschende ein zentrales internes Signal in einzelnen Bakterienzellen in Echtzeit beobachten können, und nutzt sie, um eine überraschende Verbindung zwischen der Drehgeschwindigkeit der winzigen Propeller eines Bakteriums und seiner Entscheidung zum Biofilmbau aufzudecken.
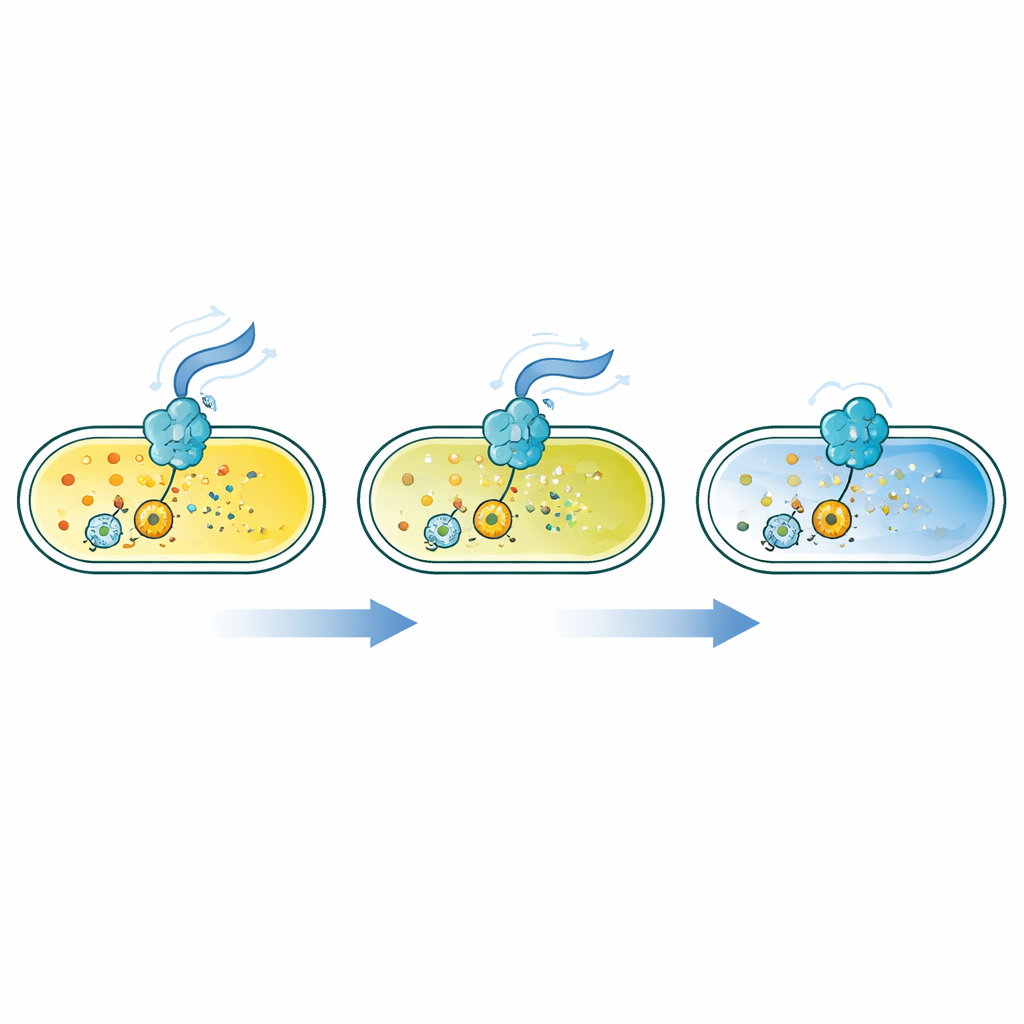
Ein winziges Molekül, das das bakterielle Leben verändert
Viele Bakterien nutzen ein kleines, ringförmiges Molekül, c-di-GMP, als internen Schalter. Niedrige Mengen begünstigen schnelles Schwimmen, während höhere Mengen die Zellen zum Verweilen, Festkleben an Oberflächen und zur Biofilmbildung treiben. Dieses Signal wird von Enzymfamilien hergestellt und abgebaut, die auf Nährstoffe, Sauerstoff, Stress und mehr reagieren. Bisher fehlte jedoch ein einheitlicher Satz empfindlicher, schneller und breit justierbarer Sensoren, um den gesamten Bereich der c-di-GMP-Spiegel in lebenden Zellen zu erfassen — insbesondere bei sehr niedrigen Konzentrationen.
Aufbau eines vielseitigen Farbwechsel-Sensor-Werkzeugkastens
Die Autoren entwickelten eine Familie von Protein-Sensoren auf Basis von FRET, einem Prozess, bei dem ein fluoreszierendes Protein Energie an ein anderes übertragen kann, wenn sie sehr dicht beieinander liegen. Sie fusionierten Paare heller fluoreszierender Proteine mit einer Reihe bakterieller „Leser“-Proteine, die ihre Form ändern, wenn sie c-di-GMP binden. Je nach Konstruktion bringt diese Formänderung das Fluoreszenzpaar näher zusammen oder trennt es, wodurch das FRET-Signal verändert wird. Durch das Screening von 90 verschiedenen Leserproteinen in Escherichia coli identifizierten sie 16 Sensoren, die stark über einen breiten Bereich von c-di-GMP-Konzentrationen ansprechen — von etwa zehn Milliardsteln eines Mols bis zu einem Millionstel — und damit sowohl die niedrigen Spiegel freischwimmender Bakterien als auch die höheren Werte in Biofilmen abdecken.
Einen genaueren Blick auf einzelne Zellen werfen
Mit diesem Werkzeugkasten verbesserten die Forschenden eine Durchflusszytometrie-Methode, die FRET präzise in tausenden Zellen pro Sekunde misst und optische Artefakte korrigiert, sodass Ergebnisse über Experimente und Sensoren hinweg vergleichbar sind. Sie bestätigten die gemessenen Bindungsstärken auf zwei Wegen: indem sie permeabilisierte Zellen in bekannte c-di-GMP-Lösungen einlegten und indem sie gereinigte Sensoren im Reagenzglas testeten. Anschließend verfolgten sie einzelne Bakterien in mikrofluidischen Kanälen und fanden, dass c-di-GMP-Werte stark von Zelle zu Zelle und über die Zeit schwanken, selbst in genetisch identischen Populationen. Hochaffine Sensoren enthüllten feine Unterschiede in diesen niedrigen Konzentrationsbereichen, die ältere, weniger empfindliche Sensoren weitgehend übersahen.
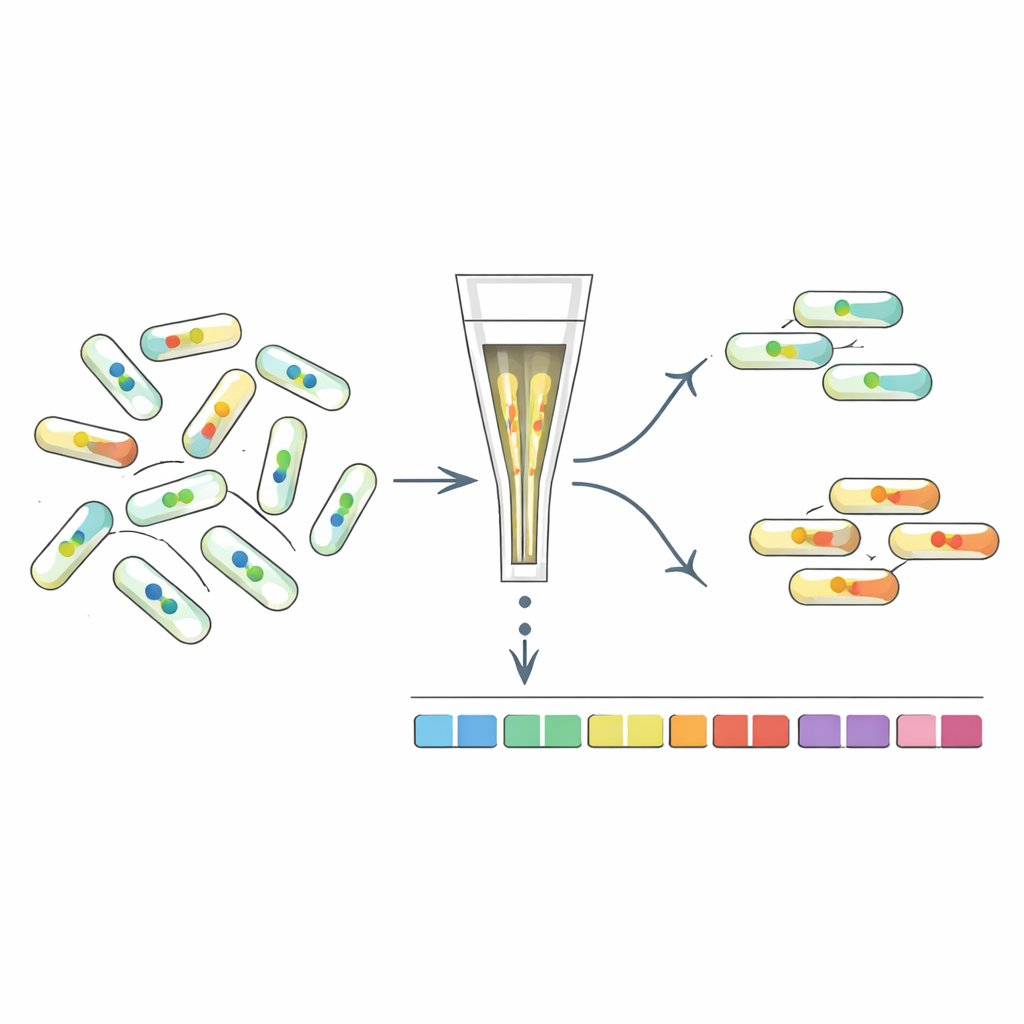
Mutanten nach ihrem internen Signal sortieren
Um zu verstehen, welche Gene die c-di-GMP-Spiegel formen, entwickelten die Forschenden „FRET-To-Sort“, das ihre Sensoren mit einem hochdurchsatzfähigen Mutanten-Screen verknüpft. Sie brachten ausgewählte Sensoren in eine barcodierte Bibliothek von Zehntausenden E. coli-Mutanten ein und nutzten dann einen Zell-Sorter, um Zellen mit ungewöhnlich hohen oder niedrigen FRET-Signalen zu sammeln — ein Hinweis auf verändertes c-di-GMP. Durch Sequenzierung der Barcodes ließ sich feststellen, welche Gene in diesen Ausreißern gestört waren. Wie zu erwarten, waren Mutanten in bekannten c-di-GMP-Enzymen angereichert. Der Screen hob jedoch auch viele andere Gene hervor, darunter solche, die an der Zellhülle, an Fimbrien (haarähnliche Oberflächenfasern), Stressantworten und bemerkenswerterweise an den rotierenden Flagellen, die das Schwimmen antreiben, beteiligt sind.
Flagellarmotoren als verborgene Stellschrauben des Signals
Die Analyse zeigte eine doppelte Rolle des Flagellarsystems. Mutationen, die frühe Schritte beim Aufbau der Flagellenbasis blockieren, erhöhten c-di-GMP, weil sie indirekt die Produktion eines wichtigen abbauenden Enzyms reduzierten. Im Gegensatz dazu hatten Mutationen, die die rotierenden Teile des Motors lahmlegten oder den äußeren Filamentstrang entfernten, den entgegengesetzten Effekt: Sie senkten c-di-GMP. Weitere Experimente zeigten, dass, wenn Flagellen sich nicht drehen können, das Membranpotenzial der Zelle — die Spannung über ihrer äußeren Grenze — ansteigt, und diese höhere Spannung die Aktivität eines wichtigen c-di-GMP-produzierenden Enzyms dämpft. Das chemische Zusammenbrechen des Membranpotenzials hatte den umgekehrten Effekt und erhöhte c-di-GMP. Sogar das physische Verklemmen der Flagellen mit spezifischen Antikörpern reduzierte c-di-GMP, was darauf hindeutet, dass Bakterien spüren, wie stark ihre Motoren belastet sind, und diese mechanische Information in Lebensstilentscheidungen übersetzen.
Was das für das Verständnis und die Kontrolle von Bakterien bedeutet
Zusammen liefern diese Ergebnisse einen standardisierten Satz von Live‑Cell-c-di-GMP-Sensoren und eine leistungsfähige Strategie, um die genetischen Netzwerke zu kartieren, die in diesen zentralen Schalter einfließen. Für Nicht‑Spezialisten ist die wichtigste Erkenntnis, dass Bakterien nicht nur auf chemische Signale reagieren; sie „fühlen“ auch, wie leicht sich ihre winzigen Propeller drehen, und passen ihre internen Signale entsprechend an. Indem mechanische Belastung und elektrischer Zustand der Zellmembran mit dem Molekül verknüpft werden, das Kleben versus Schwimmen steuert, eröffnet diese Arbeit neue Wege, Biofilmbildung bei medizinisch und ökologisch wichtigen Mikroben zu untersuchen und möglicherweise zu stören.
Zitation: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
Schlüsselwörter: bakterielle second messenger, Biofilm-Regulation, FRET-Biosensoren, flagellare Motilität, genomweite Mutanten-Screens