Clear Sky Science · fr
Boîte à outils de biosenseurs c-di-GMP basés sur le FRET et son application FRET-To-Sort pour le cartographage génomique de la régulation du c-di-GMP
Comment les bactéries décident de rester collées ou de nager
Les bactéries oscillent en permanence entre l’exploration libre et l’établissement au sein de communautés visqueuses appelées biofilms ; ce basculement influence les infections, les cycles environnementaux et même l’encrassement industriel. Cet article dévoile de nouveaux outils permettant aux chercheurs d’observer en temps réel un signal interne clé au sein de cellules bactériennes individuelles, et les utilise pour révéler un lien surprenant entre la vitesse de rotation des minuscules propulseurs d’une bactérie et sa décision de former un biofilm.
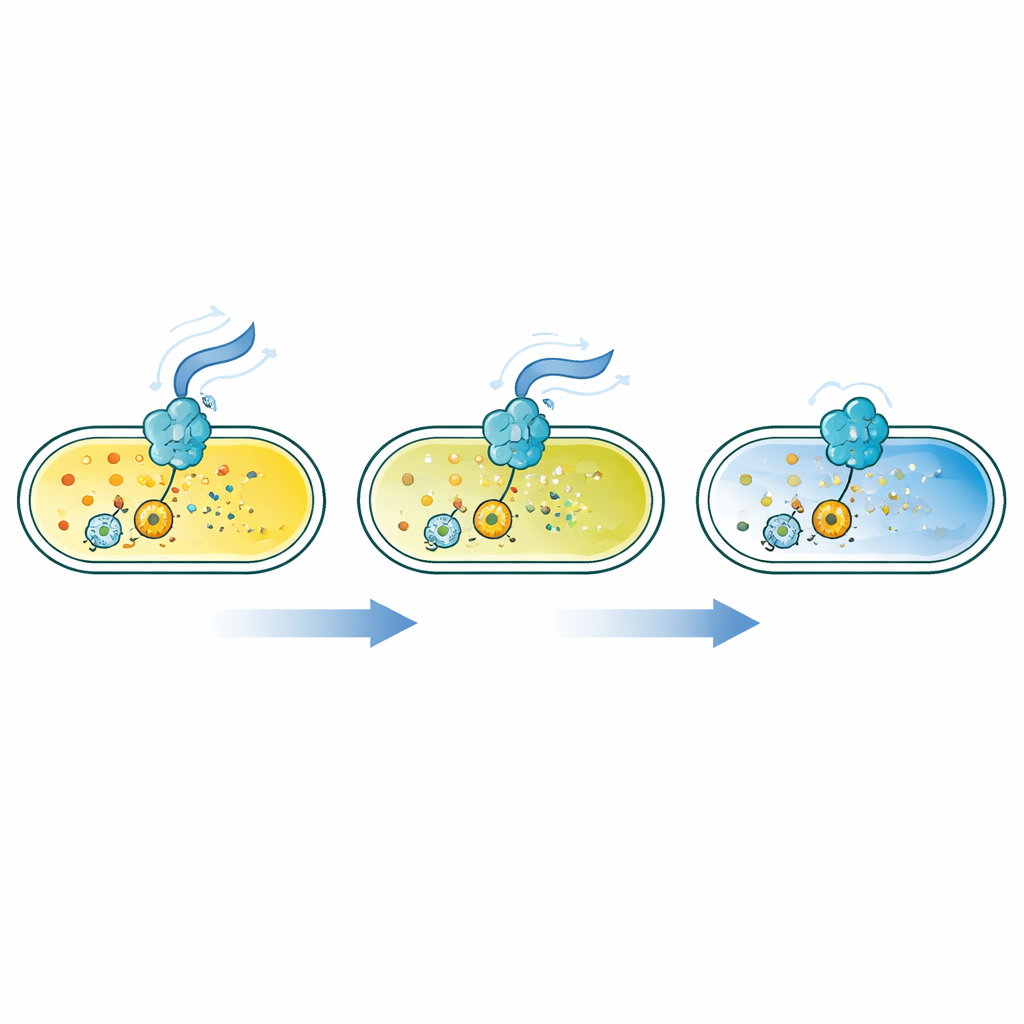
Une petite molécule qui change le mode de vie bactérien
De nombreuses bactéries utilisent une petite molécule cyclique, le c-di-GMP, comme interrupteur interne. De faibles concentrations favorisent une nage rapide, tandis que des concentrations plus élevées poussent les cellules à se fixer aux surfaces et à former des biofilms. Ce signal est produit et dégradé par des familles d’enzymes qui répondent aux nutriments, à l’oxygène, au stress, et plus encore. Jusqu’à présent, cependant, les chercheurs manquaient d’un ensemble unique de capteurs sensibles, rapides et largement modulables pour observer l’intégralité de la plage des niveaux de c-di-GMP à l’intérieur de cellules vivantes, en particulier lorsque la molécule est présente à des concentrations très faibles.
Conception d’une boîte à outils de capteurs à changement de couleur polyvalents
Les auteurs ont conçu une famille de capteurs protéiques basés sur le FRET, un processus où une protéine fluorescente peut transférer de l’énergie à une autre lorsqu’elles sont très proches. Ils ont fusionné des paires de protéines fluorescentes lumineuses à un ensemble de protéines bactériennes « lectrices » qui changent de conformation en se liant au c-di-GMP. Selon la conception, ce changement de forme rapproche la paire fluorescente ou l’éloigne, modifiant ainsi le signal FRET. En criblant 90 protéines lectrices différentes dans Escherichia coli, ils ont identifié 16 capteurs répondant fortement sur une large plage de concentrations de c-di-GMP, de l’ordre de dix milliardièmes de mole jusqu’à un millionième — couvrant les faibles niveaux souvent observés chez les bactéries nageuses libres ainsi que les niveaux plus élevés dans les biofilms.
Examiner de plus près les cellules individuelles
Avec cette boîte à outils, l’équipe a amélioré une méthode de cytométrie en flux capable de mesurer précisément le FRET dans des milliers de cellules par seconde, en corrigeant les artefacts optiques pour que les résultats soient comparables entre expériences et capteurs. Ils ont confirmé les constantes d’affinité mesurées de deux manières : en imprégnant des cellules perméabilisées de solutions de c-di-GMP de concentration connue et en testant des capteurs purifiés en tube. Ils ont ensuite suivi des bactéries individuelles dans des canaux microfluidiques, constatant que les niveaux de c-di-GMP fluctuent fortement d’une cellule à l’autre et au cours du temps, même dans des populations génétiquement identiques. Les capteurs à haute affinité ont révélé des différences subtiles à ces faibles concentrations que les capteurs plus anciens et moins sensibles manquaient largement.
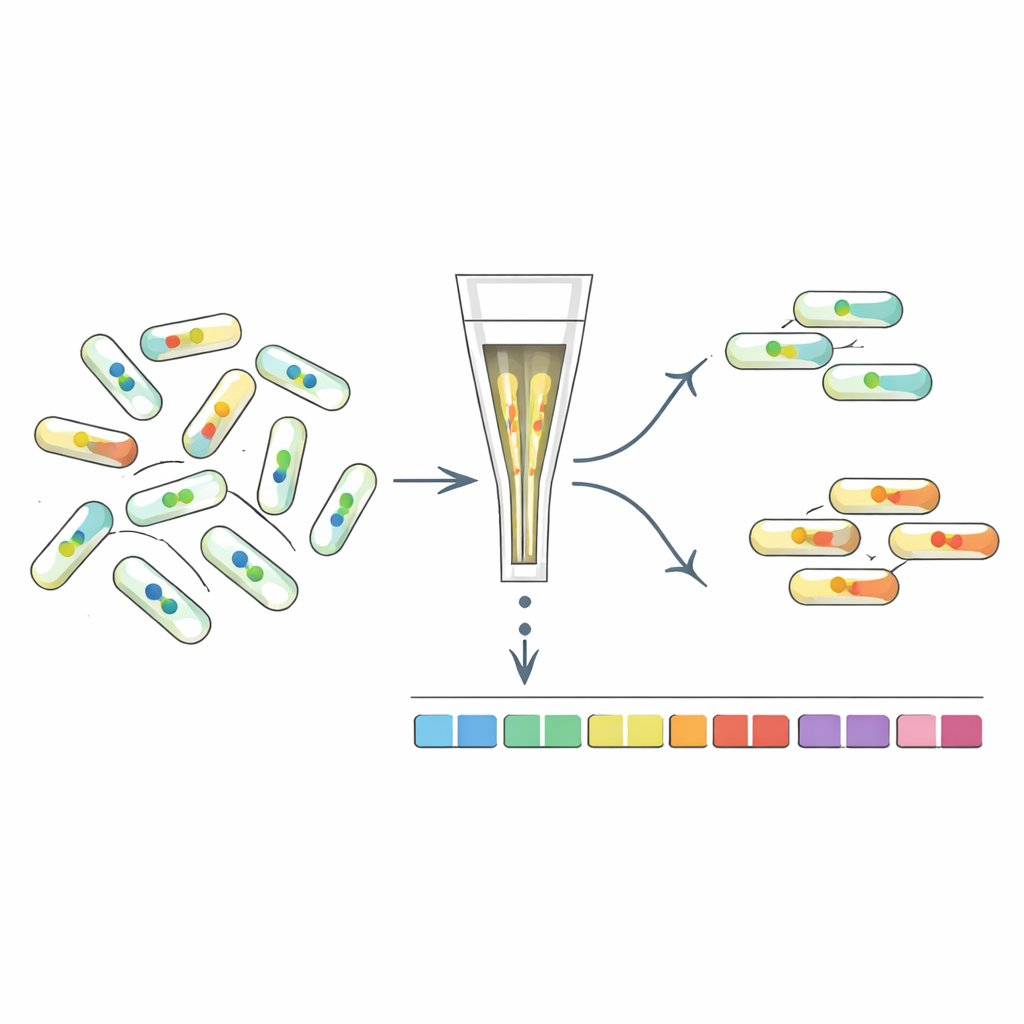
Trier des mutants selon leur signal interne
Pour comprendre quels gènes déterminent les niveaux de c-di-GMP, les chercheurs ont développé « FRET-To-Sort », qui couple leurs capteurs à un criblage de mutants à haut débit. Ils ont introduit des capteurs sélectionnés dans une bibliothèque codée par codes-barres de dizaines de milliers de mutants d’E. coli, puis ont utilisé un trieur de cellules pour collecter celles présentant des signaux FRET anormalement élevés ou faibles, indiquant un c-di-GMP altéré. Le séquençage des codes-barres a révélé quels gènes étaient perturbés dans ces cellules hors normes. Comme prévu, des mutants affectant des enzymes connues du métabolisme du c-di-GMP étaient enrichis. Mais le criblage a aussi mis en évidence de nombreux autres gènes, notamment ceux impliqués dans l’enveloppe cellulaire, les fimbriae (fibres superficielles en forme de poils), les réponses au stress et, de façon frappante, les flagelles rotatifs qui assurent la nage.
Les moteurs flagellaires comme réglages cachés du signal
L’analyse a révélé un rôle ambivalent du système flagellaire. Des mutations bloquant les premières étapes de construction de la base flagellaire augmentaient le c-di-GMP, car elles diminuaient indirectement la production d’une enzyme clé qui dégrade la molécule. En revanche, des mutations qui désactivaient les parties tournantes du moteur ou supprimaient le filament externe avaient l’effet inverse : elles réduisaient le c-di-GMP. Des expériences supplémentaires ont montré que lorsque les flagelles ne peuvent pas tourner, le potentiel de membrane de la cellule — la différence de tension électrique à travers sa membrane — augmente, et cette tension élevée atténue l’activité d’une enzyme majeure productrice de c-di-GMP. L’effondrement chimique du potentiel de membrane avait l’effet inverse, augmentant le c-di-GMP. Même le blocage physique des flagelles avec des anticorps spécifiques réduisait le c-di-GMP, suggérant que les bactéries détectent la charge sur leurs moteurs et traduisent cette information mécanique en décisions de mode de vie.
Ce que cela signifie pour comprendre et contrôler les bactéries
Ensemble, ces résultats fournissent un ensemble standardisé de capteurs de c-di-GMP en cellules vivantes et une stratégie puissante pour cartographier les réseaux génétiques qui alimentent cet interrupteur central. Pour les non-spécialistes, l’essentiel est que les bactéries ne se contentent pas de répondre aux signaux chimiques ; elles « ressentent » aussi la facilité de rotation de leurs minuscules propulseurs et ajustent leurs signaux internes en conséquence. En reliant la contrainte mécanique et l’état électrique de la membrane cellulaire à la molécule qui gouverne le choix entre adhérence et nage, ce travail ouvre de nouvelles voies pour sonder et peut-être perturber la formation de biofilms chez des microbes d’importance médicale et environnementale.
Citation: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
Mots-clés: second messagers bactériens, régulation des biofilms, biosenseurs FRET, motilité flagellaire, dépistage mutanomal à l’échelle du génome