Clear Sky Science · it
Kit di sensori c-di-GMP basati su FRET e la loro applicazione FRET-To-Sort per la mappatura genomica della regolazione di c-di-GMP
Come i batteri decidono se restare attaccati o nuotare
I batteri scelgono continuamente tra muoversi liberamente e stabilirsi in comunità viscose chiamate biofilm, uno switch che influenza infezioni, cicli ambientali e persino l’incrostazione industriale. Questo articolo presenta nuovi strumenti che permettono agli scienziati di osservare un segnale interno chiave in singole cellule batteriche in tempo reale e li usa per rivelare un collegamento sorprendente tra la velocità di rotazione dei minuscoli propulsori di un batterio e la sua decisione di formare biofilm.
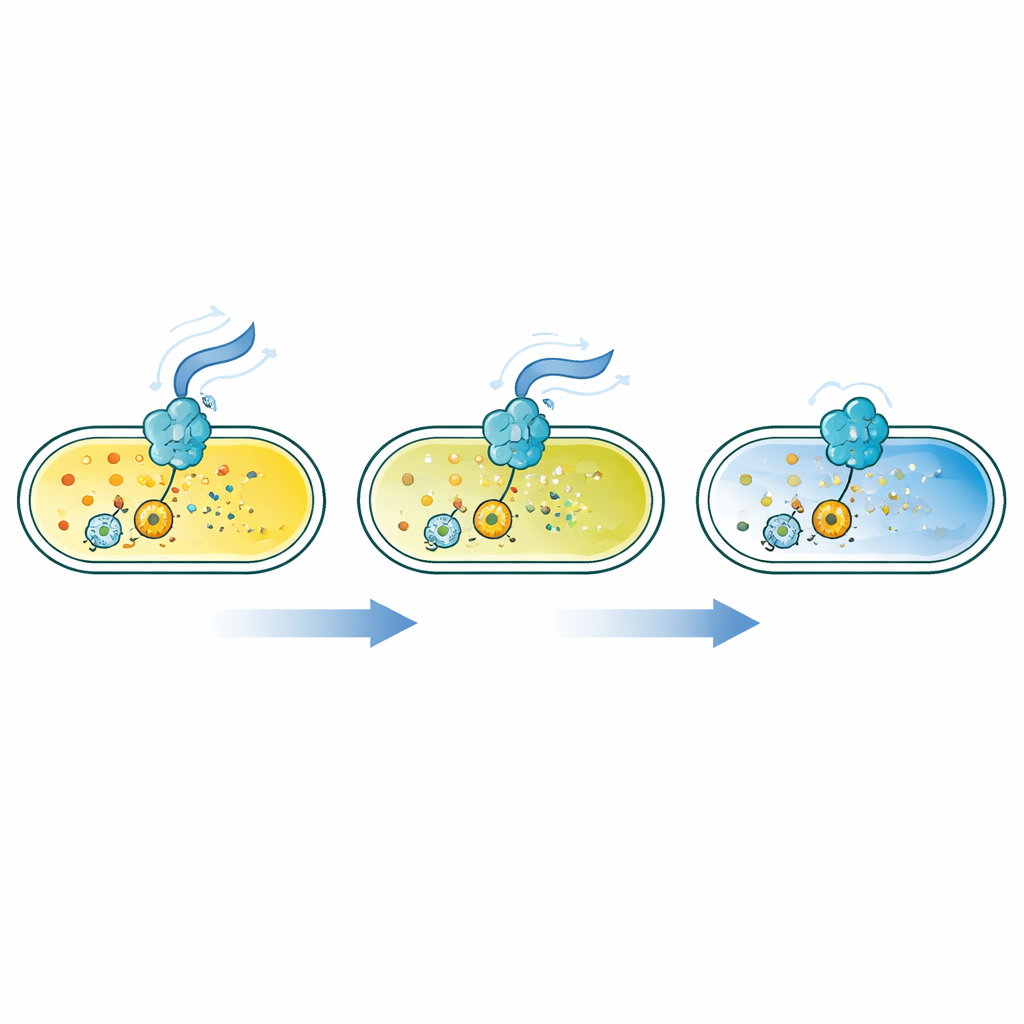
Una piccola molecola che cambia lo stile di vita batterico
Molti batteri fanno affidamento su una piccola molecola ad anello, il c-di-GMP, come interruttore interno. Basse quantità favoriscono una nuotata veloce, mentre quantità più elevate spingono le cellule a stabilirsi, aderire alle superfici e formare biofilm. Questo segnale è sintetizzato e degradato da famiglie di enzimi che rispondono a nutrienti, ossigeno, stress e altro. Finora, però, mancava ai ricercatori un set unico di sensori sensibili, veloci e ampiamente tarabili per osservare l’intera gamma dei livelli di c-di-GMP nelle cellule vive, specialmente quando la molecola è presente a concentrazioni molto basse.
Costruire una cassetta di strumenti sensoriale versatile a cambiamento di colore
Gli autori hanno progettato una famiglia di sensori proteici basati sul FRET, un processo in cui una proteina fluorescente può trasferire energia a un’altra quando sono molto vicine. Hanno fuso coppie di proteine fluorescenti brillanti a una serie di proteine “lettori” batteriche che cambiano forma quando legano il c-di-GMP. A seconda del progetto, questo cambiamento conformazionale o avvicina la coppia fluorescente o la allontana, modificando il segnale FRET. Screenando 90 diversi lettori in Escherichia coli, hanno identificato 16 sensori che rispondono in modo marcato su un ampio intervallo di concentrazioni di c-di-GMP, da circa dieci miliardesimi di mole fino a un milionesimo—coprendo i bassi livelli spesso presenti nei batteri liberi e i livelli più alti nei biofilm.
Osservare più da vicino le singole cellule
Con questa cassetta di strumenti, il team ha migliorato un metodo di citometria a flusso che misura il FRET con precisione in migliaia di cellule al secondo, correggendo gli artefatti ottici in modo che i risultati possano essere confrontati tra esperimenti e sensori. Hanno confermato le affinità di legame misurate in due modi: immergendo cellule permeabilizzate in soluzioni di c-di-GMP a concentrazione nota e testando sensori purificati in provetta. Hanno poi seguito singoli batteri in canali microfluidici, scoprendo che i livelli di c-di-GMP fluttuano fortemente da cellula a cellula e nel tempo, anche in popolazioni geneticamente identiche. Sensori ad alta affinità hanno rivelato differenze sottili in questi intervalli di bassa concentrazione che sensori più vecchi e meno sensibili per lo più non coglievano.
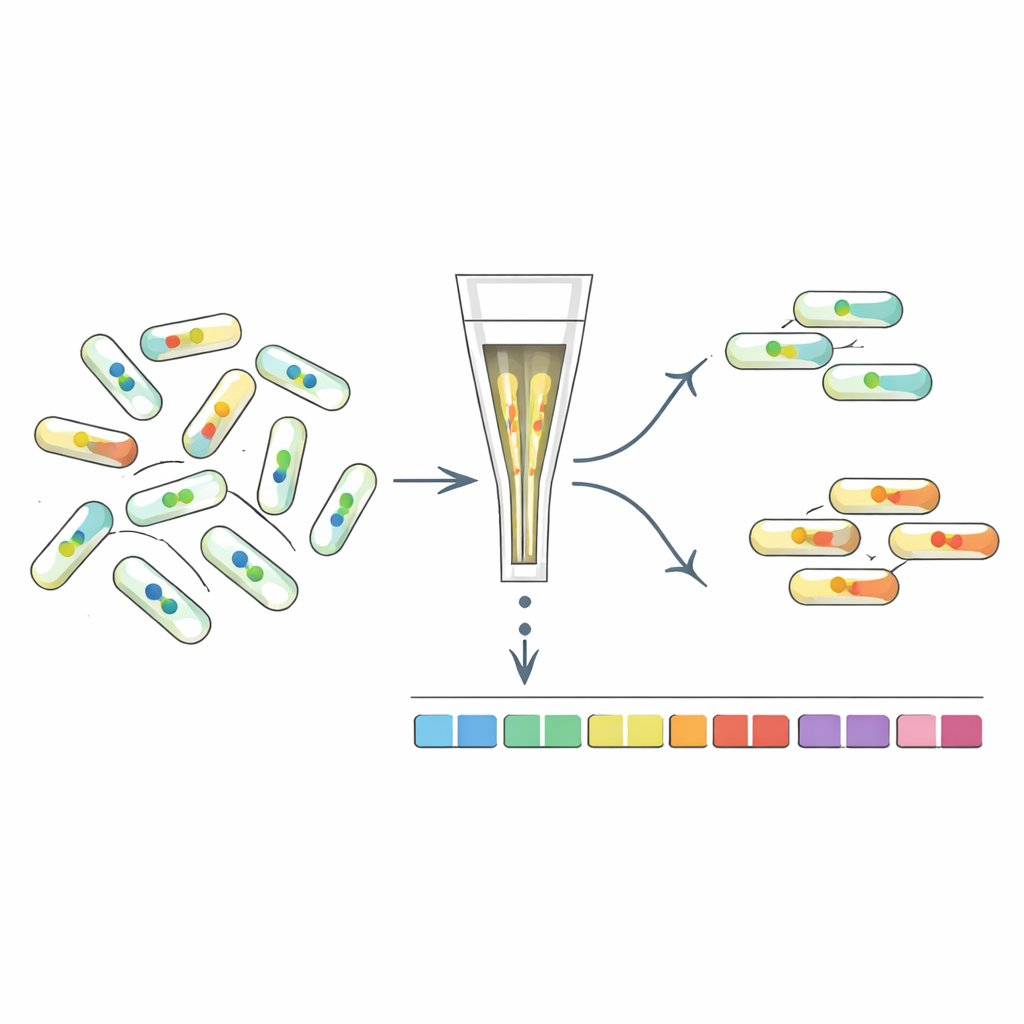
Ordinare i mutanti in base al loro segnale interno
Per capire quali geni modellano i livelli di c-di-GMP, i ricercatori hanno sviluppato “FRET-To-Sort”, che accoppia i loro sensori a uno screening ad alta produttività di mutanti. Hanno introdotto sensori selezionati in una libreria barcode di decine di migliaia di mutanti di E. coli, quindi hanno usato un sorter cellulare per raccogliere cellule con segnali FRET insolitamente alti o bassi, indicatori di c-di-GMP alterato. Il sequenziamento dei barcode ha rivelato quali geni erano interrotti in questi outlier. Come previsto, i mutanti negli enzimi noti per gestire il c-di-GMP risultavano arricchiti. Ma lo screening ha anche evidenziato molti altri geni, inclusi quelli coinvolti nell’involucro cellulare, nelle fimbrie (fibre superficiali simili a peli), nelle risposte allo stress e, in modo sorprendente, nei flagelli rotanti che alimentano il nuoto.
I motori flagellari come manopole nascoste del segnale
L’analisi ha messo in luce un ruolo duplice per il sistema flagellare. Mutazioni che bloccano i primi passaggi nella costruzione della base flagellare aumentavano il c-di-GMP, perché indirettamente riducevano la produzione di un enzima chiave che degrada la molecola. Al contrario, mutazioni che disabilitavano le parti rotanti del motore o rimuovevano il filamento esterno avevano l’effetto opposto: riducevano il c-di-GMP. Ulteriori esperimenti hanno mostrato che quando i flagelli non possono ruotare, il potenziale di membrana della cellula—la tensione attraverso il suo confine esterno—aumenta, e questo alto voltaggio smorza l’attività di un importante enzima che produce c-di-GMP. L’induzione chimica del collasso del potenziale di membrana aveva l’effetto inverso, aumentando il c-di-GMP. Anche l’inceppamento fisico dei flagelli con anticorpi specifici riduceva il c-di-GMP, suggerendo che i batteri percepiscono il carico sui loro motori e traducono questa informazione meccanica in decisioni sullo stile di vita.
Cosa significa per comprendere e controllare i batteri
Nel complesso, questi risultati forniscono un set standardizzato di sensori per c-di-GMP in cellule vive e una strategia potente per mappare le reti genetiche che confluenzano in questo interruttore centrale. Per il pubblico non specialista, il punto chiave è che i batteri non rispondono solo a segnali chimici; essi «sentono» anche quanto facilmente girano i loro minuscoli propulsori e regolano di conseguenza i segnali interni. Collegando la sollecitazione meccanica e lo stato elettrico della membrana cellulare alla molecola che governa l’aderenza rispetto al nuoto, questo lavoro apre nuove vie per sondare e forse interrompere la formazione di biofilm in microrganismi di rilevanza medica e ambientale.
Citazione: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
Parole chiave: secondi messaggeri batterici, regolazione dei biofilm, sensori FRET, motilità flagellare, screening genomico di mutanti