Clear Sky Science · tr
FRET tabanlı c-di-GMP biyosensörlerinin araç kutusu ve genom çapında c-di-GMP regülasyonunun haritalanması için FRET-To-Sort uygulaması
Bakteri Yapışmaya mı Yüzmeye mi Karar Veriyor?
Bakteriler sürekli olarak özgürce dolaşmak ile yapışkan topluluklar olan biyo-filmlere yerleşmek arasında seçim yapar; bu geçiş enfeksiyonları, çevresel döngüleri ve endüstriyel kirlenmeyi şekillendirir. Bu makale, bilim insanlarının tek tek bakteri hücrelerinde kilit bir iç sinyali gerçek zamanlı izlemelerini sağlayan yeni araçları ortaya koyuyor ve bunları kullanarak bir bakterinin küçük pervanelerinin ne kadar hızlı döndüğü ile biyo-film kurma kararı arasında şaşırtıcı bir bağlantı keşfediyor.
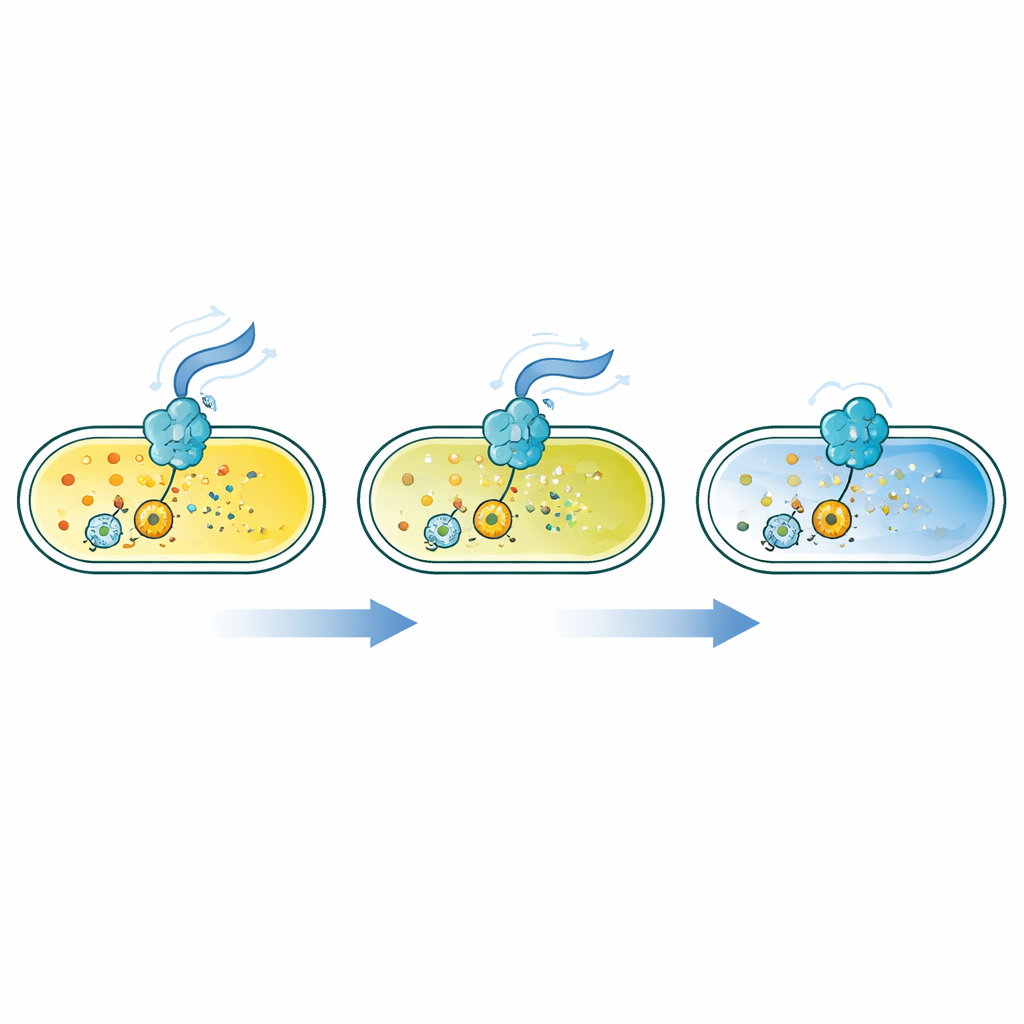
Bakteriyel Yaşam Biçimlerini Değiştiren Küçük Bir Molekül
Birçok bakteri, c-di-GMP adlı küçük halka yapılı bir molekülü içsel bir anahtar olarak kullanır. Düşük düzeyler hızlı yüzmeyi desteklerken, daha yüksek düzeyler hücreleri yerleşmeye, yüzeylere yapışmaya ve biyo-filmler oluşturmaya yönlendirir. Bu sinyal, besinler, oksijen, stres ve daha fazlasına yanıt veren enzim aileleri tarafından üretilir ve parçalanır. Ancak şimdiye dek, araştırmacıların yaşayan hücreler içinde c-di-GMP düzeylerinin tam aralığını, özellikle molekülün çok düşük konsantrasyonlarda bulunduğu durumları görmelerini sağlayan tek bir hassas, hızlı ve genişçe ayarlanabilir sensör seti eksikti.
Çok Yönlü Bir Renk Değiştiren Sensör Araç Kutusu İnşa Etmek
Yazarlar, FRET'e dayalı bir protein sensör ailesi tasarladılar; bu süreçte bir floresan protein yakın konumlandığında enerjiyi diğerine aktarır. Parlak floresan protein çiftlerini, c-di-GMP bağlandığında şekil değiştiren bakteri "okuyucu" proteinlere birleştirdiler. Tasarıma bağlı olarak bu şekil değişimi floresan çiftini ya birbirine daha da yaklaştırıyor ya da uzaklaştırıyor ve böylece FRET sinyalini değiştiriyordu. Escherichia coli içinde 90 farklı okuyucu proteini tarayarak, yaklaşık on milyarda bir molden (10^-10 M) bir milyonda bire (10^-6 M) kadar geniş bir c-di-GMP konsantrasyon aralığında güçlü yanıt veren 16 sensör tanımladılar—serbest yüzen bakterilerde sık görülen düşük düzeyleri ve biyo-filmlerdeki daha yüksek düzeyleri kapsayacak şekilde.
Tek Hücreleri Daha Yakından İncelemek
Bu araç kutusuyla ekip, saniyede binlerce hücrede FRET'i hassas biçimde ölçen akış sitometrisi yöntemini geliştirdi; optik artefaktları düzelterek sonuçların deneyler ve sensörler arasında karşılaştırılabilmesini sağladılar. Ölçülen bağlanma güçlerini iki şekilde doğruladılar: geçirgenleştirilmiş hücreleri bilinen c-di-GMP çözeltilerine batırarak ve saflaştırılmış sensörleri test tüplerinde deneyerek. Ardından mikroakışkan kanallarda bireysel bakterileri izlediler ve c-di-GMP düzeylerinin hücreden hücreye ve zaman içinde güçlü dalgalanmalar gösterdiğini, genetik olarak aynı popülasyonlarda bile değişim olduğunu buldular. Yüksek afiniteli sensörler, daha eski ve daha zayıf sensörlerin büyük ölçüde kaçırdığı bu düşük konsantrasyon aralıklarındaki ince farkları ortaya koydu.
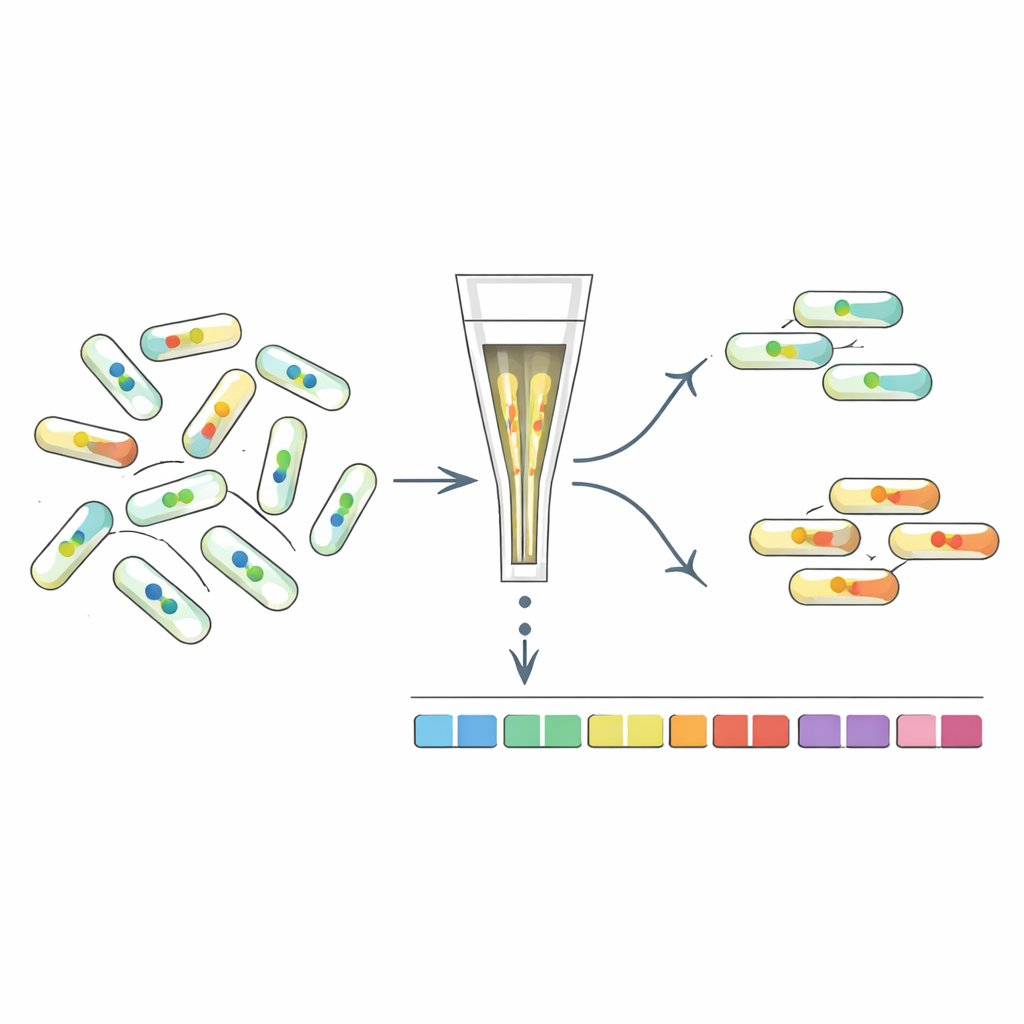
İç Sinyale Göre Mutantları Sıralamak
c-di-GMP düzeylerini hangi genlerin şekillendirdiğini anlamak için araştırmacılar sensörlerini yüksek verimli mutant taramasıyla birleştiren "FRET-To-Sort" yöntemini geliştirdiler. Seçilen sensörleri on binlerce barkodlu E. coli mutantından oluşan bir kütüphaneye soktular, sonra bir hücre sıralayıcı kullanarak olağanüstü yüksek veya düşük FRET sinyali gösteren hücreleri topladılar; bu, altere olmuş c-di-GMP'yi işaret ediyordu. Barkodları dizileyerek bu uç örneklerde hangi genlerin bozulduğunu tespit ettiler. Beklendiği gibi, bilinen c-di-GMP enzimlerindeki mutasyonlar zenginleşti. Ancak tarama ayrıca birçok başka geni de vurguladı; bunlar arasında hücre zarfıyla ilgili genler, fimbrialar (kıl benzeri yüzey lifleri), stres yanıtları ve dikkat çekici biçimde yüzmeyi sağlayan döner kamçılar yer aldı.
Kamçı Motorları Gizli Sinyal Ayarları Olarak
Analiz, kamçı sisteminin iki yönlü bir rolünü açığa çıkardı. Kamçının tabanının inşasında erken adımları engelleyen mutasyonlar c-di-GMP'yi artırdı; bunun nedeni dolaylı olarak molekülü parçalayan anahtar bir enzimin üretimini düşürmeleriydi. Buna karşılık, motorun dönen parçalarını devre dışı bırakan veya dış filamentleri çıkaran mutasyonlar ters etki gösterdi: c-di-GMP'yi düşürdü. İleri deneyler, kamçalar döndürülemediğinde hücre zar potansiyelinin—dış sınırı boyunca oluşan voltajın—yükseldiğini ve bu yüksek voltajın büyük bir c-di-GMP üreten enzimin aktivitesini bastırdığını gösterdi. Zar potansiyelini kimyasal olarak çökertmek ters etki yaptı ve c-di-GMP'yi artırdı. Hatta kamçıları spesifik antikorlarla fiziksel olarak sıkıştırmak bile c-di-GMP'yi azalttı; bu, bakterilerin motorlarının yük altında olup olmadığını hissettiğini ve bu mekanik bilgiyi yaşam biçimi kararlarına çevirdiğini düşündürüyor.
Bu, Bakterileri Anlamak ve Kontrol Etmek İçin Ne Anlama Geliyor?
Birlikte ele alındığında, bu sonuçlar canlı hücre c-di-GMP sensörlerinin standart bir setini ve bu merkezi anahtara girdi sağlayan genetik ağları haritalamak için güçlü bir stratejiyi sunuyor. Uzman olmayanlar için temel çıkarım şudur: bakteriler sadece kimyasallara tepki vermez; aynı zamanda küçük pervanelerinin ne kadar kolay döndüğünü “hisseder” ve iç sinyallerini buna göre ayarlar. Hücre zarındaki mekanik gerilim ve elektriksel durumu, yapışma ile yüzmeyi yöneten moleküle bağlayarak bu çalışma biyo-film oluşumunu incelemek ve belki de tıp ve çevre açısından önemli mikroplarda engellemek için yeni yollar açıyor.
Atıf: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
Anahtar kelimeler: bakteriyel ikinci haberci moleküller, biyofilm düzenlemesi, FRET biyosensörleri, kamçı hareketliliği, genom çapında mutant taraması