Clear Sky Science · pl
Zestaw czujników biosensorowych FRET dla c-di-GMP i zastosowanie FRET-To-Sort do mapowania regulacji c-di-GMP w skali genomu
Jak bakterie decydują, kiedy przylgnąć, a kiedy pływać
Bakterie nieustannie wybierają między swobodnym przemieszczaniem się a osiedlaniem w śliskich skupiskach zwanych biofilmami — przełączenie to kształtuje przebieg zakażeń, cykle środowiskowe, a nawet zanieczyszczenia w przemyśle. W artykule przedstawiono nowe narzędzia, które pozwalają naukowcom obserwować kluczowy wewnętrzny sygnał w pojedynczych komórkach bakteryjnych w czasie rzeczywistym, oraz wykorzystano je do ujawnienia zaskakującego związku między siłą obrotu mikrośmigieł bakterii a ich decyzją o tworzeniu biofilmów.
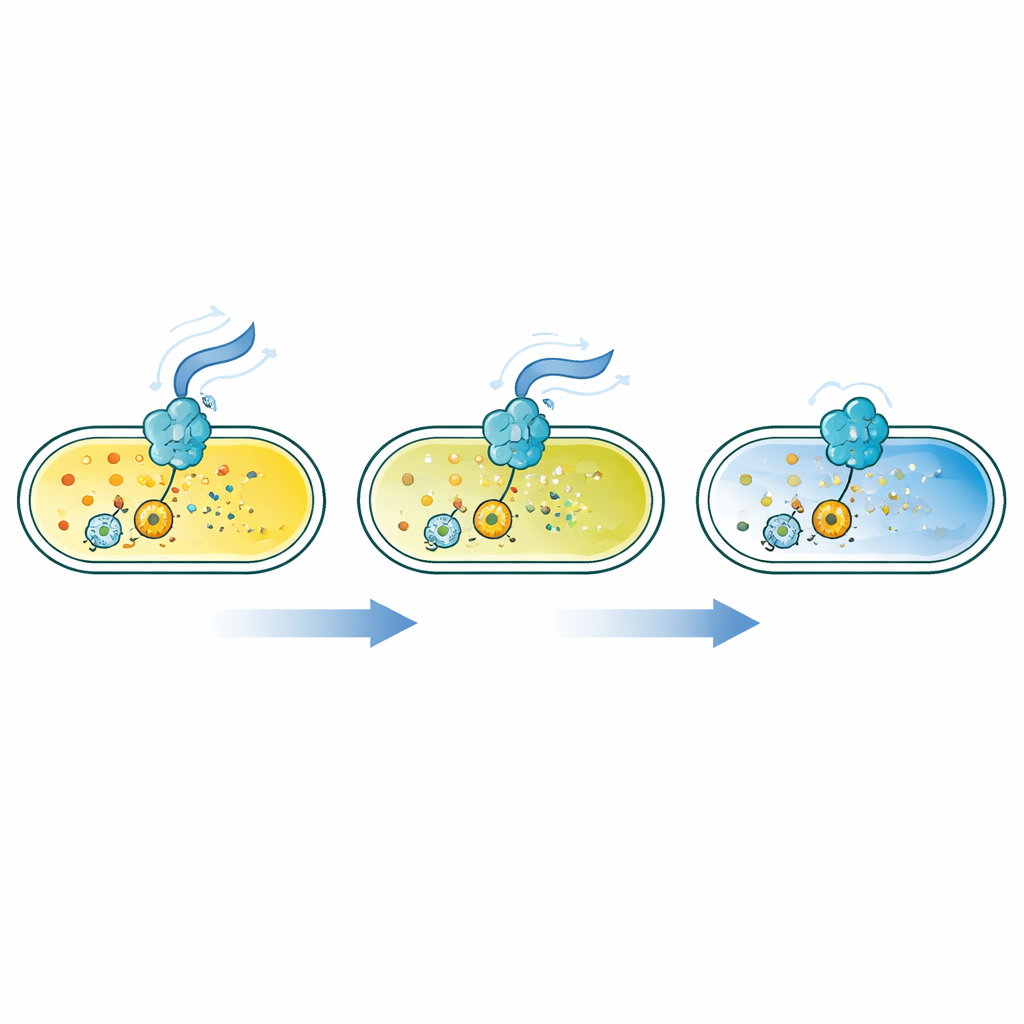
Maleńka cząsteczka, która zmienia styl życia bakterii
Wiele bakterii polega na małej pierścieniowej cząsteczce, c-di-GMP, jako wewnętrznym przełączniku. Niskie stężenia sprzyjają szybszemu pływaniu, podczas gdy wyższe skłaniają komórki do osiadania, przylegania do powierzchni i tworzenia biofilmów. Ten sygnał jest syntetyzowany i rozkładany przez rodziny enzymów reagujących na dostępność składników odżywczych, tlen, stres i inne czynniki. Do tej pory jednak badaczom brakowało jednego zestawu czułych, szybkich i szeroko regulowanych czujników, które pozwoliłyby zobaczyć pełen zakres poziomów c-di-GMP w żywych komórkach, zwłaszcza gdy cząsteczka występuje w bardzo niskich stężeniach.
Budowa wszechstronnego zestawu czujników zmieniających barwę
Autorzy zaprojektowali rodzinę białkowych czujników opartych na FRET — procesie, w którym jedno białko fluorescencyjne może przekazywać energię drugiemu, gdy znajdują się bardzo blisko siebie. Połączyli pary jasnych białek fluorescencyjnych z zestawem bakteryjnych „czytników”, które zmieniają kształt po związaniu c-di-GMP. W zależności od konstrukcji ta zmiana konformacji albo przybliża parę fluorescencyjną, albo ją rozsuwa, zmieniając sygnał FRET. Poprzez screening 90 różnych czytników w Escherichia coli zidentyfikowali 16 czujników, które reagują silnie w szerokim zakresie stężeń c-di-GMP — od około dziesięciu miliardowych mola do jednego milionowego — obejmując niskie poziomy typowe dla swobodnie pływających bakterii oraz wyższe poziomy w biofilmach.
Bliższe spojrzenie na pojedyncze komórki
Dysponując tym zestawem, zespół udoskonalił metodę cytometrii przepływowej, która precyzyjnie mierzy FRET w tysiącach komórek na sekundę, koregując optyczne artefakty tak, by wyniki mogły być porównywane między eksperymentami i czujnikami. Potwierdzili siłę wiązania w dwóch podejściach: poprzez zanurzenie przepuszczalnionych komórek w roztworach o znanym stężeniu c-di-GMP oraz testując oczyszczone czujniki w probówkach. Następnie śledzili pojedyncze bakterie w kanałach mikroprzepływowych, odkrywając, że poziomy c-di-GMP silnie fluktuują między komórkami i w czasie, nawet w genetycznie identycznych populacjach. Czujniki o wysokim powinowactwie ujawniły subtelne różnice na tych niskich zakresach stężeń, które starsze, słabsze czujniki w dużej mierze pomijały.
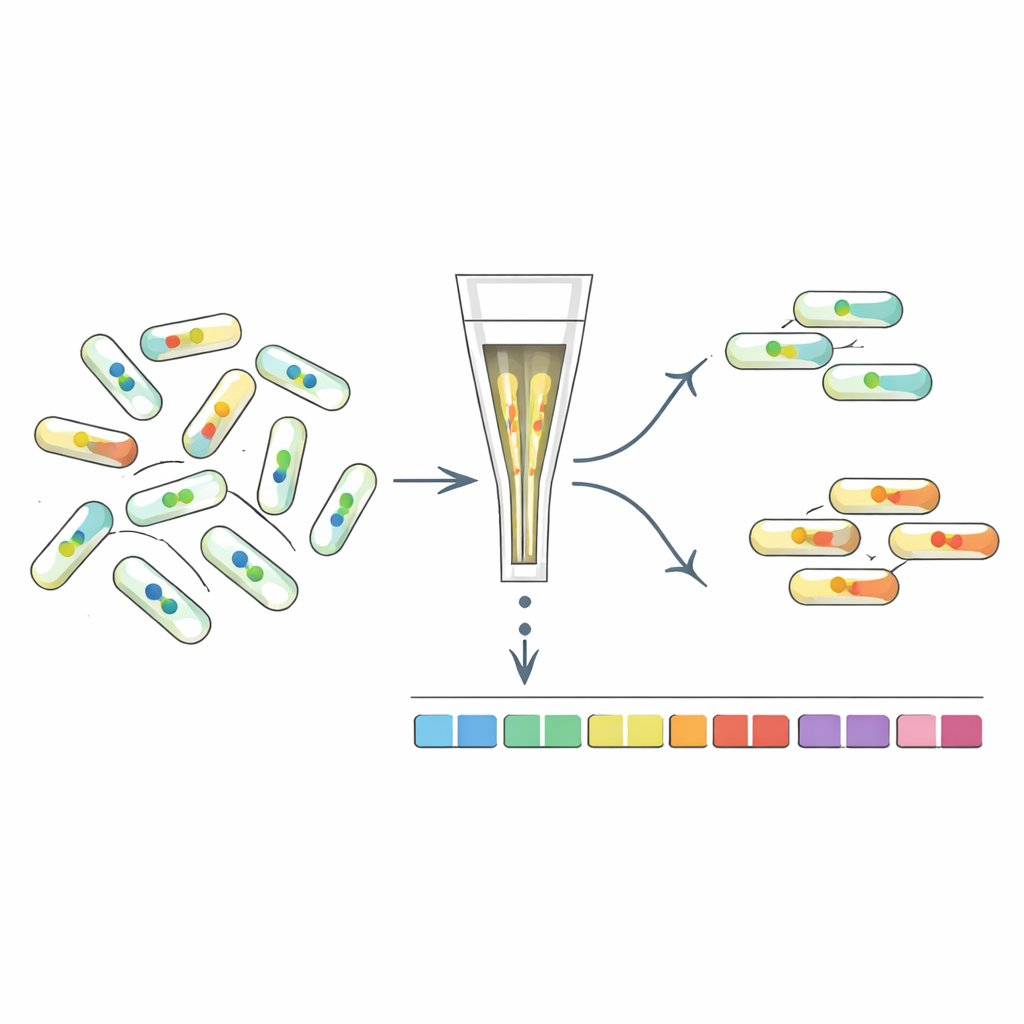
Sortowanie mutantów według ich wewnętrznego sygnału
Aby zrozumieć, jakie geny kształtują poziomy c-di-GMP, badacze opracowali „FRET-To-Sort”, łączący ich czujniki z wysokoprzepustowym screenowaniem mutantów. Wprowadzili wybrane czujniki do bibliotek z oznakowanymi kodami kreskowymi dziesiątek tysięcy mutantów E. coli, a następnie użyli sortera komórek, aby zebrać komórki o nietypowo wysokich lub niskich sygnałach FRET, wskazujących na zmienione stężenia c-di-GMP. Sekwencjonowanie kodów kreskowych ujawniło, które geny były zaburzone u tych odstających komórek. Jak można było oczekiwać, wzbogaciły się mutanty w znanych enzymach związanych z c-di-GMP. Jednak screening wyróżnił również wiele innych genów, w tym te związane z otoczką komórkową, fimbriae (włosopodobne włókna powierzchniowe), odpowiedziami na stres oraz, co uderzające, z obrotową wicią napędzającą ruch.
Silniki wici jako ukryte regulatory sygnału
Analiza ujawniła dwoistą rolę systemu wici. Mutacje blokujące wczesne etapy budowy podstawy wici podnosiły poziom c-di-GMP, ponieważ pośrednio obniżały produkcję kluczowego enzymu rozkładającego tę cząsteczkę. Natomiast mutacje wyłączające obracające się części silnika lub usuwające zewnętrzny filament działały przeciwnie: obniżały c-di-GMP. Dalsze eksperymenty pokazały, że gdy wici nie mogą się obracać, potencjał błony komórkowej — napięcie na granicy komórki — rośnie, a wysokie napięcie tłumi aktywność głównego enzymu produkującego c-di-GMP. Chemiczne zniszczenie potencjału błonowego miało odwrotny skutek, zwiększając c-di-GMP. Nawet fizyczne zablokowanie wici przy pomocy specyficznych przeciwciał obniżało poziom c-di-GMP, co sugeruje, że bakterie wyczuwają obciążenie swoich silników i przekładają tę informację mechaniczną na decyzje dotyczące stylu życia.
Co to oznacza dla zrozumienia i kontroli bakterii
W sumie wyniki dostarczają standaryzowanego zestawu czujników c-di-GMP do pracy na żywych komórkach oraz potężnej strategii mapowania sieci genetycznych zasilających ten centralny przełącznik. Dla osób spoza specjalności kluczowym wnioskiem jest to, że bakterie nie reagują jedynie na związki chemiczne; one także „czują”, jak łatwo obracają się ich maleńkie śmigiełka i dostosowują swoje wewnętrzne sygnały odpowiednio. Powiązanie naprężenia mechanicznego i stanu elektrycznego błony komórkowej z molekułą rządzącą przywieraniem versus pływaniem otwiera nowe drogi do badania, a potencjalnie do zakłócania, tworzenia biofilmów w mikrobach istotnych medycznie i środowiskowo.
Cytowanie: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
Słowa kluczowe: bakteryjne drugi komunikatory, regulacja biofilmów, biosensory FRET, ruchliwość za pomocą wici, screening mutantów w skali genomu