Clear Sky Science · ja
FRETベースのc-di-GMPバイオセンサーのツールボックスとゲノム全体でのc-di-GMP制御マッピングのためのFRET-To-Sortアプリケーション
細菌はいつ定着し、いつ泳ぐと決めるのか
細菌は常に自由に泳ぎ回るか、粘性のあるコミュニティであるバイオフィルムに定着するかを選択しており、この切り替えは感染、環境サイクル、産業的な付着汚れに影響します。本論文は、単一細胞内の重要な内部シグナルをリアルタイムで観察できる新しいツールを示し、それらを用いて細菌の小さな推進器の回転の強さとバイオフィルム形成の意思決定との意外な関連を明らかにします。
細菌の生活様式を変える小さな分子
多くの細菌は、環状の小分子であるc-di-GMPを内部のスイッチとして利用しています。濃度が低いと迅速な泳動が促進され、一方で濃度が高くなると細胞は表面への付着や定着、バイオフィルム形成へと傾きます。このシグナルは栄養、酸素、ストレスなどに応答する酵素群によって合成・分解されます。しかしこれまで、生きた細胞内での非常に低濃度を含むc-di-GMPの全範囲を感度高く・迅速に・広く調整可能に可視化できる、単一のセンサー群は存在していませんでした。
多用途の色変化センサーの構築
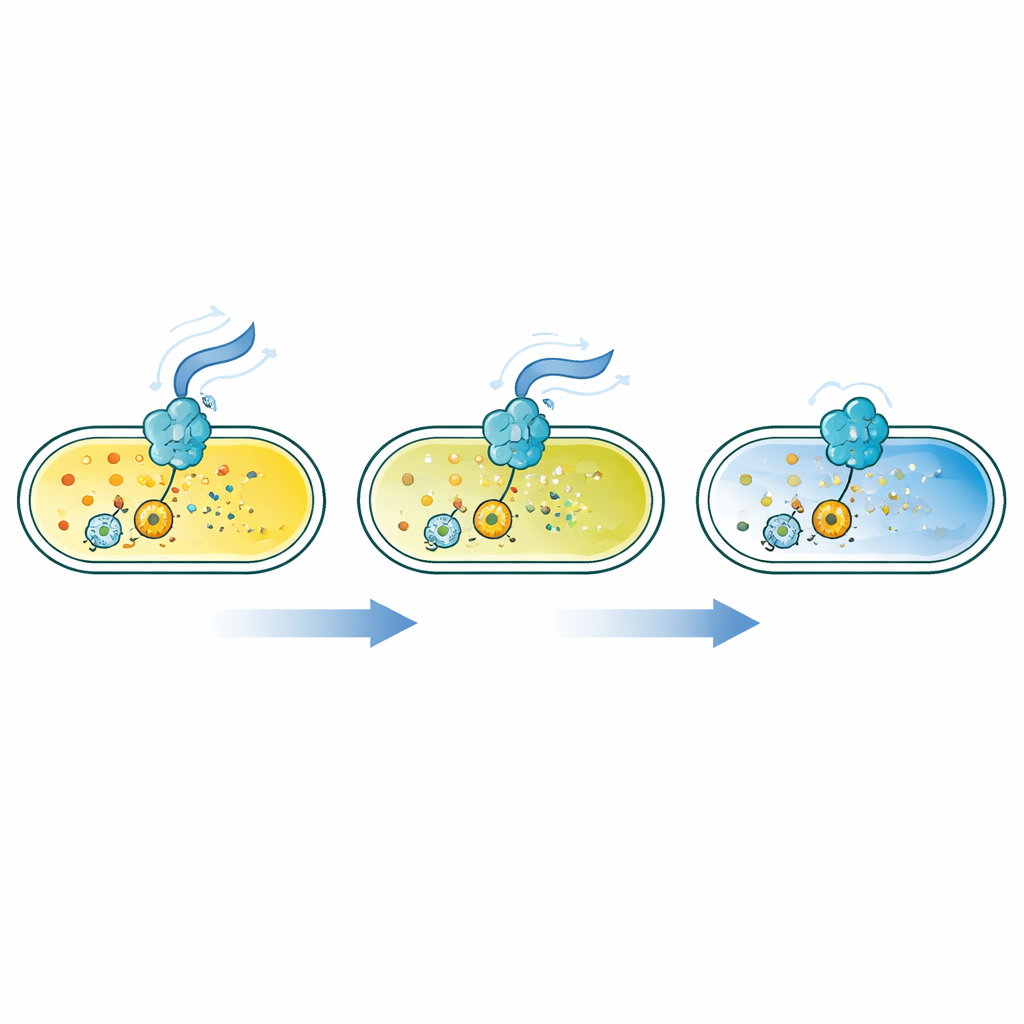
著者らはFRET(励起エネルギーの一方の蛍光タンパク質から他方へ近接時に移動する現象)に基づく一連のタンパク質センサーを設計しました。彼らは明るい蛍光タンパク質の対を、c-di-GMP結合で形を変える一連の細菌由来“リーダー”タンパク質に融合しました。設計により、その形変化が蛍光対を近づけるか離すかを決め、FRET信号が変化します。90種類のリーダータンパク質をEscherichia coliでスクリーニングすることで、約10^-10モルから10^-6モルという広いc-di-GMP濃度範囲で強く応答する16個のセンサーを特定しました。これは自由泳動細菌で見られる低濃度からバイオフィルムでの高濃度までをカバーします。
単一細胞をより詳しく見る
このツールボックスを用いて、チームは毎秒数千個の細胞でFRETを正確に測定するフローサイトメトリー法を改良し、光学的アーティファクトを補正して実験やセンサー間で結果を比較可能にしました。結合強度の測定は二通りで確認されました:透過化した細胞を既知のc-di-GMP溶液に浸す方法と、精製したセンサーを試験管内で測る方法です。次にマイクロフルイディクスチャネル内の個々の細菌を追跡したところ、遺伝的に同一の集団でも細胞ごとおよび時間経過でc-di-GMPレベルが大きく変動することが見いだされました。高親和性センサーは、従来の弱いセンサーではほとんど捉えられなかった低濃度域の微妙な違いを明らかにしました。
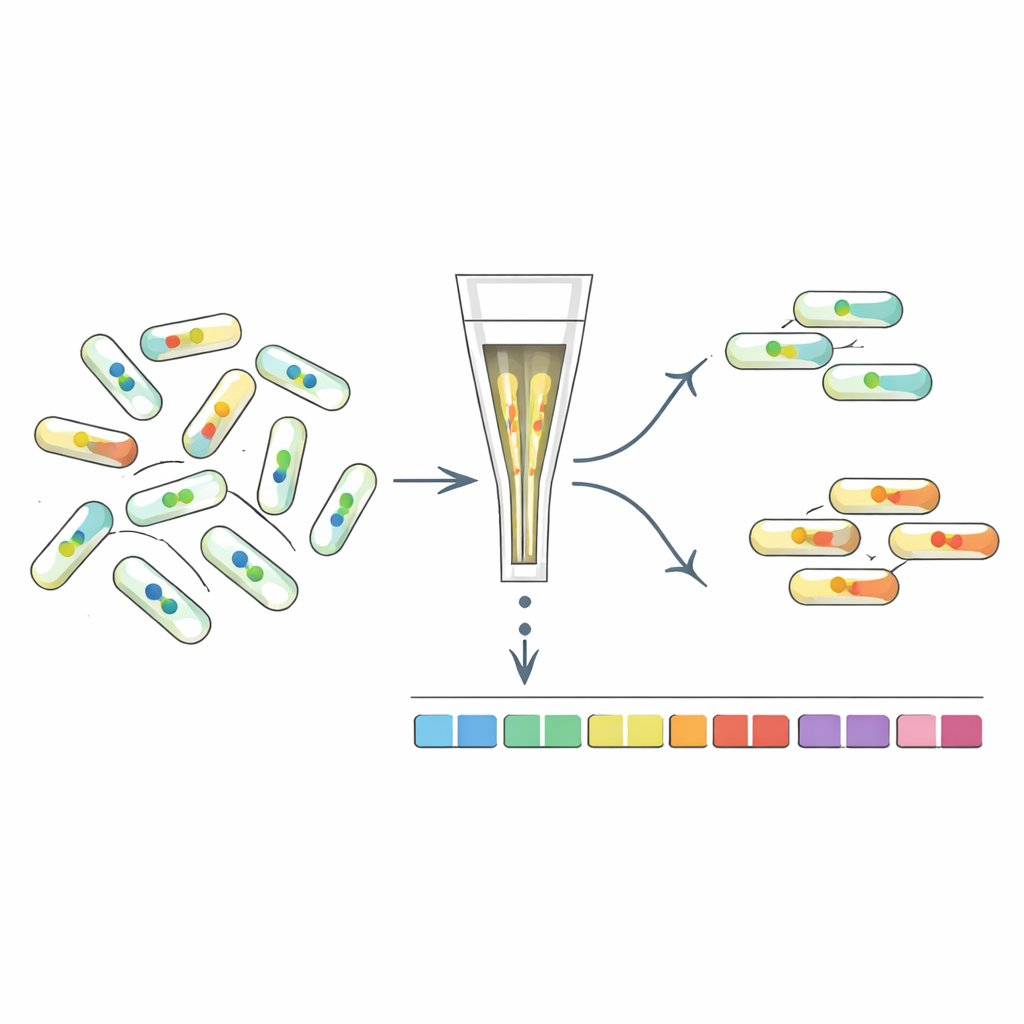
内部シグナルによる変異体のソーティング
どの遺伝子がc-di-GMPレベルを形作るかを理解するため、研究者らはセンサーとハイスループット変異体スクリーニングを結びつけた「FRET-To-Sort」を開発しました。選定したセンサーを数万のバーコード付きE. coli変異体ライブラリに導入し、細胞ソーターで異常に高いまたは低いFRET信号を示す細胞を収集しました。これらは変化したc-di-GMPを示唆します。バーコードをシーケンスすることで、これらの外れ値でどの遺伝子が破壊されているかを特定しました。既知のc-di-GMP関連酵素の変異体が濃縮されることは予想通りでしたが、細胞外膜、線毛(表面の毛状繊維)、ストレス応答、そして驚くべきことに遊泳を駆動する回転する鞭毛に関わる多くの他の遺伝子も強調されました。
鞭毛モーターは隠れた信号調節ノブ
解析は鞭毛システムの二面性を明らかにしました。鞭毛の基部構築の初期段階を阻害する変異はc-di-GMPを上昇させました。これは間接的にその分解を担う主要酵素の産生を低下させるためです。一方で、モーターの回転部を無効にしたり外部の糸状体を取り除く変異は逆の効果を示し、c-di-GMPを低下させました。さらなる実験で、鞭毛が回転できないと細胞膜電位(細胞外境界の電圧)が上昇し、この高い電位が主要なc-di-GMP合成酵素の活性を抑えることが示されました。膜電位を化学的に崩すと逆にc-di-GMPが増加しました。特定の抗体で鞭毛を物理的に詰まらせてもc-di-GMPが減少したことは、細菌がモーターの負荷を感知し、この機械的情報を生活様式の決定に変換していることを示唆します。
細菌を理解し制御するうえでの意義
総じて、これらの結果は生細胞内のc-di-GMPを標準化して測るための一連のセンサーと、この中心的スイッチに入力する遺伝的ネットワークをマッピングする強力な戦略を提供します。専門外の読者にとっての重要なポイントは、細菌が化学物質に反応するだけでなく、自分たちの小さな推進器がどれだけ回転しやすいかを「感じ取り」、それに応じて内部シグナルを調整するということです。機械的な負荷と細胞膜の電気的状態を、付着か遊泳かを支配する分子に結び付けることで、この研究は医学的・環境的に重要な微生物のバイオフィルム形成を探る、あるいは撹乱する新しい手段を開きます。
引用: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
キーワード: 細菌のセカンドメッセンジャー, バイオフィルム制御, FRETバイオセンサー, 鞭毛運動, ゲノム全体の変異体スクリーニング