Clear Sky Science · pt
Caixa de ferramentas de biossensores c-di-GMP baseados em FRET e sua aplicação FRET-To-Sort para mapeamento genômico da regulação de c-di-GMP
Como as bactérias decidem quando aderir ou nadar
As bactérias constantemente escolhem entre vagar livremente e se estabelecer em comunidades viscosas chamadas biofilmes, uma troca que molda infecções, ciclos ambientais e até incrustações industriais. Este artigo revela novas ferramentas que permitem aos cientistas observar um sinal interno chave em células bacterianas individuais em tempo real, e as utiliza para descobrir uma ligação surpreendente entre a velocidade de rotação das pequenas hélices de uma bactéria e sua decisão de formar biofilmes.
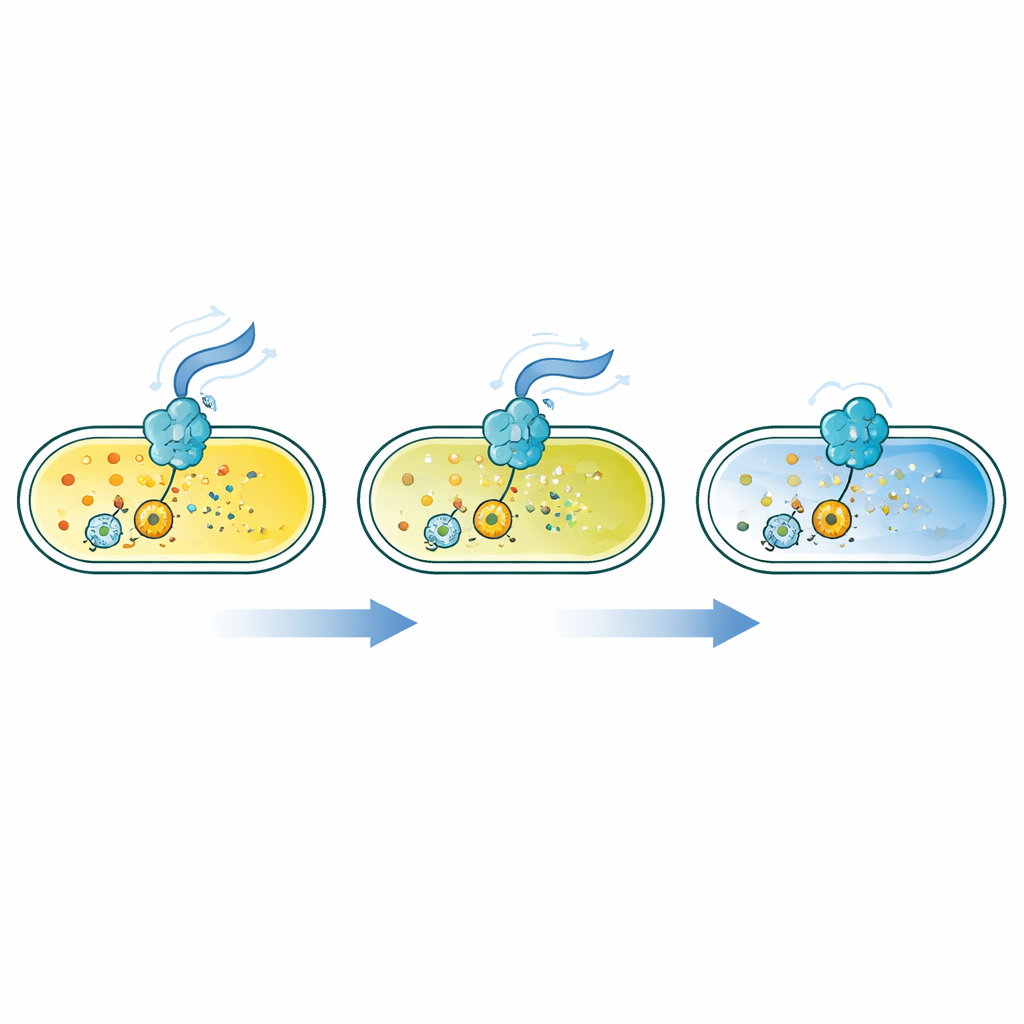
Uma molécula diminuta que muda os estilos de vida bacterianos
Muitas bactérias dependem de uma pequena molécula em anel, o c-di-GMP, como um interruptor interno. Quantidades baixas favorecem nado rápido, enquanto níveis mais altos empurram as células ao assentamento, à adesão a superfícies e à formação de biofilmes. Esse sinal é sintetizado e degradado por famílias de enzimas que respondem a nutrientes, oxigênio, estresse e mais. Até agora, porém, os pesquisadores não dispunham de um conjunto único de sensores sensíveis, rápidos e amplamente ajustáveis para ver toda a faixa de níveis de c-di-GMP dentro de células vivas, especialmente quando a molécula está presente em concentrações muito baixas.
Construindo uma caixa de ferramentas de sensores com mudança de cor versátil
Os autores projetaram uma família de sensores proteicos baseados em FRET, um processo no qual uma proteína fluorescente pode transferir energia para outra quando estão muito próximas. Eles fundiram pares de proteínas fluorescentes brilhantes a um conjunto de proteínas “leitoras” bacterianas que mudam de forma ao se ligarem ao c-di-GMP. Dependendo do projeto, essa mudança conformacional ou aproxima o par de fluorescentes ou os afasta, alterando o sinal FRET. Ao rastrear 90 proteínas leitoras diferentes em Escherichia coli, identificaram 16 sensores que respondem fortemente ao longo de uma ampla faixa de concentrações de c-di-GMP, desde cerca de dez bilionésimos de mol até um milionésimo — cobrindo os níveis baixos frequentemente encontrados em bactérias nadadoras livres, bem como níveis mais altos em biofilmes.
Observando mais de perto células individuais
Com essa caixa de ferramentas em mãos, a equipe aperfeiçoou um método de citometria de fluxo que mede FRET com precisão em milhares de células por segundo, corrigindo artefatos ópticos para que os resultados possam ser comparados entre experimentos e sensores. Confirmaram as afinidades de ligação medidas de duas maneiras: imergindo células permeabilizadas em soluções de c-di-GMP de concentração conhecida e testando sensores purificados em tubos de ensaio. Em seguida, acompanharam bactérias individuais em canais microfluídicos, descobrindo que os níveis de c-di-GMP flutuam fortemente de célula para célula e ao longo do tempo, mesmo em populações geneticamente idênticas. Sensores de alta afinidade revelaram diferenças sutis nessas faixas de baixa concentração que sensores antigos e menos sensíveis em grande parte deixavam passar.
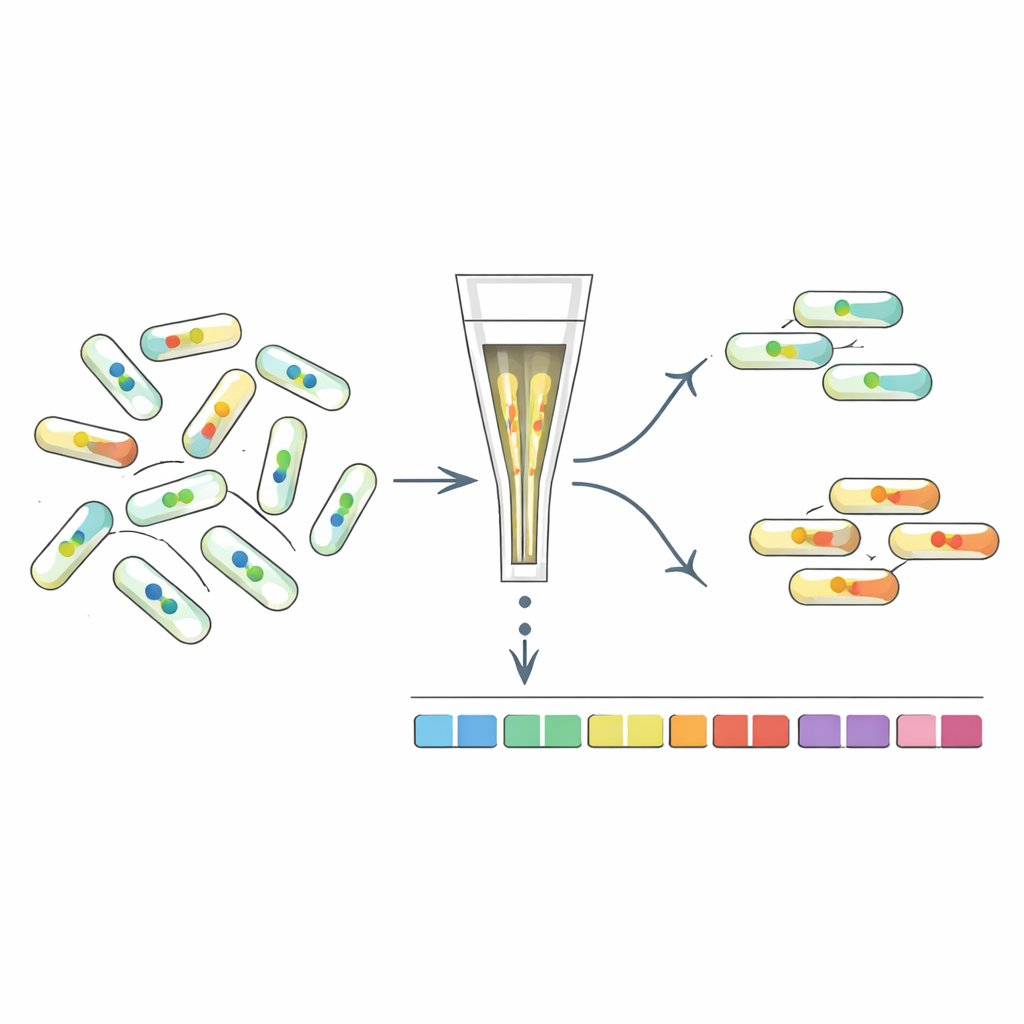
Classificando mutantes pelo seu sinal interno
Para entender quais genes moldam os níveis de c-di-GMP, os pesquisadores desenvolveram o “FRET-To-Sort”, que acopla seus sensores a uma triagem de mutantes de alto rendimento. Introduziram sensores selecionados em uma biblioteca com códigos de barras de dezenas de milhares de mutantes de E. coli, então usaram um classificador celular para coletar células com sinais FRET incomumente altos ou baixos, indicando c-di-GMP alterado. O sequenciamento dos códigos de barras revelou quais genes estavam interrompidos nesses outliers. Como esperado, mutantes em enzimas conhecidas de c-di-GMP foram enriquecidos. Mas a triagem também destacou muitos outros genes, incluindo os envolvidos na camada celular, fímbria (fibras superficiais semelhantes a pelos), respostas ao estresse e, de forma marcante, os flagelos rotativos que impulsionam a natação.
Motores flagelares como botões ocultos de sinal
A análise revelou um papel duplo para o sistema flagelar. Mutações que bloqueiam etapas iniciais na construção da base flagelar elevaram o c-di-GMP, porque indiretamente reduziram a produção de uma enzima chave que degrada a molécula. Em contraste, mutações que desativaram as partes giratórias do motor ou removeram o filamento externo tiveram o efeito oposto: reduziram o c-di-GMP. Experimentos adicionais mostraram que quando os flagelos não podem girar, o potencial de membrana da célula — a voltagem através de sua barreira externa — aumenta, e essa voltagem elevada reduz a atividade de uma importante enzima produtora de c-di-GMP. Colapsar quimicamente o potencial de membrana teve o efeito reverso, aumentando o c-di-GMP. Mesmo travar fisicamente os flagelos com anticorpos específicos reduziu o c-di-GMP, sugerindo que as bactérias percebem quão carregados estão seus motores e traduzem essa informação mecânica em decisões sobre seu estilo de vida.
O que isso significa para entender e controlar bactérias
Em conjunto, esses resultados fornecem um conjunto padronizado de sensores de c-di-GMP em células vivas e uma estratégia poderosa para mapear as redes genéticas que alimentam esse interruptor central. Para não especialistas, a principal conclusão é que as bactérias não respondem apenas a químicos; elas também “sentem” quão facilmente suas pequenas hélices giram e ajustam seus sinais internos de acordo. Ao ligar tensão mecânica e estado elétrico da membrana celular à molécula que governa aderir versus nadar, este trabalho abre novas maneiras de sondar e talvez interromper a formação de biofilmes em micróbios de importância médica e ambiental.
Citação: Wang, L., Malengo, G., Sanches-Medeiros, A. et al. Toolbox of FRET-based c-di-GMP biosensors and its FRET-To-Sort application for genome-wide mapping of c-di-GMP regulation. Nat Commun 17, 2955 (2026). https://doi.org/10.1038/s41467-026-71105-8
Palavras-chave: mensageiros secundários bacterianos, regulação de biofilme, biossensores FRET, motilidade flagelar, triagem de mutantes em escala genômica